Clear Sky Science · de
Kartierung, Entstehung und Rolle von Transposon–Gen-Chimären bei der Erweiterung der Transkriptom‑Plastizität
Verborgene Passagiere in unserer DNA
Ein großer Teil unserer DNA besteht aus uralten viralen Mitreisenden, den transponierbaren Elementen — genetischen Sequenzen, die einst wie parasitäre Tramper durch Genome sprangen. Diese Studie zeigt, dass diese alten viralen Fragmente nicht nur stummer Müll sind: Sie können sich in unsere Gene einklinken, um hybride Botschaften zu erzeugen, Zellen helfen, sich an veränderte Bedingungen anzupassen, und gelegentlich Krankheiten antreiben. Durch die Kartierung dieser Hybride während Entwicklung, Alterung und Krebs offenbaren die Autoren eine überraschende Weise, wie virale DNA bis heute die menschliche Biologie formt.
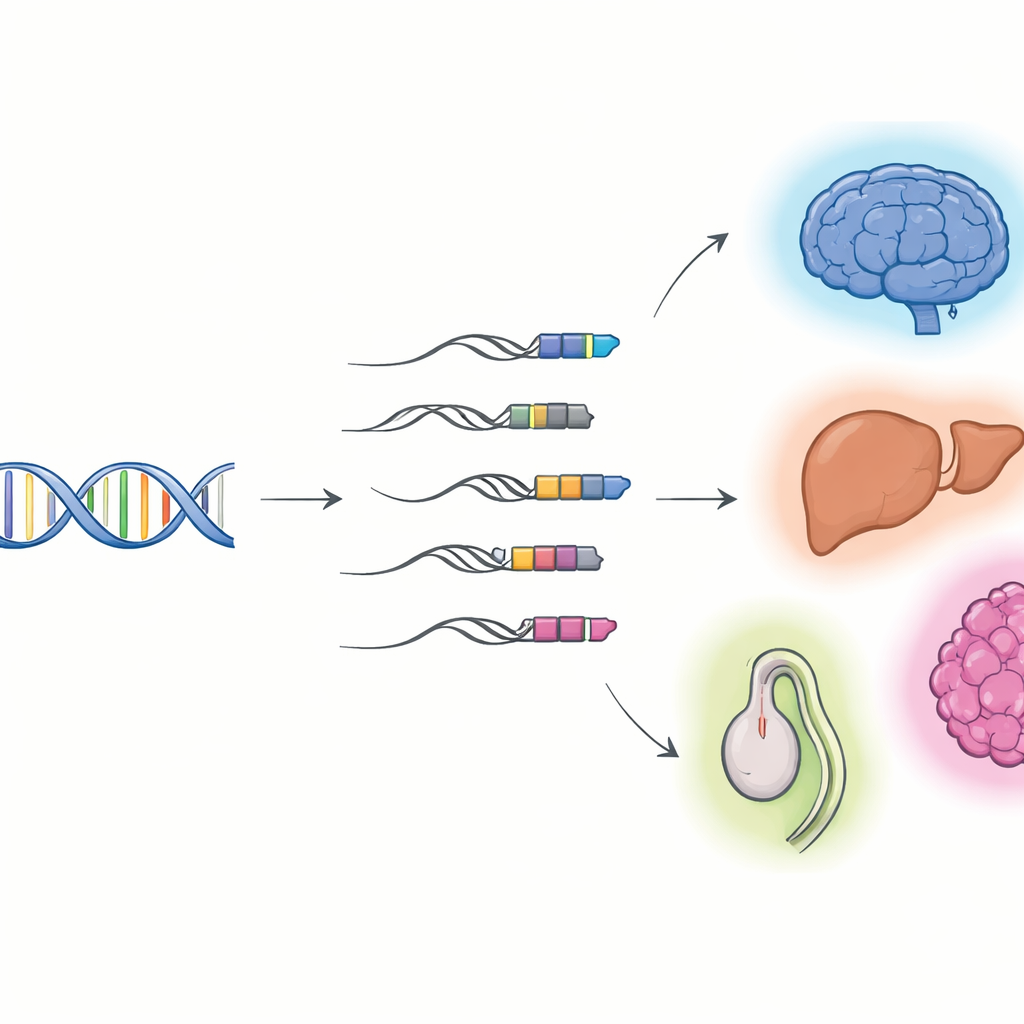
Wenn virale DNA Teil unserer Gene wird
Die Forschenden konzentrierten sich auf „TE–Gen‑Chimären“: RNA‑Moleküle, die in einem transponierbaren Element beginnen und dann in ein Wirtsgen weiterlaufen. Mithilfe von Lang‑Read‑Sequenzierung, die ganze RNA‑Moleküle end‑zu‑end erfassen kann, kombiniert mit herkömmlicher Kurz‑Read‑Sequenzierung, erstellten sie detaillierte Kataloge dieser Hybride in Maus‑ und menschlichen Zellen und Organen. Sie fanden tausende zuvor unbekannter chimerischer Transkripte, von denen die meisten nicht kodierend sind und keine Proteinvorlagen darstellen. Viele beginnen in einer Klasse viraler Überreste, den long terminal repeats (LTRs), die häufig vor Genen liegen und wie alternative An‑/Aus‑Schalter wirken können. Verschiedene Gewebe und Organe nutzen unterschiedliche Sets dieser Chimären, besonders aktiv sind Gehirn, Leber und Hoden, und ihre Nutzung verändert sich, wenn Gewebe vom fetalen zum adulten Stadium reifen.
Chimären beim Altern und im Krebs
Um zu untersuchen, wie sich diese viral–wirtlichen Hybride in realen Populationen verhalten, wertete das Team große menschliche Datensätze aus, die Dutzende Gewebe von Hunderten Menschen sowie Tumorproben abdecken. Sie identifizierten mehrere hundert hochzuverlässige Chimären, die bei verschiedenen Individuen wiederkehren. Ihre Expression variiert nicht nur zwischen Organen, sondern auch mit dem Alter: In Geweben wie Blut und Gehirn nehmen einige LTR‑getriebene Chimären bei älteren Erwachsenen ab, während sie in bestimmten peripheren Geweben zunehmen. In vielen Krebsarten sind diese LTR‑basierten Hybride in Tumoren im Vergleich zum umgebenden Normalgewebe allgemein hochreguliert, und Patientinnen und Patienten, deren Tumoren mehr davon exprimieren, haben tendenziell schlechtere Prognosen. In Datensätzen von Personen, die gegen Chemotherapie oder Immuntherapie resistent sind, liegen die durch neue LTR‑exonisierten Gene betroffenen Wege oft in Pfaden, die mit der Wirkungsweise dieser Medikamente verknüpft sind, was nahelegt, dass TE‑Chimären Tumoren helfen können, sich unter Therapiedruck umzustrukturieren.
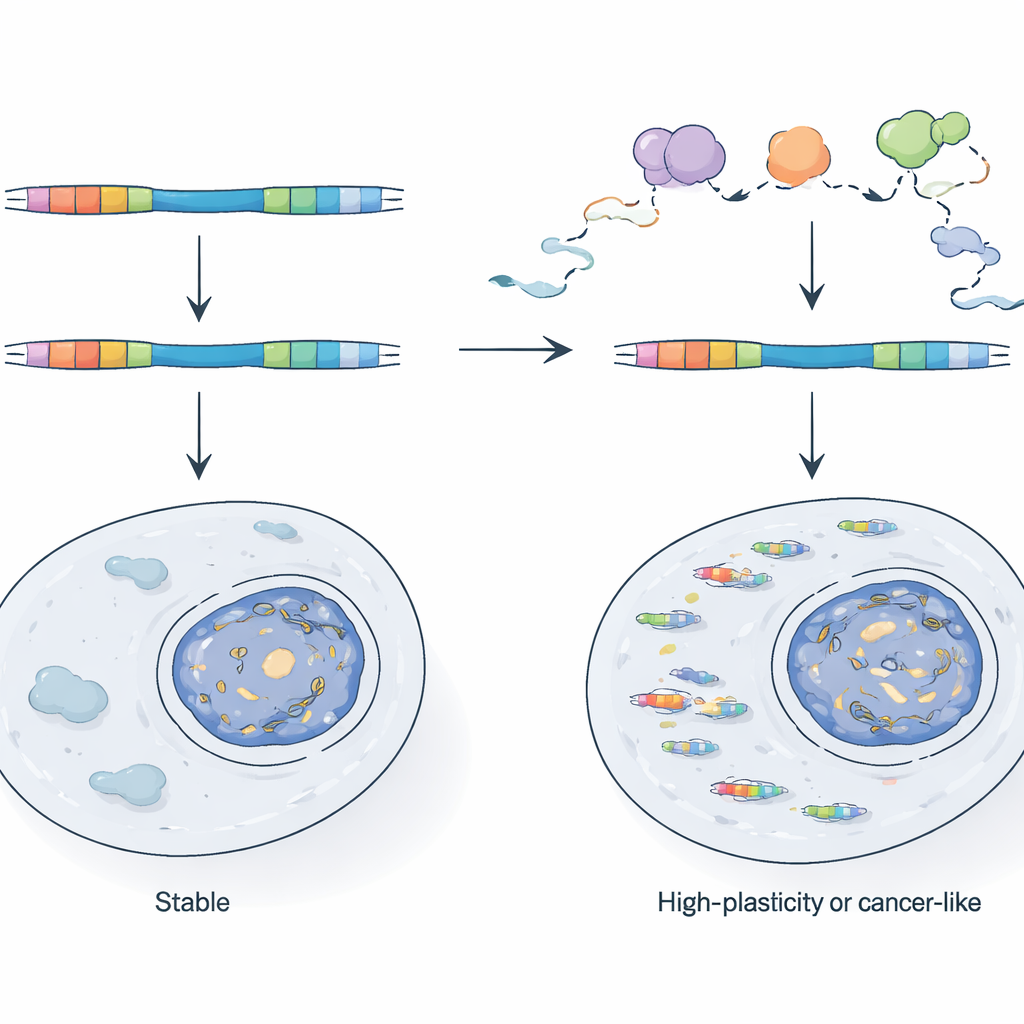
Wie Zellen virale Hybride in Schach halten
Angesichts ihrer Potenz: Warum überfluten TE‑Chimären nicht normale Zellen? Die Autorinnen und Autoren zeigen, dass Zellen auf ein RNA‑Qualitätskontrollsystem angewiesen sind, das vom nukleären Exosom‑Komplex ausgeht, um viele dieser Transkripte während ihrer Entstehung zu überwachen und zu zerstören. Wenn sie eine zentrale Exosomkomponente in Maus‑Stammzellen genetisch außer Kraft setzen, werden LTR‑getriebene Promotoren deutlich aktiver und chimerische RNAs schießen in die Höhe. Durch den Vergleich neu gebildeter RNA mit stabiler RNA zeigen sie, dass einige LTRs normalerweise deshalb kontrolliert werden, weil ihre Transkripte rasch abgebaut werden, während andere auf der Ebene der Transkriptionsinitiation reguliert sind. Diese aktiven LTRs liegen häufig in Genomregionen, die bereits zugänglich und häufig transkribiert sind, was darauf hindeutet, dass das bloße Vorhandensein in der Nähe eines aktiven Gens oder eines Antisense‑Transkripts einem viralen Fragment helfen kann, der klassischen epigenetischen Abschaltung zu entgehen.
Spleißen, Stammzellplastizität und ein viraler „Hauptschalter“
Die Geschichte wird komplexer, wenn die Spleißmaschinerie der Zelle gestört wird. Die Autorinnen und Autoren schalten mehrere zentrale Spleißfaktoren herunter oder hemmen das Spleißosom chemisch und beobachten ein gemeinsames Ergebnis mit dem Verlust des Exosoms: einen starken Anstieg LTR‑getriebener Chimären und von kurzen, intron‑armen Genen. Zu den Gewinnern zählt MERVL, ein endogenes Retrovirus, das in sehr frühen Maus‑Embryonen aktiv ist. Wenn MERVLs interne Sequenz und die davon abhängigen Transkriptionsfaktoren hochreguliert werden, verschieben sich Stammzellen in einen stärker „totipotenten‑ähnlichen“ Zustand, ähnlich frühen embryonalen Zellen, die alle Gewebe bilden können. Umgekehrt dämpft der Abbau von MERVL‑RNA mit antisense Oligonukleotiden diese Verschiebung und reduziert die Aktivität von LTR‑Promotoren, was darauf hindeutet, dass MERVL als Hauptschalter fungiert, der ein breiteres Netzwerk von TE‑Chimären und Zellzustandsplastizität auslösen kann.
Virale Innovationen über die Evolution hinweg
Beim Blick über viele Säugetiergenome hinweg verfolgt das Team, wann verschiedene TE‑Familien begonnen haben, Exons an Wirtsgene zu spenden. Sowohl beim Menschen als auch bei der Maus neigen relativ junge LTR‑Familien besonders dazu, Chimären in der „Sense“‑Orientierung zu bilden, die als Teil von Wirts‑Transkripten lesbar sind. Dieses Muster legt nahe, dass neue Wellen von TE‑Insertionen wiederholt Rohmaterial in Genregulationsnetzwerke eingespeist haben. Statt nur schädlich zu sein, können diese Insertionsereignisse von der Transkriptions‑ und Abbaumaschinerie der Zelle geprüft werden: Die meisten werden stillgelegt oder abgebaut, aber eine Minderheit landet am richtigen Ort und im richtigen Kontext, um als nützliche regulatorische Elemente oder neue Genstarts umgenutzt zu werden.
Warum diese viralen Überreste wichtig sind
Für Nicht‑Spezialisten zeigt diese Arbeit, dass ein großer und einst abgetaner Teil unseres Genoms aktiv beeinflusst, wie Gene gelesen werden, wie Zellen ihre Identität ändern und wie Krankheiten verlaufen. Uralte virale Sequenzen können zu alternativen „Vordertüren“ von Genen werden und chimerische RNAs produzieren, die normalerweise von zellulären Aufräumsystemen überwacht werden. Wenn diese Überwachung oder das normale Spleißen versagt, können diese Hybride aufschießen, Stammzellen in flexiblere Zustände schubsen oder Tumoren helfen, sich anzupassen und Therapien zu widerstehen. Über Millionen Jahre hat die Evolution wiederholt an diesen viralen Fragmenten getüftelt, viele von ihnen von genomischen Parasiten zu Bausteinen regulatorischer Komplexität umgewandelt — und uns ein Transkriptom hinterlassen, das weit plastischer und dynamischer ist, als eine einfache Liste von Genen vermuten ließe.
Zitation: Cheon, Y., Alvstad, E.G., Torre, D. et al. Transposable element–gene chimera cartography, origination and role in enhancing transcriptome plasticity. Nat Struct Mol Biol 33, 448–463 (2026). https://doi.org/10.1038/s41594-026-01757-z
Schlüsselwörter: transponierbare Elemente, chimerische Transkripte, RNA-Überwachung, Stammzellplastizität, Krebsentwicklung