Clear Sky Science · de
Stressanpassung des mitochondrialen Proteinimports durch OMA1-vermittelte Degradation von DNAJC15
Wie unsere Zellen reagieren, wenn ihre Kraftwerke unter Stress stehen
Jede Zelle in Ihrem Körper ist auf winzige Strukturen namens Mitochondrien angewiesen, die Nahrung in nutzbare Energie umwandeln. Wie Miniaturfabriken importieren Mitochondrien ständig neue Bauteile — Proteine, die anderswo in der Zelle hergestellt wurden — um ihre Maschinen am Laufen zu halten. Diese Arbeit zeigt, wie Zellen bei Stress oder Schädigung der Mitochondrien gezielt die Protein-Importpipeline drosseln. Dadurch schützen sie sich vor Überlastung und koordinieren eine breitere Stressantwort, die nicht nur die Mitochondrien, sondern auch ein weiteres zentrales Kompartiment, das endoplasmatische Retikulum, einbezieht.
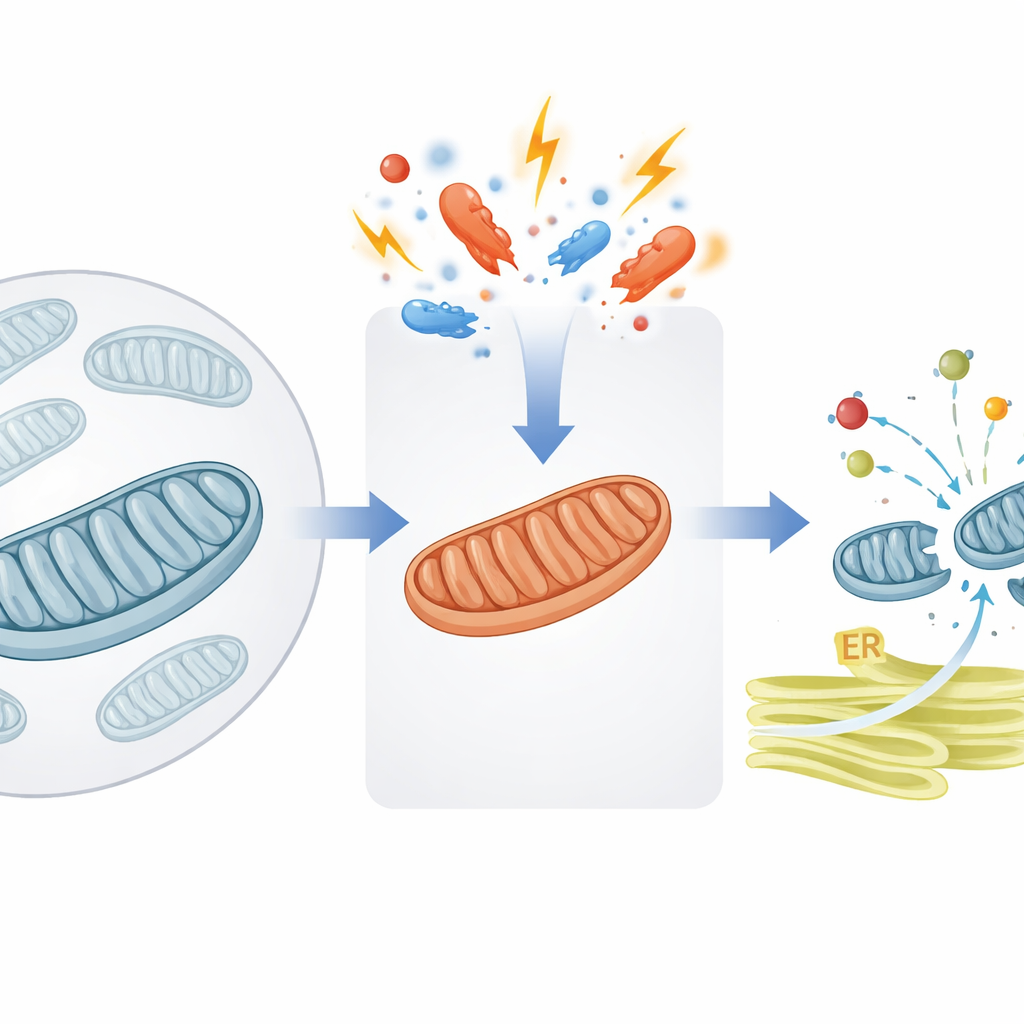
Ein Sicherheitsventil für den mitochondrialen Proteinverkehr
Mitochondrien sind auf tausende Proteine angewiesen, die zuerst im Hauptkompartiment der Zelle synthetisiert und dann hineingeschafft werden. Die Autoren konzentrieren sich auf ein entscheidendes Tor in der inneren Mitochondrienmembran, das von einem Hilfsprotein namens DNAJC15 unterstützt wird. Unter normalen Bedingungen hilft DNAJC15 dabei, neue Protein-»Pakete« durch den Importkanal in das Mitochondrieninnere zu ziehen, wo viele von ihnen Teil der energieerzeugenden Maschinerie der oxidativen Phosphorylierung (OXPHOS) werden. Die Studie zeigt, dass die Zelle bei mitochondrialem Stress — etwa bei gestörter Energieproduktion oder veränderten Membraneigenschaften — einen molekularen Schalter umlegt, der bestimmt, wie viel Protein das Organell noch aufnehmen will.
OMA1: der stressaktivierte Schneider
Im Zentrum dieses Schalters steht ein stresssensitives Enzym namens OMA1, das in der inneren Mitochondrienmembran verankert ist. Wenn Mitochondrien in Schwierigkeiten geraten, wird OMA1 aktiv und schneidet DNAJC15 an einer spezifischen Position nahe dessen N‑Ende. Dieser Schnitt erzeugt eine kürzere Form von DNAJC15, die rasch von einem anderen mitochondrialen Enzymkomplex, dem m‑AAA‑Protease, abgebaut wird. Das gesamte, importkompetente DNAJC15 geht so verloren. Die Autoren zeigen, dass Zellen ohne DNAJC15 oder solche, in denen DNAJC15 nach OMA1‑Aktivierung schnell zerstört wird, eine verringerte Fähigkeit haben, neue Proteine in die Mitochondrien aufzunehmen, insbesondere solche, die zum Aufbau und Erhalt der OXPHOS‑Komplexe nötig sind.
Energieaufbau verlangsamen, um sich an den Zustand der Mitochondrien anzupassen
Mit großflächigen Proteinmessungen und Importassays fand das Team heraus, dass DNAJC15 besonders wichtig ist, um das Mitochondrieninnere mit Proteinen zu versorgen, die an Genexpression und am Zusammenbau der Atmungskette beteiligt sind. Fehlt DNAJC15, akkumulieren diese Proteine langsamer in den Mitochondrien, und die Fähigkeit der Organellen, Sauerstoff zu verbrauchen und Energie zu erzeugen — gemessen an isolierten Mitochondrien — nimmt ab, besonders hinsichtlich Komplex I der Atmungskette. Eine weitere Komponente des Importkanals, TIMM17A, arbeitet eng mit DNAJC15 zusammen: Gehen beide verloren, zeigen sich besonders ausgeprägte Defekte bei den Mengen mitochondrialer ribosomaler Proteine und OXPHOS‑Komponenten. Zusammen deuten diese Befunde darauf hin, dass die OMA1‑vermittelte Zerstörung von DNAJC15 ein Mechanismus ist, um den Aufbau neuer Energiemaschinerie vorübergehend zu drosseln, bis sich das Organell erholt.
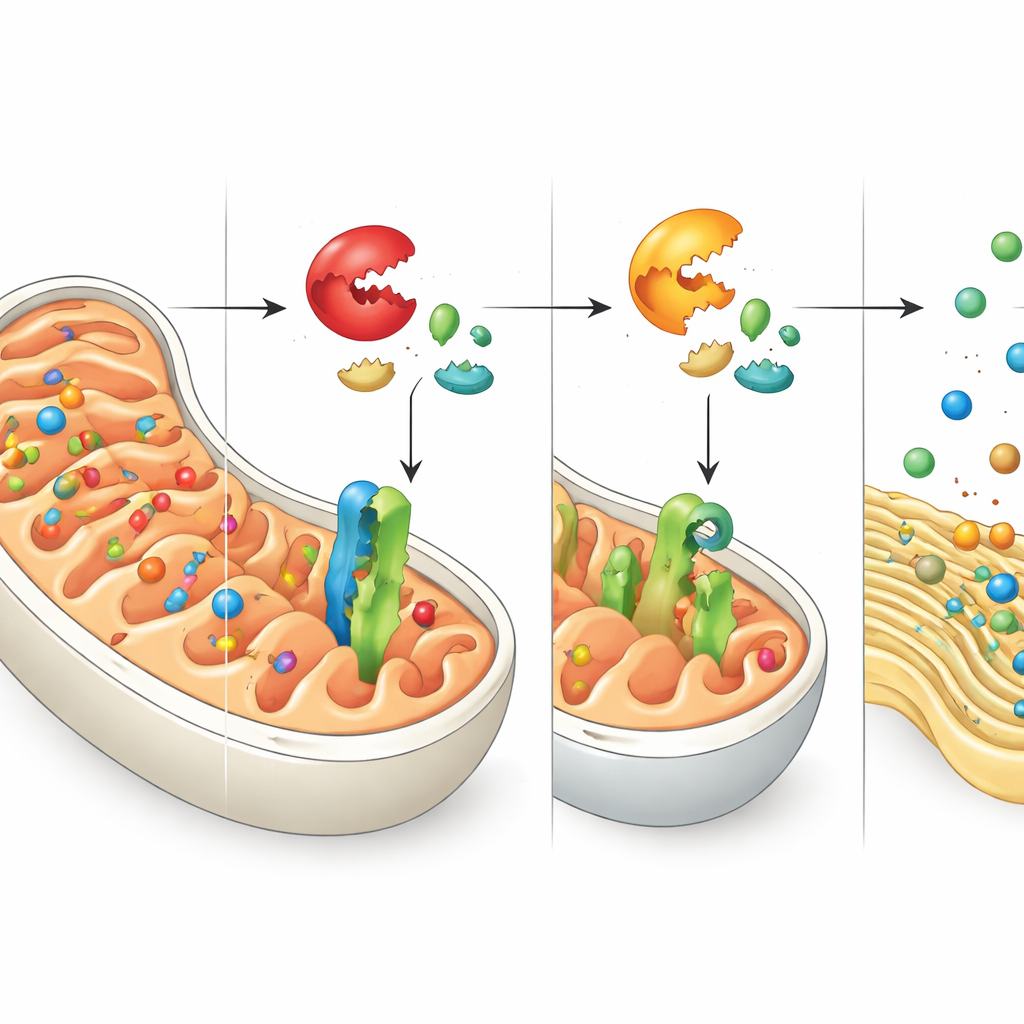
Falsch zugestellte Pakete und ein Hilferuf ans ER
Die Abschaltung von DNAJC15 verhindert nicht, dass die Zelle mitochondriale Proteine herstellt — sie verhindert hauptsächlich, dass diese an ihrem vorgesehenen Bestimmungsort ankommen. Die Autoren verfolgten, wohin diese gestrandeten Proteine gelangen, und stellten fest, dass viele im endoplasmatischen Retikulum (ER) landen, einem Netzwerk von Membranen, das normalerweise hilft, verschiedene Proteine zu falten und zu verarbeiten. Diese fehlgeleiteten mitochondrialen Proteine lagern sich in ER‑Membranen ein und stören das dortige Gleichgewicht der Qualitätskontrolle. Als Reaktion aktiviert die Zelle ein Schutzprogramm, bekannt als die Antwort auf entfaltete Proteine (unfolded protein response), spezifisch über einen Ast, der vom Sensor ATF6 gesteuert wird. Diese Antwort erhöht die Kapazität des ER, mit fehlgefalteten oder fehlplatzierten Proteinen umzugehen, und offenbart damit eine enge Koordination zwischen mitochondrialen und ER‑Stresssystemen.
Ein abgestimmter Bremsvorgang zum Schutz der Zelle
Insgesamt zeichnet die Studie das Bild eines eingebauten Bremssystems für die mitochondriale Biogenese. Wenn Mitochondrien unter Stress stehen, trimmt OMA1 und führt indirekt zur Zerstörung von DNAJC15, wodurch der Zustrom neuer, energiebezogener Proteine in beeinträchtigte Organellen reduziert wird. Einige dieser Proteine werden vorübergehend im ER gepuffert, das seinerseits eine Schutzantwort startet. Indem die Importkapazität der Mitochondrien an den Organellzustand gekoppelt wird und das ER als Auffangstelle für überschüssige Proteine dient, können Zellen verhindern, dass beschädigte Mitochondrien verstopfen, und gewinnen Zeit, um sie zu reparieren oder zu entfernen. Für einen Laien zeigt diese Arbeit, wie tief integriert unsere zellulären Qualitätskontrollsysteme sind: Selbst kleinste Fehltritte in einem Kompartiment werden von anderen wahrgenommen und ausgeglichen, um die Energieproduktion — und damit das Leben selbst — auf Kurs zu halten.
Zitation: Kroczek, L., Nolte, H., Lasarzewski, Y. et al. Stress adaptation of mitochondrial protein import by OMA1-mediated degradation of DNAJC15. Nat Struct Mol Biol 33, 499–511 (2026). https://doi.org/10.1038/s41594-026-01756-0
Schlüsselwörter: mitochondrialer Stress, Proteinimport, zelluläre Qualitätskontrolle, oxidative Phosphorylierung, endoplasmatisches Retikulum