Clear Sky Science · de
Struktur und Mechanismus des antiphagenen Retrons Eco2
Wie Bakterien eine eingebaute „Selbstzerstörung“ gegen Viren einsetzen
Viren, die Bakterien infizieren — sogenannte Phagen — sind überall anzutreffen, von den Ozeanen bis zu unserem Darm. Diese Studie legt offen, wie ein winziges genetisches „Gadget“ in einigen Bakterien, das Eco2-Retron, ihnen hilft, einen Phagenangriff zu überstehen. Durch die Aufklärung der 3D-Struktur von Eco2 und des Mechanismus seiner Aktivierung beschreibt die Arbeit eine neue Art von Notfallabwehr: Erkennt die Zelle eine Infektion, schaltet sie gezielt die eigene Proteinsynthese ab, um die Ausbreitung des Virus zu verhindern.
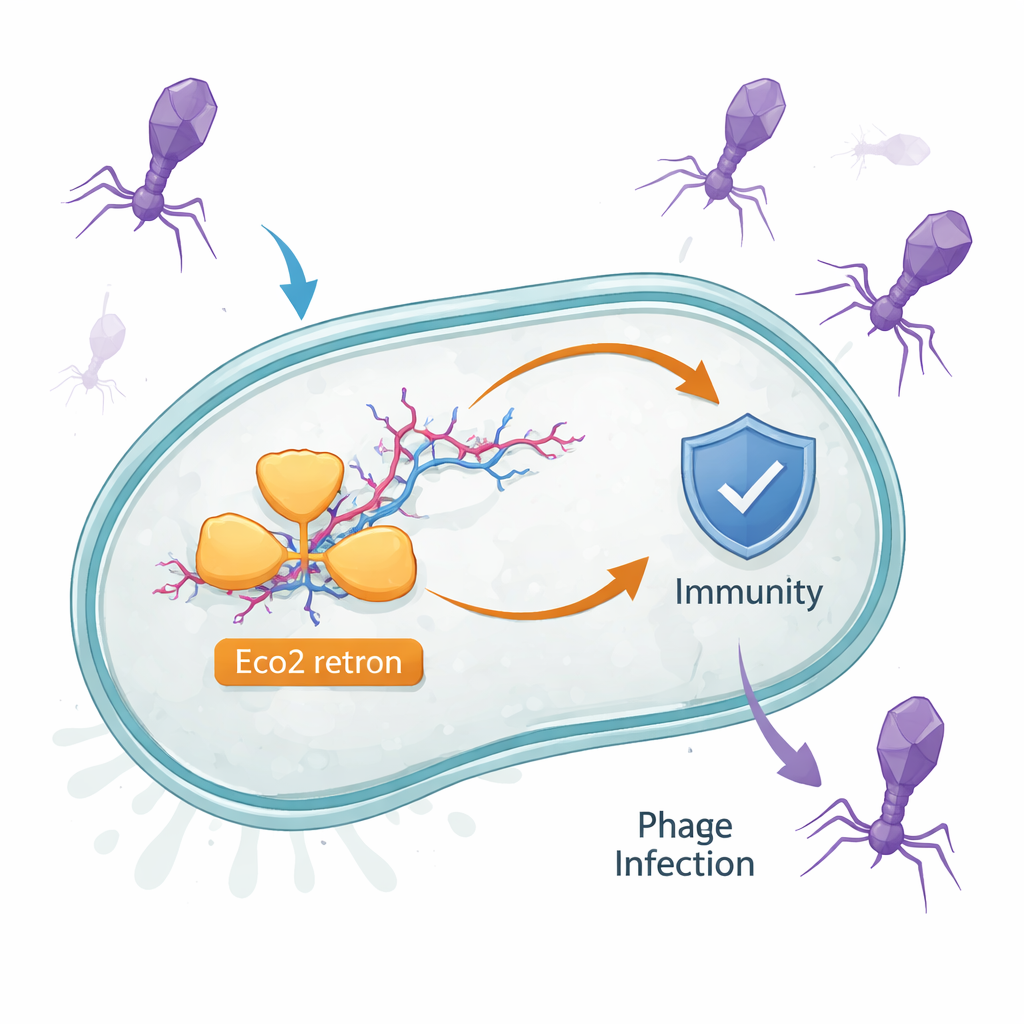
Ein verborgenes DNA–RNA-Gadget in bakteriellen Zellen
Bakterien tragen viele kleine Abwehrsysteme, die erst während einer Infektion aktiv werden. Eco2 ist eines davon. Es kommt in Escherichia coli vor und besteht aus einem einzigen Protein, das sowohl RNA in DNA umschreiben kann als auch Nukleinsäuren schneiden kann. Dieses Protein arbeitet mit einem ungewöhnlichen Molekül zusammen, der msDNA — einem Hybrid aus RNA und einzelsträngiger DNA, der wie ein verzweigter Zweig aussieht. Frühere Hinweise deuteten darauf hin, dass Retron-Systeme wie Eco2 gegen Phagen schützen, doch wie ein einzelnes Protein und seine msDNA-Partnerin eine Infektion erkennen und darauf reagieren, war unklar.
Breiter Schutz gegen viele Viren
Die Forschenden fragten zunächst, wie gut Eco2 Bakterien gegen eine Vielzahl von Phagen schützt. Durch den Einsatz einer großen, divers zusammengesetzten Virussammlung gegen Eco2-tragende Zellen fanden sie, dass Eco2 viele Phagenfamilien blockiert, aber nicht alle. Bei den Phagen, die entkamen, zeigten die Genome Mutationen in Genen für virale DNA-schneidende Enzyme, besonders in einem namens DenB. Dieses Muster legt nahe, dass Eco2 durch bestimmte virale Nukleasen ausgelöst wird: Sind diese Enzyme durch Mutation inaktiviert, kann das Virus der Abwehr entkommen.
Ein dreilappiger molekularer Schild
Um zu sehen, wie Eco2 aufgebaut ist, nutzte das Team kryogene Elektronenmikroskopie, um den Komplex nahezu in atomaren Details zu visualisieren. Eco2 agiert nicht allein: Drei Kopien des Eco2-Proteins assemblieren zu einer dreilappigen, shurikenähnlichen Struktur. Die verzweigte msDNA zieht sich durch und um diese drei Proteine und verbindet sie mechanisch. Dabei bildet die msDNA eine dreiweggabel in der Mitte und „käfigt“ den Nuklease‑Teil von Eco2, indem sie dessen Schnittstelle blockiert. Wasserstoff‑Deuterium‑Austausch‑Experimente, die zeigen, wie flexibel verschiedene Regionen sind, belegten, dass die Bindung der msDNA den Komplex versteift und stabilisiert. In diesem Ruhestandard ist Eco2 effektiv in der AUS‑Position verriegelt.
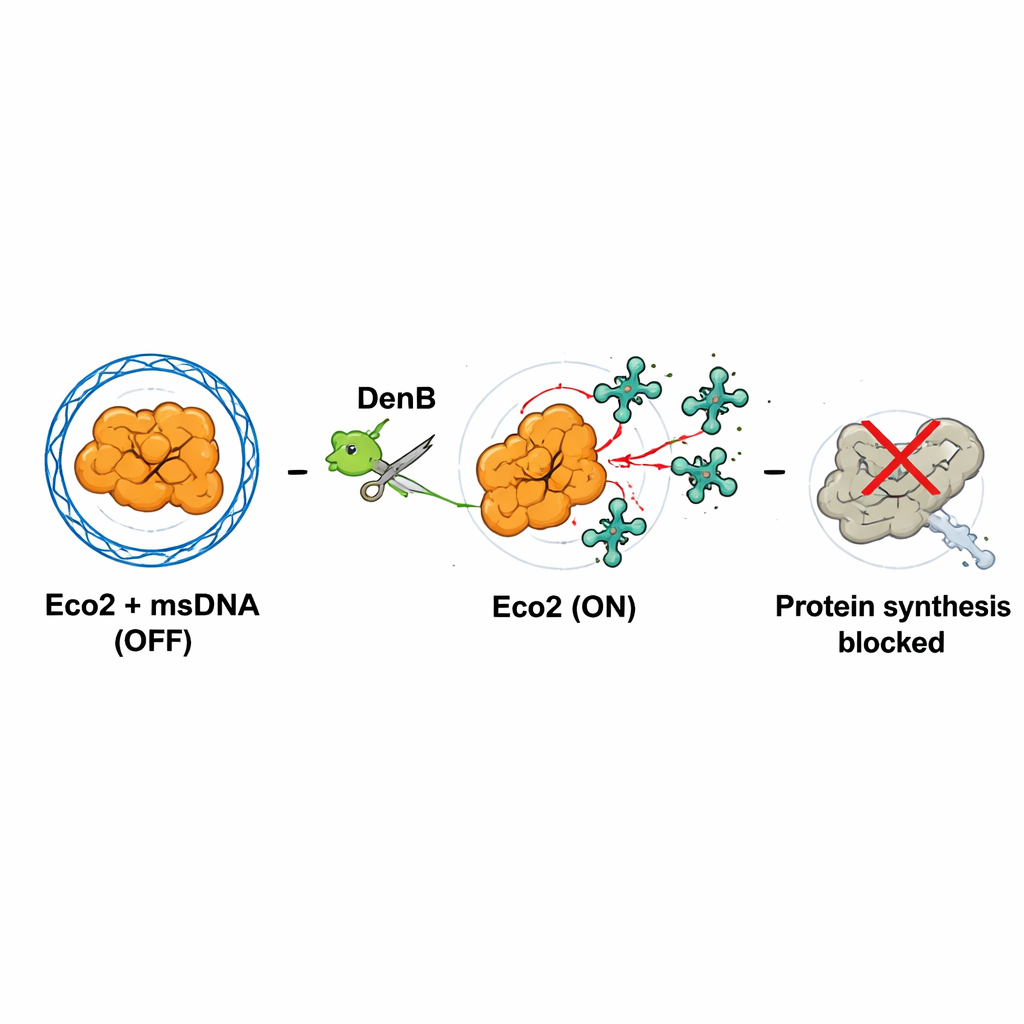
Viraler Angriff schaltet das System ein
Der Schlüssel zur Aktivierung ist die Zerstörung der msDNA. Das virale Enzym DenB, das normalerweise dem Phagen bei der DNA‑Verarbeitung hilft, schneidet auch in die msDNA, die Eco2 einsperrt. Die Autoren ahmten diesen Prozess mit gereinigtem DenB und einem Standard‑DNA‑Schneideenzym nach und beobachteten, dass nach dem Durchtrennen der msDNA die Nuklease‑Stelle von Eco2 freigelegt wird und sich in eine aktive Konfiguration umordnet. Hochauflösende Strukturen dieses „AN‑Zustands“ zeigten, dass eine kritische Aminosäure in der Nuklease‑Tasche in eine Position wandert, in der sie ein Magnesiumion richtig koordinieren kann — essentiell für das Schneiden von RNA. Somit zieht die virale Nukleaseaktivität, die eigentlich das Wirts‑DNA‑Management verändern soll, versehentlich den Sicherungsstift von Eco2.
Eigene tRNAs der Zelle werden zerschnitten, um das Virus zu stoppen
Was schneidet das aktivierte Eco2? Mithilfe zellfreier Systeme, radioaktiver Markierung und RNA‑Sequenzierung bei echten Infektionen fanden die Forschenden heraus, dass Eco2 vor allem Transfer‑RNAs (tRNAs) nickt — jene Adaptormoleküle, die Aminosäuren in das Ribosom liefern. Eco2 schneidet diese tRNAs in der Nähe ihrer Enden, besonders an Stellen, die reich an der Base Cytosin sind. Sind viele tRNAs beschädigt, können Ribosomen keine Proteine mehr effizient herstellen. In Anwesenheit von DenB und aktivem Eco2 sank die Produktion von grünem Fluoreszenzprotein stark, und sowohl bakterielle als auch phagische RNAs wurden zersetzt. Diese Abschaltung entspricht wahrscheinlich einer „abrupten Infektionsbeendigung“ (abortive infection): die infizierte Bakterienzelle opfert ihr eigenes Wachstum, damit das Virus sich nicht erfolgreich replizieren und ausbreiten kann.
Warum das auch über Bakterien hinaus Bedeutung hat
Die Arbeit zeigt, wie ein minimales Retron ein virales Enzym erkennt, vom inaktiven in den aktiven Zustand umschaltet und dann die Proteinsynthese durch das Anvisieren von tRNAs lahmlegt. Für Nicht‑Spezialisten ist die zentrale Idee: Bakterien schlagen Viren manchmal nicht durch punktgenauen Angriff, sondern dadurch, dass sie im richtigen Moment ihr eigenes zelluläres System herunterfahren. Über das Verständnis mikrobieller Immunität hinaus liefern die detaillierten Strukturen von Eco2 und seinem msDNA‑Gerüst eine Blaupause für Ingenieure, die Retron‑Systeme als Werkzeuge für Genome‑Editing und synthetische Biologie umnutzen wollen.
Zitation: Jasnauskaitė, M., Juozapaitis, J., Liegutė, T. et al. Structure and mechanism of antiphage retron Eco2. Nat Struct Mol Biol 33, 330–340 (2026). https://doi.org/10.1038/s41594-026-01754-2
Schlüsselwörter: Bakteriophagen-Immunität, Retron Eco2, Bakterielle antivirale Abwehr, tRNA-Spaltung, msDNA