Clear Sky Science · de
Struktur und Funktion des Hefe‑Aminosäure‑sinnenden SEAC–EGOC‑Superkomplexes
Wie Zellen entscheiden, wann sie wachsen
Jede Zelle muss ständig abwägen, ob sie sich Wachstum leisten kann oder Ressourcen sparen sollte. Diese Entscheidung hängt stark von Aminosäuren ab, den Bausteinen der Proteine und einer wichtigen Stickstoffquelle. Diese Arbeit legt in bemerkenswerter struktureller Detailfülle offen, wie Hefezellen die Verfügbarkeit von Aminosäuren über einen riesigen molekularen Verbund wahrnehmen und diese Information nutzen, um einen zentralen Wachstumsschalter, genannt TORC1, ein‑ oder auszuschalten. Weil dieselbe Schaltungslogik in menschlichen Zellen erhalten ist und mit Krebs sowie Stoffwechselerkrankungen verknüpft ist, bieten Erkenntnisse aus Hefe Einblicke, wie auch unsere Zellen beurteilen, ob die Bedingungen für Wachstum günstig sind.
Ein filigranes Zentrum am Recycling‑Zentrum der Zelle
In Hefe sitzt ein zentrales Entscheidungszentrum namens SEAC auf der Membran des Vakuols, eines Organells, das als Recycling‑Zentrum der Zelle fungiert. Dort trifft es auf einen weiteren Komplex, EGOC, der Informationen über Aminosäurespiegel weiterleitet. Gemeinsam geben sie Signale an TORC1, den Hauptwachstumsschalter. SEAC besteht aus zwei funktionalen Hälften: SEACIT, das TORC1 ausschalten kann, und SEACAT, von dem man lange annahm, es halte SEACIT in Schach. Die Autoren nutzten hochaufgelöste Kryo‑Elektronenmikroskopie, um das vollständige SEAC in Bindung an EGOC zu visualisieren und eine Momentaufnahme dieses molekularen Zentrums genau dort einzufangen, wo Signalübertragung stattfindet – an der Vakuolmembran. 
Die molekulare Architektur aus nächster Nähe
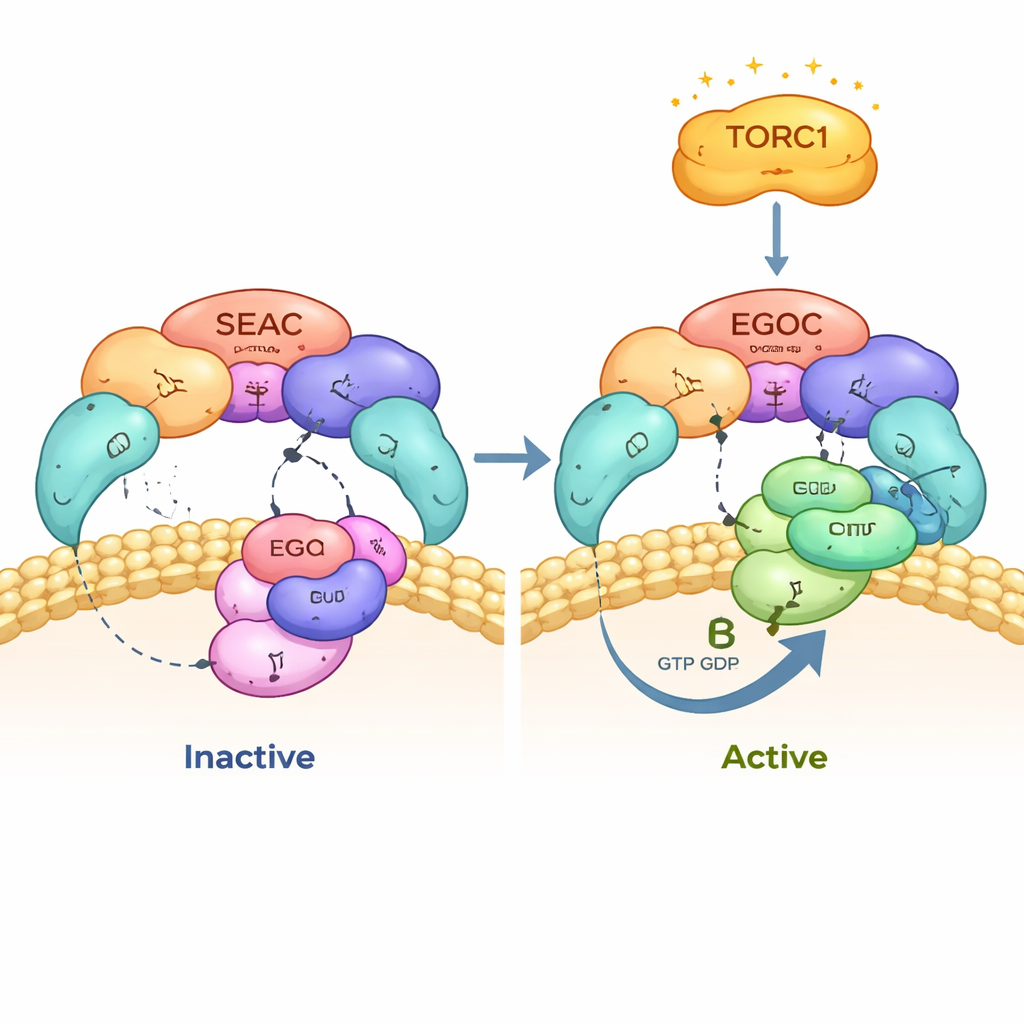
Die Struktur zeigt SEAC als einen großen Kern aus SEACAT‑Untereinheiten, von dem zwei flexible „Flügel“ aus SEACIT ausgehen. Jeder Flügel kann ein EGOC‑Komplex binden, sodass ein einzelnes SEAC zwei Signale gleichzeitig aufnehmen kann. Auffällig ist, dass EGOC nur an den Flügeln anhaftet und nicht am Kern, und dass sich die Gesamtform von SEAC kaum ändert, wenn EGOC gebunden ist. Das zeigt, dass SEACAT die aktive Stelle von SEACIT nicht physisch blockiert und EGOC nicht am Andocken hindert. Die Orientierung des Komplexes an der Vakuolmembran positioniert zudem den SEAC‑Kern zum Zytoplasma hin, wo er mit zusätzlichen Regulatoren interagieren kann, während die Flügel dicht an der Membran liegen und ideal positioniert sind, um EGOC und andere membranverankerte Partner zu kontaktieren.
Wie SEAC das richtige Signal auswählt
Die Autoren fokussierten die Kontakte zwischen SEAC und EGOC und fanden, dass SEAC nur die „aktive“ Form von EGOC erkennt, in der einer seiner kleinen GTPasen, Gtr1, ein GTP‑ähnliches Nukleotid trägt, während sein Partner Gtr2 GDP gebunden hat. SEACIT stellt einen katalytischen „Finger“ bereit, der in die Nukleotidtasche von Gtr1 greift und den GTP‑Abbau beschleunigt, wodurch EGOC von einem aktiven in einen inaktiven Zustand umgeschaltet wird. Detaillierte Kryo‑EM‑Kartierungen und Mutationsversuche zeigen, dass dieser katalytische Finger und eine benachbarte Hilfsrestseite für die Interaktion und das korrekte Erkennen des Nukleotidzustands unerlässlich sind. Wenn die Autoren diese Schlüsselreste veränderten, lokalisierte sich SEAC nicht mehr richtig an der Vakuole und EGOC konnte nicht produktiv interagieren.
Schnelle versus langsame Kontrolle des Wachstumsschalters
Um die Bedeutung für die lebende Zelle zu verstehen, verfolgten die Forscher die TORC1‑Aktivität über die Zeit, nachdem Aminosäuren entzogen und dann wieder zugeführt wurden. In normalen Zellen schaltet TORC1 innerhalb weniger Minuten nach Stickstoffentzug schnell ab und geht nach Rückkehr der Aminosäuren rasch wieder an. Wurde der katalytische Finger von SEACIT deaktiviert oder SEACIT‑Untereinheiten entfernt, reagierte TORC1 in diesem frühen Zeitfenster kaum. Dasselbe galt, wenn sowohl Gtr1 als auch Gtr2 entfernt wurden, was zeigt, dass das SEAC–EGOC‑Paar der dominante, schnelle Weg für die Aminosäurekontrolle von TORC1 ist. Allerdings stellte sich nach späteren Zeitpunkten – rund nach einer halben Stunde – die TORC1‑Aktivität auch in diesen Mutanten langsam wieder ein, was darauf hindeutet, dass in Zellen ein separater, langsamerer Weg zu TORC1 unabhängig von diesem GTPase‑System ebenfalls aktiv ist.
Eine überraschende Rolle für eine entfernte Untereinheit
Eine besonders interessante Beobachtung betrifft Sea2, eine SEACAT‑Komponente mit einer flexiblen „Propeller“‑Domäne, die aus dem Kern herausragt. Entfernen von Sea2 oder nur seines Propellers erzeugte Signaldefekte, die fast identisch waren mit denen, die beim Verlust der katalytischen Aktivität von SEAC beobachtet wurden: TORC1 reagierte träge auf sowohl Aminosäureentzug als auch Wiederzufuhr. Dabei sitzt Sea2 weit entfernt von der katalytischen Stelle und berührt die SEACIT‑Flügel nicht direkt, was eine einfache Blockierungsmechanik unwahrscheinlich macht. Genetische Experimente, die den Verlust von Sea2 mit einer katalytisch inaktiven SEAC‑Variante kombinierten, deuteten darauf hin, dass ein vollständig ein‑ oder ausgeschaltetes GAP‑Aktivitätsniveau die schnelle Reaktion stört, während eine intermediate Regulation erforderlich ist. Die Autoren schlagen vor, dass Sea2s Propeller als Andockplattform für einen unbekannten Faktor fungiert, der die Aktivität von SEACIT dämpft und es den Zellen ermöglicht, TORC1 feinzujustieren, statt es dauerhaft abzuschalten.
Was das für Entscheidungen über Zellwachstum bedeutet
Insgesamt stellt die Studie SEAC nicht als zwei gegensätzliche Einheiten dar, sondern als eine einzige, integrierte Maschine, deren katalytischer Flügel (SEACIT) und struktureller Kern (SEACAT) zusammenarbeiten, um Aminosäuren zu erkennen und den Wachstumsschalter TORC1 schnell anzupassen. Die enzymatische Wirkung von SEACIT auf EGOC liefert die schnelle, präzise Kontrolle, während Sea2s Propeller wahrscheinlich Regulatoren rekrutiert, die diese Aktivität modulieren. Gleichzeitig sorgen langsamere, parallele Wege dafür, dass TORC1 langfristig weiterhin den Nährstoffstatus widerspiegelt, selbst wenn der primäre Sensor gestört ist. Da eng verwandte Komplexe die gleiche Aufgabe in menschlichen Zellen erfüllen, beleuchten diese Erkenntnisse aus der Hefe, wie unsere eigenen Zellen Wachstum und Nährstoffangebot ausbalancieren — mit Relevanz für das Verständnis von Krankheiten, in denen TORC1‑Signalgebung gestört ist.
Zitation: Tafur, L., Bonadei, L., Zheng, Y. et al. Structure and function of the yeast amino acid-sensing SEAC–EGOC supercomplex. Nat Struct Mol Biol 33, 488–498 (2026). https://doi.org/10.1038/s41594-026-01746-2
Schlüsselwörter: Aminosäureerkennung, TORC1‑Signalgebung, SEAC GATOR‑Komplex, Zellwachstumskontrolle, Cryo‑Elektronenmikroskopie