Clear Sky Science · de
Die filamentöse Ultrastruktur des PopZ-Kondensats ist für seine zelluläre Funktion erforderlich
Wie Zellen weiche Tropfen zur Organisation nutzen
Im Inneren jeder lebenden Zelle ist die Chemie dicht gepackt und chaotisch. Dennoch schaffen es Zellen, wichtige Moleküle zur richtigen Zeit am richtigen Ort zu halten. Eine Möglichkeit, dies zu erreichen, ist die Bildung winziger, flüssigkeitsähnlicher Tröpfchen oder Kondensate, die bestimmte Proteine anreichern und andere ausschließen. Diese Studie untersucht eingehend ein solches tropfenbildendes Protein in Bakterien, genannt PopZ, und zeigt, dass sein inneres Gerüst aus feinen Filamenten entscheidend ist, damit lebensnotwendige Prozesse der Zelle korrekt ablaufen.
Ein mikroskopischer Organisator an den Zellpolen
Im Bakterium Caulobacter crescentus sammelt sich PopZ an den beiden Enden bzw. Polen der Zelle und bildet dort konzentrierte Kompartimente. Diese PopZ-reichen „Mikrodomänen“ helfen, den Zellzyklus zu steuern, indem sie spezifische Partnerproteine anziehen und das Chromosom während der Teilung verankern. Fehlt PopZ, teilen sich die Zellen schlecht, verlieren ihre normale Form und gehen mit ihrer DNA fehlerhaft um. Frühere Arbeiten zeigten, dass Zellen auch dann Probleme haben, wenn PopZ-Tröpfchen zu flüssig oder zu steif sind. Unklar war jedoch, wie die detaillierte innere Struktur dieser Tröpfchen – also die Art und Weise, wie PopZ-Moleküle zu größeren Gebilden zusammengebaut sind – ihre Materialeigenschaften und damit das zelluläre Verhalten bestimmt.
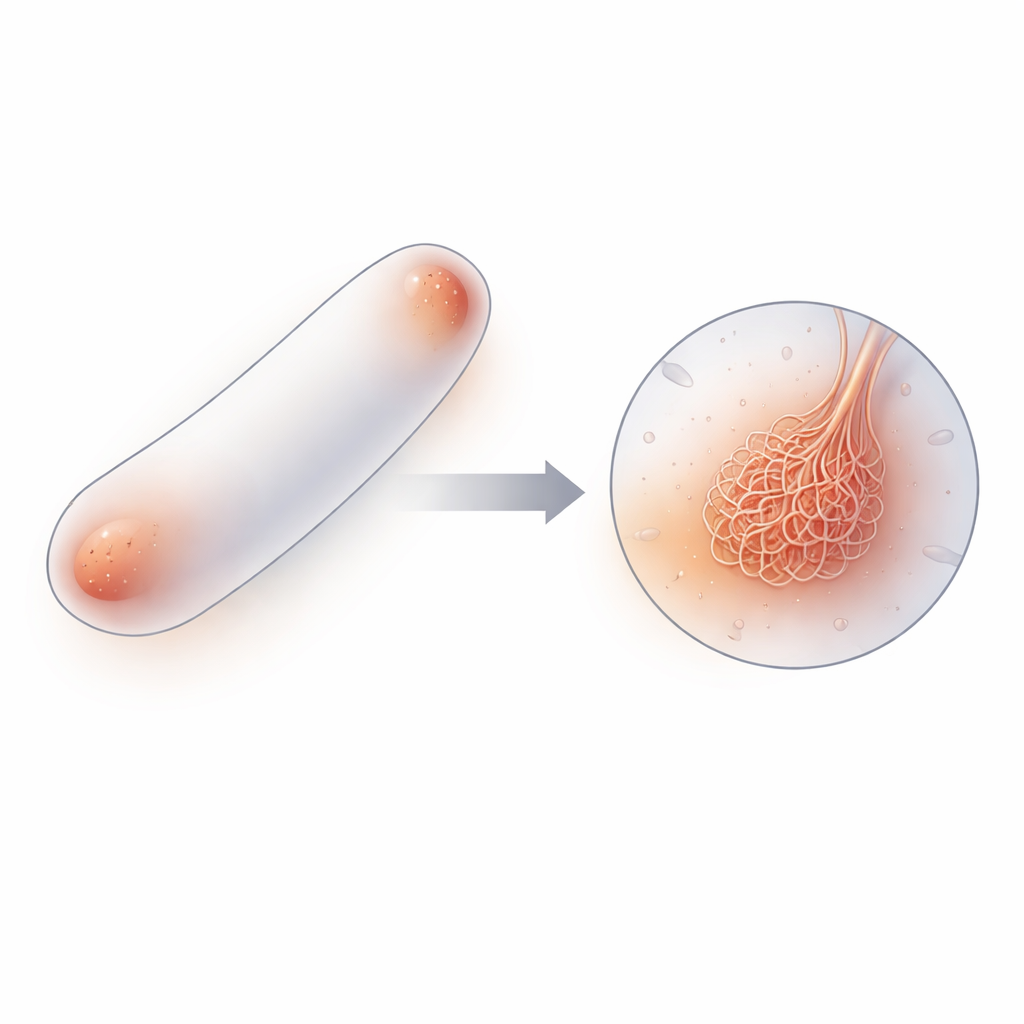
Vom einzelnen Molekül zum Filamentnetz
Mithilfe einer Kombination aus Kryo-Elektronentomographie (einem 3D-Bildgebungsverfahren bei sehr niedrigen Temperaturen), biochemischen Tests, Einzelmolekül-Fluoreszenz und Computersimulationen kartierten die Autoren, wie PopZ-Moleküle über verschiedene Skalen hinweg zusammengebaut werden. Einzelne PopZ-Proteine verbinden sich zunächst zu Dreier-Einheiten (Trimere), die paarweise zu Sechser-Einheiten (Hexamere) zusammenkommen. Diese Hexamere stapeln sich von Ende zu Ende zu kurzen, flexiblen Filamenten von einigen Dutzend Nanometern Länge, und verwobene Netzwerke dieser Filamente bilden das PopZ-Kondensat. Bildgebungen sowohl von gereinigten PopZ-Tröpfchen als auch von PopZ in intakten Zellen zeigten dasselbe filamentöse Geflecht, was belegt, dass diese Architektur kein Artefakt der Reagenzglas-Experimente, sondern ein Kernmerkmal der Funktionsweise von PopZ in lebenden Bakterien ist.
Eingebaute Bremsen und Schalter für die Tropfenbildung
PopZ besteht aus verschiedenen Abschnitten, von denen jeder eine andere Rolle in dieser Assemblierungskaskade spielt. Ein kompakter, helikaler Abschnitt am Schwanzende fungiert als zentrales Oligomerisierungs- und Filamentbildungsmodul und ist allein stark genug, um Filamente und Tröpfchen zu bilden. Dagegen neigt ein flexibler, negativ geladener Mittelbereich dazu, Moleküle auseinanderzuhalten und die Kondensation zu erschweren. Am gegenüberliegenden Ende rekrutiert eine kurze Helix sowohl Klientenproteine als auch – im verdünnten Zustand – klappt sie zurück und kontaktiert den Schwanz, wodurch ein frühzeitiges Zusammenlagern zusätzlich unterdrückt wird. Wenn sich die Bedingungen ändern – etwa durch vorhandene Salze – werden diese abstoßenden Wechselwirkungen abgeschwächt. PopZ ändert dann seine Konformation: die klientenbindende Helix schwenkt vom Schwanz weg, die hemmende Wolke ungeordneter Segmente öffnet sich, Hexamere stapeln sich leichter zu Filamenten und Inter-Filament-Kontakte werden begünstigt. Diese zustandsabhängige Konformationsänderung bedeutet, dass derselbe Proteinbereich, der im verdünnten Zustand die Bindung blockiert, in der dichten Phase zur aktiven Dockingstelle wird.
Was passiert, wenn die Filamente entfernt werden
Um zu untersuchen, wie sich Filamente auf das physikalische Verhalten der Tröpfchen auswirken, erzeugte das Team PopZ-Mutanten, die zwar noch Hexamere bilden konnten, diese aber nicht zu Filamenten stapeln konnten. Diese Varianten bildeten zwar Kondensate, zeigten jedoch auffallend andere Eigenschaften. Anstatt sich zu schönen Kugeln zu formen, die auf der Oberfläche sitzen, flachten die Tröpfchen ab und breiteten sich aus, was auf eine geringere Oberflächenspannung und stärkere Benetzung der Umgebung hindeutet. Innerhalb dieser filamentarmen Kondensate bewegten sich sowohl PopZ selbst als auch seine Klientenproteine deutlich schneller, gemessen mittels Fluoreszenz-Wiederherstellung nach Photobleichen. Anders ausgedrückt: Das Entfernen der Filamente machte die Tröpfchen weicher und durchlässiger. Wurden solche Mutanten in Caulobacter-Zellen eingebracht, störten sie das normale PopZ-Verhalten an den Polen, beeinträchtigten die Chromosomenverankerung und schädigten das Wachstum stark, selbst wenn Wildtyp-PopZ weiterhin vorhanden war. Andere konstruierte Varianten zeigten das entgegengesetzte Missverhältnis: Sie konnten Filamente bilden, kondensierten aber nur schlecht, und auch diese konnten die zelluläre Rolle von PopZ nicht vollständig wiederherstellen.
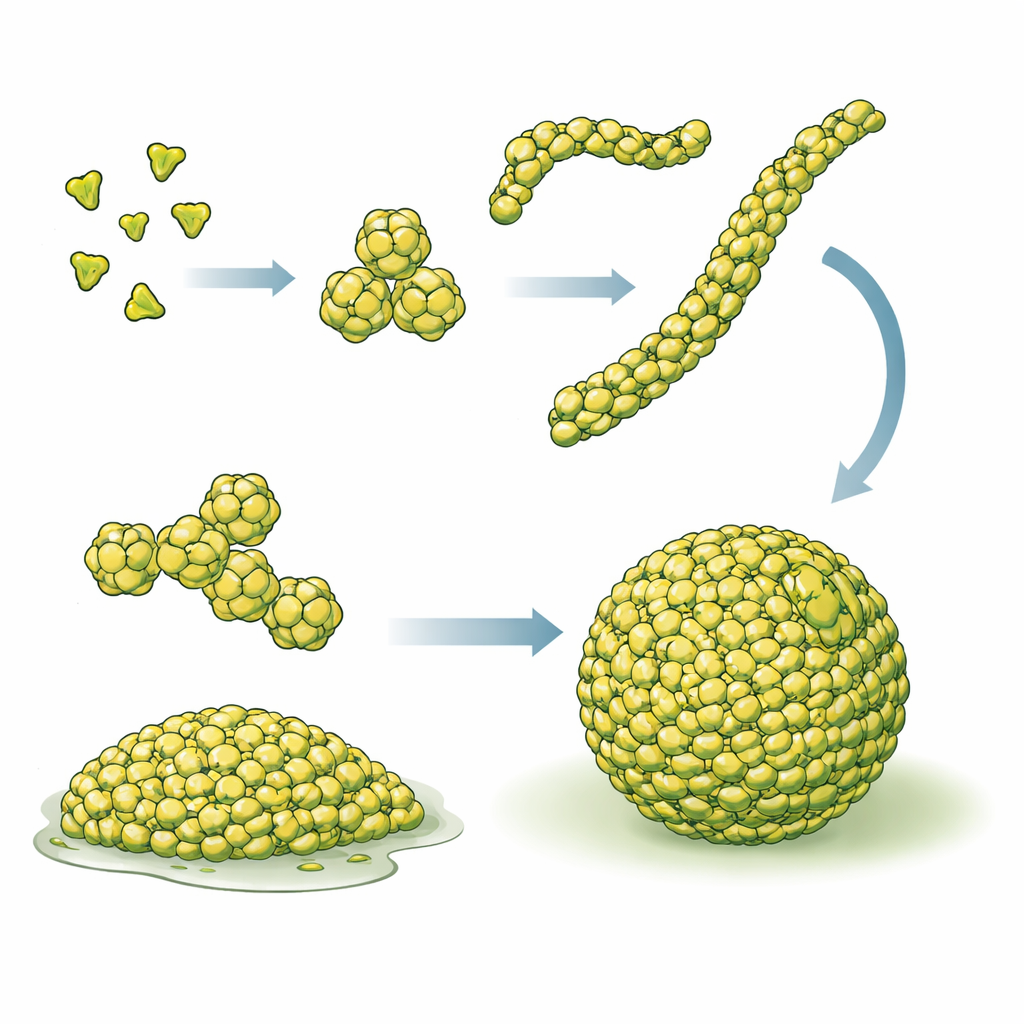
Ein Rezept für funktionale zelluläre Tröpfchen
Die Arbeit führt zu einer klaren Botschaft für Nicht-Spezialisten: Es reicht nicht aus, dass ein Protein wie PopZ einfach nur zusammenklumpt, und es reicht auch nicht, Filamente isoliert zu bilden. Entscheidend für die Zellfunktion ist eine sehr spezifische Ultrastruktur – Kondensate, die selbst aus kurzen, miteinander verbundenen Filamenten bestehen. Dieses filamentöse Gerüst erhöht die Anzahl der Kontaktpunkte zwischen Molekülen, erhöht die Oberflächenspannung des Tropfens, verlangsamt die Bewegung wichtiger Klienten und bietet einen eingebauten molekularen Schalter, der die Klientenbindung nur in der dichten Phase einschaltet. Indem die Studie diese Kausalkette vom Aminosäuresequenz über molekulare Assemblies bis hin zum Verhalten ganzer Zellen nachzeichnet, liefert sie einen allgemeinen Bauplan dafür, wie Zellen das „Gefühl" ihrer weichen inneren Tröpfchen einstellen können, um lebenswichtige Prozesse zu kontrollieren.
Zitation: Scholl, D., Boyd, T., Latham, A.P. et al. The filamentous ultrastructure of the PopZ condensate is required for its cellular function. Nat Struct Mol Biol 33, 420–432 (2026). https://doi.org/10.1038/s41594-025-01742-y
Schlüsselwörter: biomolekulare Kondensate, Proteinfilamente, zellulare Polarität, Phasentrennung, bakterieller Zellzyklus