Clear Sky Science · de
Mechanismus und Rekonstitution zirkadianer Transkription in Cyanobakterien
Warum innere Uhren wichtig sind, sogar für Bakterien
Alle Lebewesen, vom Menschen bis zu winzigen Mikroben, halten Zeit. Diese inneren Uhren helfen Organismen, Sonnenaufgang und Sonnenuntergang vorherzusehen und Aktivitäten wie Nahrungsaufnahme, Reparatur und Wachstum zeitlich zu planen. In diesem Artikel wird untersucht, wie ein einfacher photosynthetischer Bakterium, Synechococcus elongatus, eine proteinbasierte Uhr nutzt, um Gene mit bemerkenswerter Präzision über einen 24‑Stunden‑Zyklus an- und auszuschalten. Indem die Forschenden dieses Zeitgebers im Reagenzglas wiederaufbauten, zeigen sie eine reduzierte Version einer biologischen Uhr, die als Inspiration für neue Werkzeuge in Biotechnologie und synthetischer Biologie dienen könnte.
Eine winzige Uhr, die auf Chemie läuft
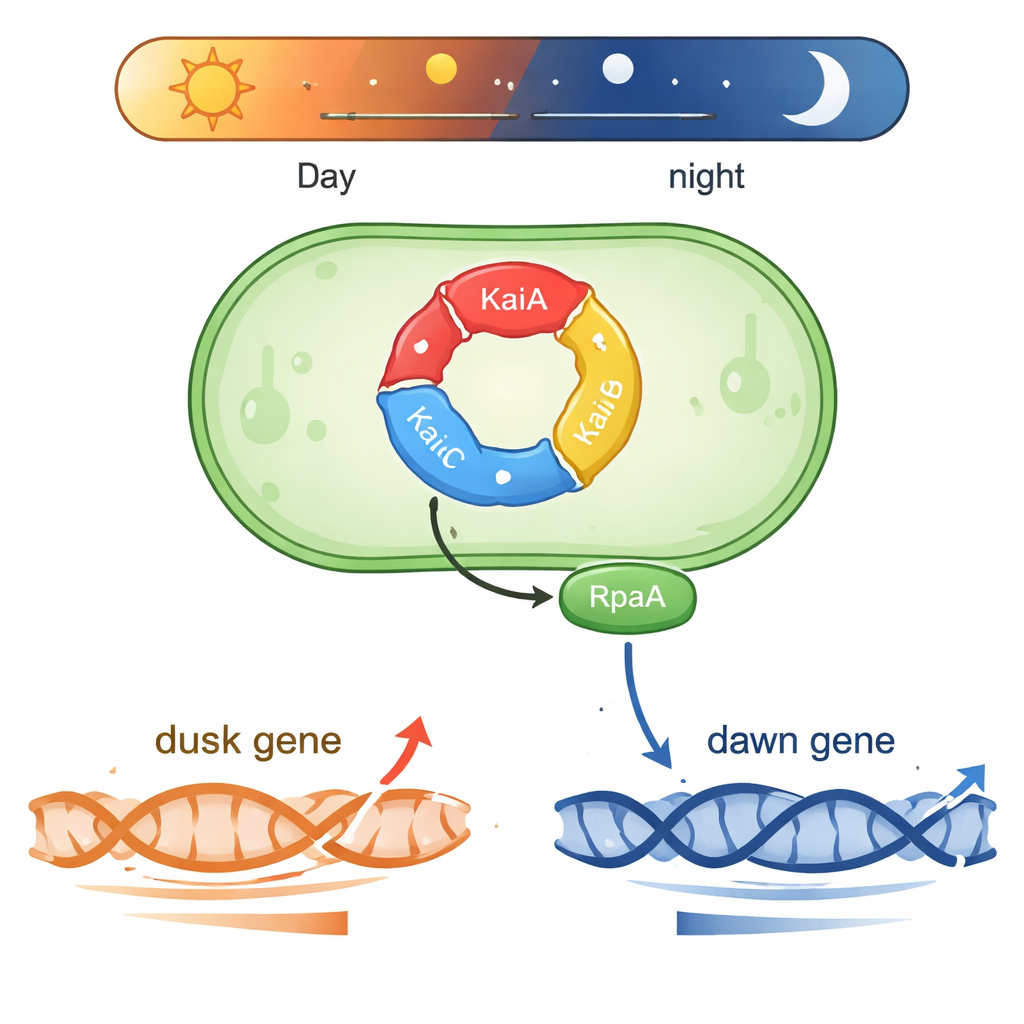
Synechococcus lebt in sonnenbeschienenen Gewässern und muss tägliche Lichtwechsel vorhersagen. Im Kern steht eine dreiteilige Proteinmaschine aus KaiA, KaiB und KaiC. Diese Proteine übertragen Phosphatgruppen in einem sich wiederholenden Zyklus von etwa 24 Stunden und bilden ein biochemisches »Zahnradgetriebe«, das die Zeit auch außerhalb der Zelle aufrechterhält. Zwei weitere Proteine, SasA und CikA, lesen den Phosphorylierungszustand von KaiC und nutzen diese Information, um ein anderes Protein, RpaA, zu steuern. Wenn RpaA phosphoryliert ist, bindet es an DNA und fungiert als Hauptschalter für Hunderte von Genen, die entweder um das subjektive »Morgengrauen« oder »Abenddämmerung« in konstantem Licht ansteigen und fallen.
Ein Protein, zwei entgegengesetzte Gen‑Zeitpläne
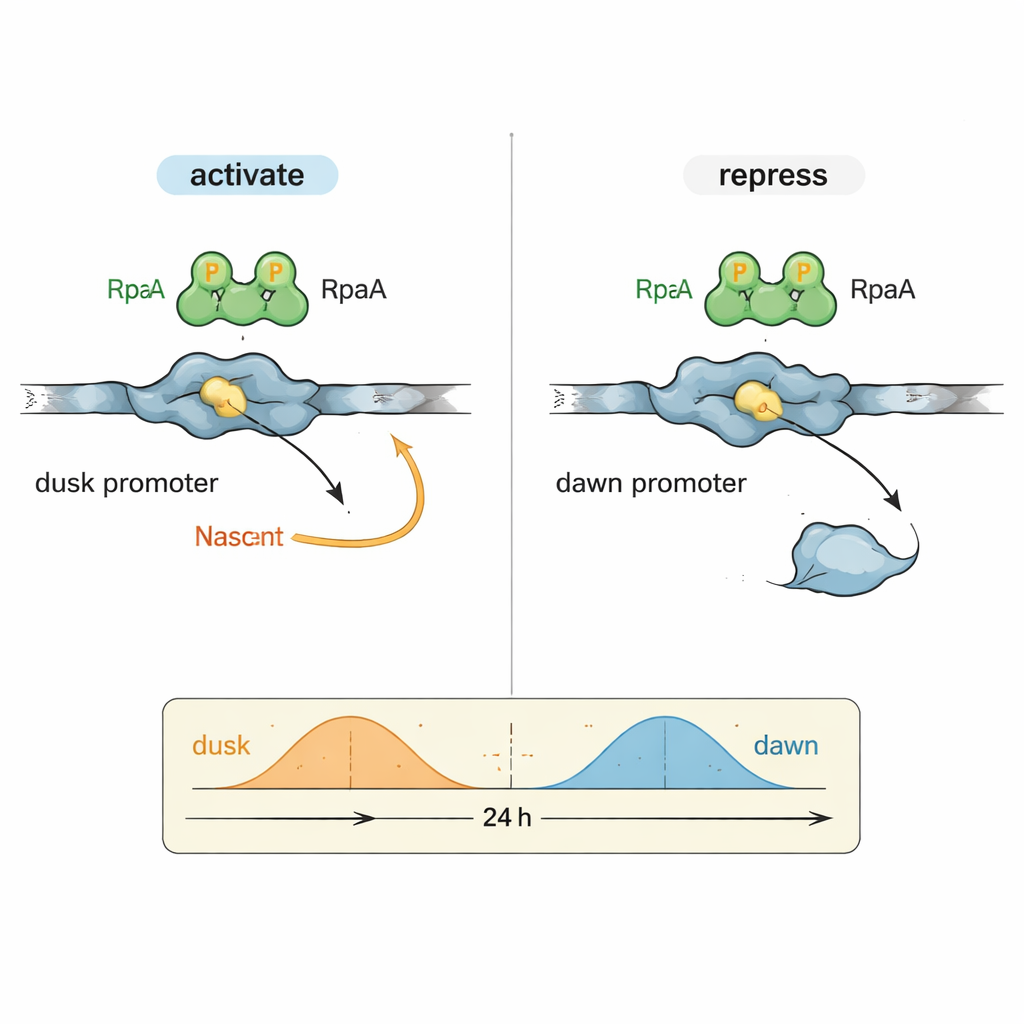
Ein Rätsel der zirkadianen Biologie bestand darin, wie ein Ausgangsfaktor wie RpaA Gene koordinieren kann, die zu sehr unterschiedlichen Tageszeiten ihren Gipfel erreichen. Die Autorinnen und Autoren konzentrierten sich auf zwei repräsentative Kontrollregionen (Promotoren): kaiBC, das zur Dämmerung am aktivsten ist, und purF, das seinen Gipfel bei Morgendämmerung erreicht. In kontrollierten Reaktionen mit gereinigter cyanobakterieller RNA‑Polymerase und RpaA zeigten sie, dass phosphoryliertes RpaA die Transkription vom kaiBC‑Promotor verstärkt und gleichzeitig die Transkription vom purF‑Promotor vermindert. Detaillierte Footprinting‑Experimente kartierten genau, wo RpaA auf jedem DNA‑Abschnitt bindet, und zeigten, dass seine Position relativ zu den standardmäßigen Promotorelementen bestimmt, ob es als Beschleuniger oder Bremse wirkt.
Den Schalter der Uhr in atomaren Details sehen
Um dieses doppelte Verhalten auf molekularer Ebene zu verstehen, nutzte das Team hochauflösende Kryo‑Elektronenmikroskopie, um die Struktur von RpaA gebunden an den kaiBC‑Promotor zusammen mit der RNA‑Polymerase einzufangen. Die Bilder zeigen RpaA, das die DNA als asymmetrisches Paar umklammert und zwei Schlüsselbereiche des Enzyms kontaktiert: das Schwanzende der Alpha‑Untereinheit und eine Region des Sigma‑Faktors, die normalerweise Promotorsequenzen erkennt. Diese Kontakte biegen die DNA und helfen, die RNA‑Polymerase an einer leicht neu definierten Startstelle für die Transkription zu positionieren. Sorgfältig gewählte Mutationen, die einen dieser Kontaktpunkte schwächen, verringern oder verhindern die Aktivierung von kaiBC sowohl in vitro als auch in lebenden Zellen, was bestätigt, dass die physikalische Anwerbung der RNA‑Polymerase der Mechanismus der Dämmerungsphasaktivierung ist.
Ein uhrgetriebenes Gen von Grund auf neu bauen
Da die native cyanobakterielle RNA‑Polymerase komplex ist und schwer über Tage hinweg aktiv zu halten ist, wandten sich die Forschenden als Nächstes der viel einfacheren T7‑Bakteriophage‑Polymerase zu, die in Laboren weit verbreitet ist. RpaA kann dieses fremde Enzym nicht anwerben, aber es kann es dennoch blockieren, indem es auf der DNA sitzt. Das Team entwarf eine synthetische DNA‑Vorlage, bei der ein T7‑Promotor einen fluoreszenten RNA‑»Broccoli«‑Reporter antreibt, mit einer RpaA‑Bindungsstelle stromabwärts. Wenn sie diese Vorlage mit dem KaiA–KaiB–KaiC‑Uhrwerk, der CikA‑Kinasen/Phosphatase, RpaA und der T7‑Polymerase in einem einzigen optimierten Puffer kombinierten, beobachteten sie sich hebende und fallende Transkriptionsraten mit einer Periode von etwa 24 Stunden. Der Rhythmus ließ sich durch Änderung des ATP‑zu‑ADP‑Verhältnisses zurücksetzen und blieb über einen Temperaturbereich nahezu konstant — klassische Kennzeichen einer echten zirkadianen Uhr.
Von einfachen Uhren zu ingenieurmäßiger Zeitsteuerung
Die Studie zeigt, dass nur sechs Proteine ausreichen, um einen chemischen Taktgeber mit einem rhythmischen Gen‑Output zu verbinden: die drei Kai‑Uhrproteine, CikA, RpaA und eine RNA‑Polymerase. Indem man verändert, wo RpaA auf der DNA sitzt, kann dasselbe Molekül einige Gene zur Dämmerung und andere zum Morgengrauen zum Gipfel bringen, was hilft, die komplexen Wellen der Genaktivität in Cyanobakterien zu erklären. Da das repressionbasierte Design sogar mit einer fremden Polymerase wie T7 funktioniert, sollte es möglich sein, dieses minimale Uhrmodul in andere Mikroben oder zellfreie Systeme zu transplantieren und Forschenden zu erlauben, Gene so zu programmieren, dass sie sich mit täglichem Rhythmus an‑ und ausschalten — für Forschung, industrielle Produktion oder zukünftige therapeutische Anwendungen.
Zitation: Fang, M., Gu, Y., Leanca, M. et al. Mechanism and reconstitution of circadian transcription in cyanobacteria. Nat Struct Mol Biol 33, 275–281 (2026). https://doi.org/10.1038/s41594-025-01740-0
Schlüsselwörter: zirkadiane Uhr, Cyanobakterien, Transkriptionsregulation, RpaA, Synthetische Biologie