Clear Sky Science · de
Cereblon induziert den Abbau des Neosubstrats G3BP2 durch Nachahmung molekularer Oberflächen
Die zelluläre Reinigung als intelligentes Zielsystem
Moderne Medikamente versuchen zunehmend, Krankheiten nicht nur durch Blockade problematischer Proteine zu behandeln, sondern diese Proteine ganz gezielt zu entfernen. Diese Arbeit untersucht eine raffinierte Methode, eine der zellulären "Reinigungs"-Maschinen so umzuprogrammieren, dass sie in Verbindung mit einem kleinen Molekül ein mit Krebs und anderen Erkrankungen assoziiertes Protein erkennt und abbaut. Die Studie zeigt einen unerwarteten Trick: die Reinigungsmaschine formt einen Teil ihrer Oberfläche um, um einen natürlichen Partner des Zielproteins nachzuahmen, wodurch sie andocken und das Protein zur zellulären Entsorgung schicken kann.
Der Müllsammler der Zelle mit verborgener Flexibilität
Unsere Zellen markieren fortwährend abgenutzte oder unerwünschte Proteine für den Abbau, mithilfe eines Systems, das um E3-Ligasen herum organisiert ist — große Proteinkomplexe, die entscheiden, was entfernt werden soll. Einer dieser Komplexe nutzt eine Komponente namens Cereblon, die wie ein Sensor wirkt und bestimmte Merkmale ("Degrons") auf anderen Proteinen erkennt. Bestimmte zugelassene Arzneistoffe nutzen Cereblon bereits als "molecular glue": Sie binden an Cereblon und schaffen eine neue Andockoberfläche, die krankheitsrelevante Proteine heranzieht, welche dann markiert und abgebaut werden. Bisher folgten die meisten bekannten Ziele einem bestimmten Strukturmuster, sodass die Bandbreite der auf diese Weise entfernbaren Proteine als eingeschränkt galt.
Ein neues Ziel außerhalb der alten Regeln entdecken
In der neuen Studie untersuchten die Autoren eine Sammlung von auf Cereblon ausgerichteten molecular glues in menschlichen Zellen und identifizierten eine Verbindung namens MRT-5702. Dieses kleine Molekül bewirkte einen raschen Verlust des Proteins G3BP2, das an der RNA-Regulation beteiligt ist und Teil von Stressgranula bildet — Assemblies, die mit Krebs, Herzproblemen und neurodegenerativen Erkrankungen in Verbindung stehen. Wichtig ist, dass G3BP2 das übliche Degron-Muster, das Cereblon erkennt, nicht besitzt. Nachfolgende Zellversuche, einschließlich empfindlicher, lichtbasierter Messungen der Protein-Nähe, bestätigten, dass MRT-5702 Cereblon und G3BP2 zu einem dreiteiligen Komplex zusammenführt, der zum Abbau von G3BP2 führt, während das eng verwandte Protein G3BP1 verschont bleibt, sofern nicht seine Schlüsseldomäne ausgetauscht wird.
Nachahmung als Bindungsstrategie
Bei tiefergehender Analyse fragten die Forschenden, wie G3BP2 an Cereblon binden kann, ohne das standardmäßige Erkennungsmotiv. Anstatt nach Ähnlichkeiten zwischen G3BP2 und bekannten Cereblon-Zielen zu suchen, kehrten sie die Frage um: Könnte Cereblon einem der üblichen Bindungspartner von G3BP2 ähneln? G3BP-Proteine interagieren häufig über einen Hotspot in einer Region namens NTF2-ähnliche Domäne mit anderen Molekülen, die normalerweise kurze Sequenzmotive erkennt. Mithilfe struktureller Modelle des natürlichen Partners USP10 von G3BP2 scannten die Forschenden rechnerisch die Oberfläche von Cereblon und fanden eine Stelle in einer weniger verstandenen Region, der LON-Domäne, die Form und Chemie des USP10-Bindungsmotivs eng nachahmt. Das Mutieren nur weniger entscheidender Aminosäuren an dieser Stelle oder im Hotspot von G3BP2 schwächte den dreiteiligen Komplex, was darauf hindeutet, dass Cereblon effektiv USP10 imitiert, um an G3BP2 anzudocken.
Die neue Schnittstelle in atomarem Detail einfangen
Um diese ungewöhnliche Wechselwirkung zu visualisieren, nutzte das Team hochauflösende Kryo-Elektronenmikroskopie, um die Struktur eines Komplexes aus Cereblon, einer anderen Kernkomponente der Ligase, MRT-5702 und der NTF2-ähnlichen Domäne von G3BP2 zu lösen. Die Aufnahmen zeigten, dass sich eine flexible Schleife in der LON-Domäne von Cereblon biegt und umformt und nahezu die Hälfte der Kontaktfläche zu G3BP2 bildet. Die aktive spiegelbildliche Form von MRT-5702 sitzt in Cereblons üblichen Wirkstoffbindungsfach, trägt aber zusammen mit der Schleife dazu bei, eine breite Andockfläche zu schaffen, die eine Hälfte des G3BP2-Dimers umschließt. Bemerkenswerterweise nutzt diese Anordnung kaum die kanonische Cereblon-Stelle, die frühere Glue-Ziele handhabte, und zeigt damit, dass Cereblon je nach eingesetztem Glue und beteiligtem Protein sehr unterschiedliche Bereiche seiner Oberfläche einbinden kann. Gleichzeitig bleibt die ungenutzte Hälfte des G3BP2-Dimers frei, um andere Partner zu binden, was einen plausiblen Mechanismus für eine "kollaterale" Degradation angrenzender, zufällig gebundener Proteine bietet.
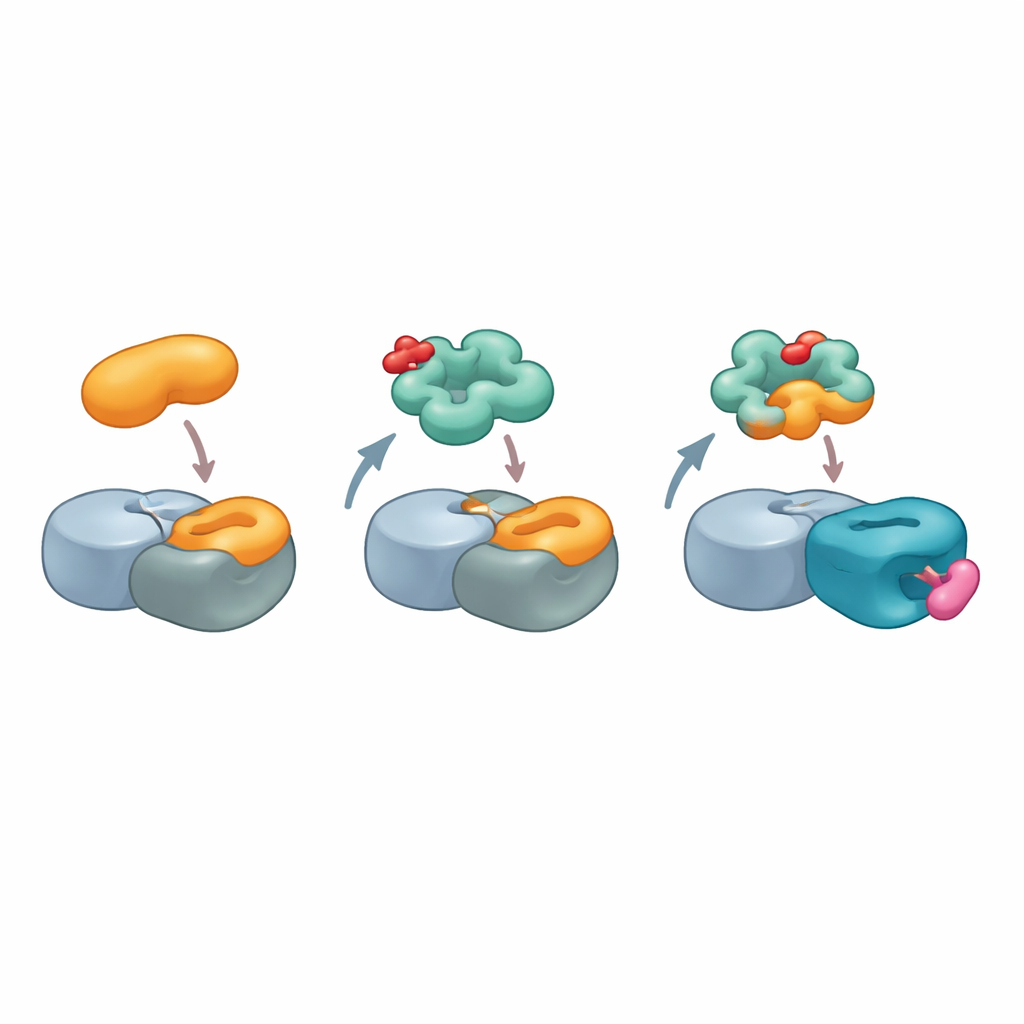
Glueprints für zukünftiges Wirkstoffdesign
In der Summe zeichnen die Ergebnisse ein Bild von Cereblon als weitaus vielseitigerem Vermittler als bislang angenommen. Anstatt darauf zu bestehen, dass Ziele einen einzigen Degron-Typ tragen, kann Cereblon, mit dem richtigen molecular glue bewaffnet, eine zusammengesetzte Oberfläche formen, die natürliche Protein–Protein-Kontakte an anderen Stellen in der Zelle nachahmt. Die Autoren schlagen vor, dass solche kombinierten Protein-und-Glue-Oberflächen, die sie "Glueprints" nennen, kartiert und entworfen werden könnten, um vorhandene Interaktionshotspots vieler krankheitsrelevanter Proteine zu imitieren. Für den Laien lautet die Kernaussage: Wirkstoffentwickler müssen nicht unbedingt völlig neue Bindungstaschen an problematischen Proteinen finden; stattdessen können sie die zelleigene Recyclingmaschine so trainieren, dass sie diese Proteine erkennt, indem sie geschickt die Formen ihrer üblichen Partner kopiert, wodurch sich die Auswahl an sicher und selektiv entfernbaren Zielen deutlich erweitert.
Zitation: Annunziato, S., Quan, C., Donckele, E.J. et al. Cereblon induces G3BP2 neosubstrate degradation using molecular surface mimicry. Nat Struct Mol Biol 33, 479–487 (2026). https://doi.org/10.1038/s41594-025-01738-8
Schlüsselwörter: molecular glue degraders, cereblon, targeted protein degradation, G3BP2, protein–protein interactions