Clear Sky Science · de
Ein verallgemeinerbares Foundation-Modell zur Analyse von menschlichen Gehirn-MRTs
Computern beibringen, Gehirnscans zu lesen
Die Magnetresonanztomographie (MRT) ermöglicht es Ärztinnen und Ärzten, das lebende Gehirn ohne Operation zu betrachten, doch das Interpretieren dieser Bilder beruht noch immer stark auf menschlichen Expertinnen und Experten und großen beschrifteten Datensätzen. Diese Studie stellt BrainIAC vor, eine Art "Allzweck-Gehirnmaschine", die aus Zehntausenden unbezeichneter Gehirnscans lernt und sich dann schnell an viele medizinische Fragestellungen anpassen lässt – von der Schätzung des Gehirnalters bis zur Abgrenzung von Tumoren – häufig schon mit nur wenigen Beispielen. Für Patientinnen und Patienten könnte eine solche Technologie letztlich schnellere Diagnosen, bessere Behandlungsplanung und Zugang zu fortgeschrittenen Bildgebungswerkzeugen auch in Krankenhäusern mit begrenzter Spezialexpertise bedeuten.
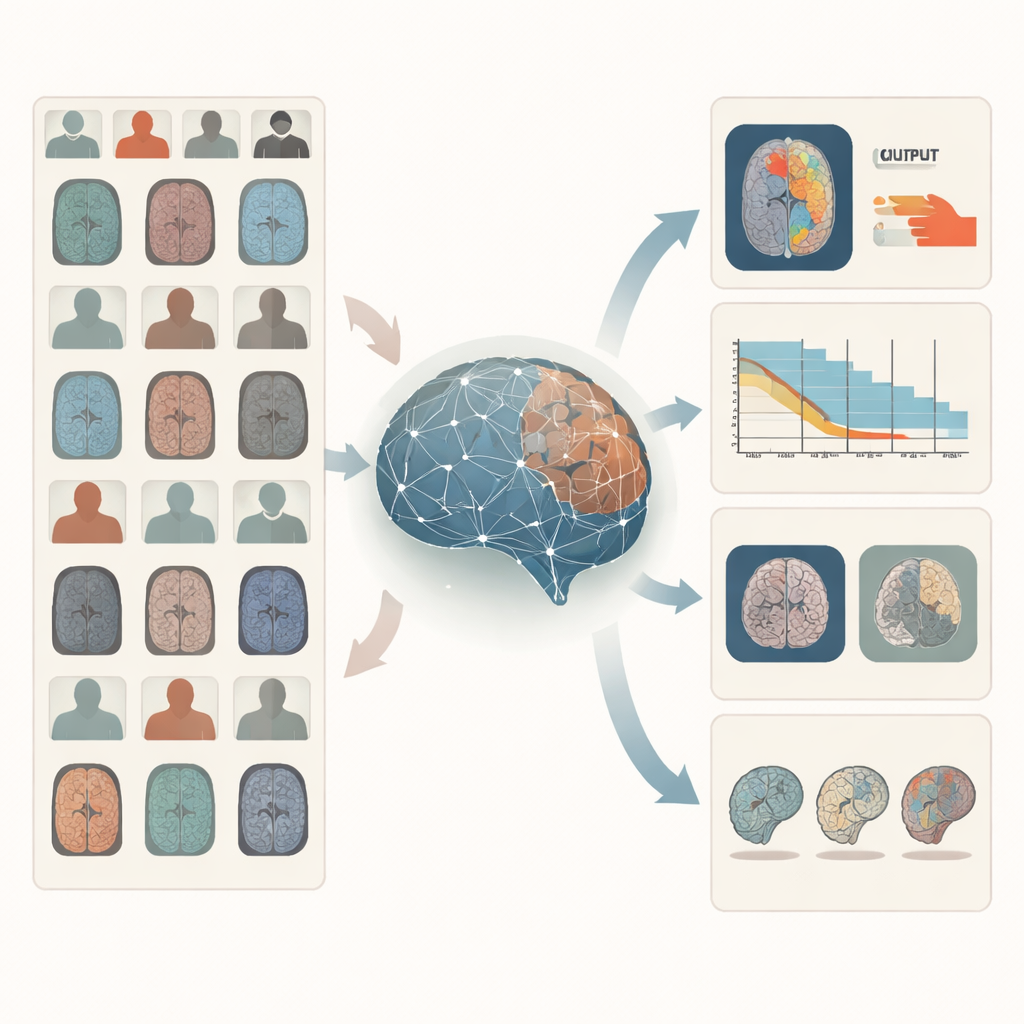
Warum Gehirnscans für Computer schwierig sind
Gehirn-MRTs sind reich an Informationen, aber unübersichtlich. Eine einzelne Person kann mit mehreren Einstellungen gescannt werden, die jeweils unterschiedliche Gewebe oder Krankheitsmerkmale hervorheben. Krankenhäuser verwenden verschiedene Scanner und Protokolle, sodass Bilder von Ort zu Ort stark variieren können. Hinzu kommt, dass detaillierte Expertenannotationen – etwa das exakte Nachzeichnen von Tumorgrenzen oder die Verfolgung der Langzeitüberlebenszeit – teuer und selten sind. Traditionelle KI-Systeme werden in der Regel für eine enge Aufgabe auf einem kuratierten Datensatz trainiert. Sie haben oft Schwierigkeiten, wenn sie auf neue Krankenhäuser, seltene Erkrankungen oder Fragestellungen stoßen, für die sie nicht speziell entwickelt wurden.
Ein einzelnes Kernmodell für viele Hirnaufgaben
BrainIAC geht einen anderen Weg: Statt eine Aufgabe nach der anderen zu lernen, erwirbt es zunächst die allgemeine "Sprache" von Gehirnstruktur und Krankheit aus 32.015 MRT-Scans, die aus 34 Datensätzen und zehn neurologischen Erkrankungen stammen, und auf die sich im gesamten Pool nahezu 49.000 Scans summieren. Das Modell wird selbstüberwacht trainiert, das heißt, es benötigt keine menschlichen Labels. Es betrachtet viele kleine dreidimensionale Patches, die aus Ganzhirnscans ausgeschnitten wurden, und lernt zu erkennen, ob zwei unterschiedlich augmentierte Versionen vom selben Ort stammen oder von verschiedenen Gehirnen. Indem es passende Patches in seinem internen Raum näher zusammenrückt und nicht zusammenhängende auseinanderdrängt, baut BrainIAC eine flexible Repräsentation davon auf, wie gesunde und erkrankte Gehirne über Alter, Scanner und Krankenhäuser hinweg typischerweise aussehen.
Den Gehirnmotor in Aktion setzen
Sobald diese Kernrepräsentation erlernt ist, testen die Forschenden BrainIAC an sieben konkreten Aufgaben, die reale klinische Probleme widerspiegeln. Dazu gehören das Sortieren von Scans nach MRT-Sequenztyp, die Schätzung, wie alt ein Gehirn erscheint, die Vorhersage, ob ein Hirntumor eine wichtige genetische Mutation trägt, die Prognose des Überlebens bei Patientinnen und Patienten mit aggressiven Tumoren, die Unterscheidung früher Gedächtnisprobleme von normaler Alterung, die Schätzung, wie lange ein Schlaganfall zurückliegt, und das Segmentieren von Tumoren auf Bildern. Für jede Aufgabe vergleichen sie drei Strategien: ein Modell von Grund auf für diese eine Aufgabe zu trainieren, von früheren medizinischen Bildgebungsmodellen auszugehen, die für andere Zwecke entwickelt wurden, oder BrainIACs bereits gelernte Gehirnfeatures feinzuverfeinern. In allen Fällen erreicht oder übertrifft BrainIAC die Alternativen, insbesondere wenn nur begrenzte beschriftete Daten zur Verfügung stehen.
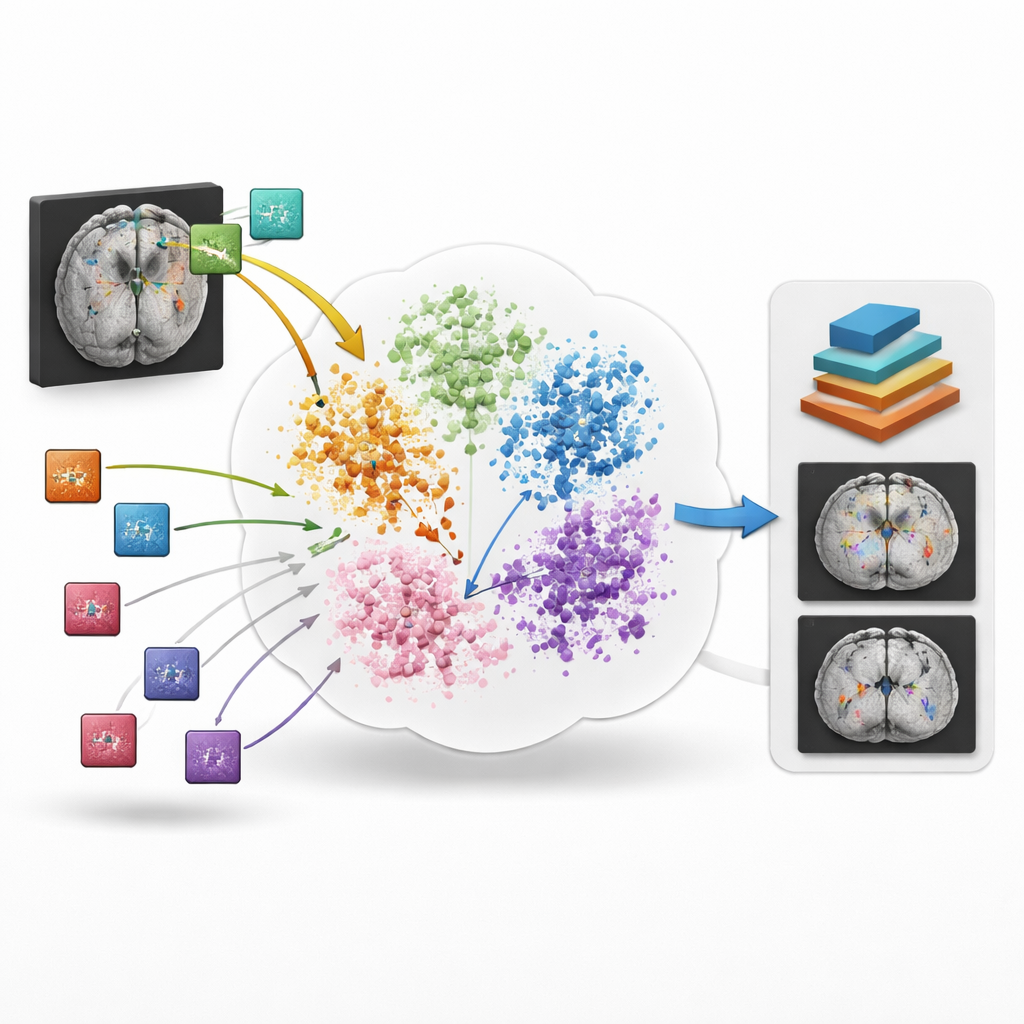
Gut funktionierend, wenn Daten knapp sind
Ein zentraler Prüfpunkt ist, wie sich das System verhält, wenn beschriftete Daten sehr knapp sind, wie es bei seltenen Erkrankungen oder teuren Bildgebungsstudien häufig vorkommt. Das Team untersucht Szenarien, in denen nur 10 % der üblichen Trainingsscans verwendet werden, und noch schwierigere "Few-Shot"-Einstellungen, in denen nur ein oder fünf beschriftete Beispiele pro Klasse vorliegen. Unter diesen strengen Bedingungen liefert BrainIAC konsistent genauere Vorhersagen als Modelle, die von Grund auf neu trainiert wurden, oder andere verfügbare Foundation-Modelle. Beispielsweise unterscheidet es subtile MRT-Sequenztypen besser, sagt Tumor-Genetik und Überleben genauer voraus und erstellt sauberere Tumorsegmentierungen mit deutlich weniger annotierten Bildern. Das Modell erweist sich zudem als stabiler, wenn gängige MRT-Artefakte wie Kontrastverschiebungen oder scannerbedingte Verzerrungen künstlich hinzugefügt werden, was darauf hindeutet, dass es robuste Merkmale gelernt hat und nicht fragile Abkürzungen.
Was das für Patientinnen, Patienten und Kliniker bedeuten könnte
Um zu prüfen, ob BrainIAC sich auf klinisch sinnvolle Regionen konzentriert, erzeugen die Autorinnen und Autoren visuelle "Aufmerksamkeitskarten", die zeigen, wo das Modell hinschaut, wenn es Entscheidungen trifft. Diese Karten heben Strukturen wie den Hippocampus bei frühen Gedächtnisproblemen, weiße Substanzbereiche zur Altersschätzung und den Tumorkern für genetische und Überlebensvorhersagen hervor – Bereiche, die mit der Intuition menschlicher Expertinnen und Experten übereinstimmen. Da BrainIAC in verschiedene Analyse-Pipelines integriert und mit minimalem zusätzlichem Training angepasst werden kann, bietet es eine flexible Grundlage für künftige Bildgebungswerkzeuge, einschließlich möglicher Kombinationen mit klinischen Aufzeichnungen oder genetischen Daten.
Ein Schritt zu intelligenterer, besser zugänglicher Gehirnbildgebung
Insgesamt zeigt die Studie, dass ein einzelnes, sorgfältig trainiertes Foundation-Modell als starker Ausgangspunkt für viele verschiedene Gehirn-MRT-Aufgaben dienen kann und häufig spezialisierte Systeme übertrifft, die jedes Mal neu aufgebaut werden müssen. Für Nicht-Spezialisten lautet die Kernaussage, dass BrainIAC wie ein breit gebildeter "Gehirnleser" agiert, der mit nur wenigen Beispielen schnell neue Fähigkeiten erlernen kann. Obwohl es maßgeschneiderte Modelle oder medizinisches Urteil nicht ersetzt, legt es eine wichtige Grundlage dafür, bildbasierte Vorhersagen genauer, robuster und breiter verfügbar zu machen – auch in Situationen, in denen das Sammeln großer beschrifteter Datensätze sonst unmöglich wäre.
Zitation: Tak, D., Garomsa, B.A., Zapaishchykova, A. et al. A generalizable foundation model for analysis of human brain MRI. Nat Neurosci 29, 945–956 (2026). https://doi.org/10.1038/s41593-026-02202-6
Schlüsselwörter: Gehirn-MRT, medizinische KI, Foundation-Modelle, selbstüberwachtes Lernen, Neuroimaging