Clear Sky Science · de
TGFβ-Signalgebung vermittelt Mikroglia-Resilienz gegen räumlich und zeitlich begrenzte Myelindegeneration
Warum die Verdrahtung des Gehirns Pfleger braucht
Mit dem Alter verschleißt die „Isolierung“ um unsere Nervenfasern — das Myelin — auf natürliche Weise. Diese Isolierung ist entscheidend für schnelle und zuverlässige Kommunikation zwischen Gehirn und Körper. Die neue Studie untersucht, warum eine bestimmte Fasertrasse im Rückenmark, der Hinterstrang, besonders anfällig für diesen Verschleiß ist und wie eine eingebaute Bremse des Immunsystems, ein Signalweg namens TGFβ, verhindert, dass sich der Schaden unkontrolliert ausbreitet. Das Verständnis dieser verborgenen Schutzfunktion ist wichtig, weil ihr Versagen bestimmte Rückenmarkserkrankungen erklären könnte und Auswirkungen darauf haben kann, wie man Erkrankungen des Gehirns und Krebserkrankungen bei älteren Menschen behandelt.
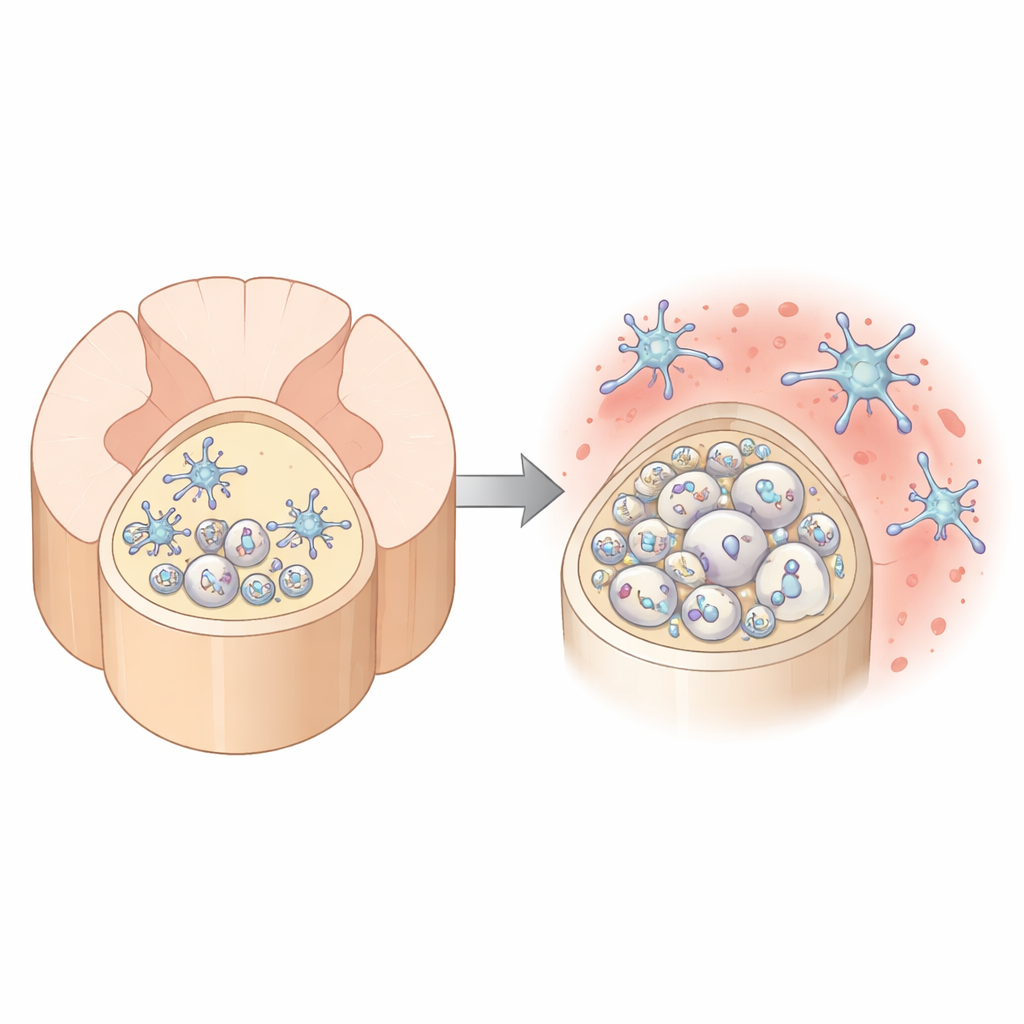
Wo das Altern die Rückenmarks‑„Autobahn“ am stärksten trifft
Die Autoren verglichen zunächst zwei große weiße Substanzbahnen im Mausrückenmark: den dorsalen (hinteren) und den ventralen (vorderen) Strang. Mithilfe hochauflösender Elektronenmikroskopie stellten sie fest, dass das Myelin im dorsalen Strang mit dem Alter zunehmend deformiert. Die normalerweise engen Umwicklungen der Nervenfasern lockern sich, wölben sich nach außen oder lösen sich ab, wodurch vergrößerte Zwischenräume zwischen Nerven und Isolierung entstehen und die Myelinzerstörung zunimmt. Im Gegensatz dazu bleibt der ventrale Strang vergleichsweise stabil. Die dorsale Region enthält außerdem deutlich mehr, aber dünnere Axone, was sie zu einer besonders anspruchsvollen Umgebung für die Zellen macht, die Myelin bilden und erhalten.
Immunwächter unter wachsendem Druck
Diese Fasern werden von Mikroglia umgeben, den ansässigen Immunzellen von Gehirn und Rückenmark. Sie patrouillieren ständig das Gewebe, räumen Trümmer weg und justieren Verbindungen. Wenn das Myelin im dorsalen Strang mit dem Alter degeneriert, verändern sich Aussehen und Verhalten dieser Mikroglia: Sie fahren Gene hoch, die mit Immunaktivierung zusammenhängen, sammeln ölige Tropfen im Inneren an und zeigen Anzeichen dafür, dass sie mehr beschädigtes Myelin aufgenommen haben. Gleichzeitig wird die Gewebeumgebung im dorsalen Strang stark mit TGFβ1 angereichert — einem Signalmolekül, das Mikroglia in einem zurückhaltenden, homöostatischen Zustand hält. Die Mikroglia selbst sind die Hauptquelle dieses TGFβ1, was darauf hindeutet, dass sie versuchen, sich selbst zu bremsen, während die Stresssignale zunehmen.
Was passiert, wenn die Sicherheitsbremse versagt
Um die Bedeutung dieser Bremse zu untersuchen, schalteten die Forschenden die TGFβ-Signalgebung gezielt in Mikroglia erwachsener Mäuse aus, entweder indem sie den Rezeptor entfernten, mit dem diese Zellen TGFβ wahrnehmen, oder indem sie verhinderten, dass sie TGFβ1 produzieren. In beiden Fällen war das Ergebnis auffallend ähnlich und stark lokalisiert: Mikroglia im dorsalen Strang wurden überzählig, hochaktiviert und nahmen ein schaumiges Erscheinungsbild mit aufgespeichertem Myelin an. Das Myelin in dieser Region wurde abgeschält, Axone zeigten Degenerationszeichen, und die Mäuse entwickelten zunehmend Bewegungs‑ und Koordinationsstörungen, besonders im Alter. Andere Rückenmarksregionen waren weit weniger betroffen, was eine regionsspezifische Abhängigkeit von diesem Signalweg aufzeigt.
Ein spezieller Mikroglia‑Subtyp und gestresste Myelinbildner
Single‑Nucleus-RNA‑Sequenzierung ermöglichte es dem Team, einzelne Zelltypen zu katalogisieren, während die Krankheit voranschritt. Sie entdeckten eine eigenständige Untergruppe von Mikroglia — bezeichnet als TGFβ‑sensitive Mikroglia — die bei Wegfall der TGFβ‑Signalgebung dramatisch zunahm. Diese Zellen exprimierten hohe Mengen an Genen, die mit starken Entzündungsreaktionen, intensivem Myelinabbau und Lipidverarbeitung verknüpft sind, und sie konzentrierten sich im dorsalen Strang. Gleichzeitig verschob sich die Population der reifen Myelin bildenden Zellen, der Oligodendrozyten. Gesunde Subtypen nahmen ab, während eine „krankheitsassoziierte“ Oligodendrozyten‑Gruppe im geschädigten dorsalen Strang zunahm, jedoch keine funktionelle Myelinschicht wieder aufbaute, sodass Axone trotz eines scheinbaren Reparaturversuchs freigelegt blieben.
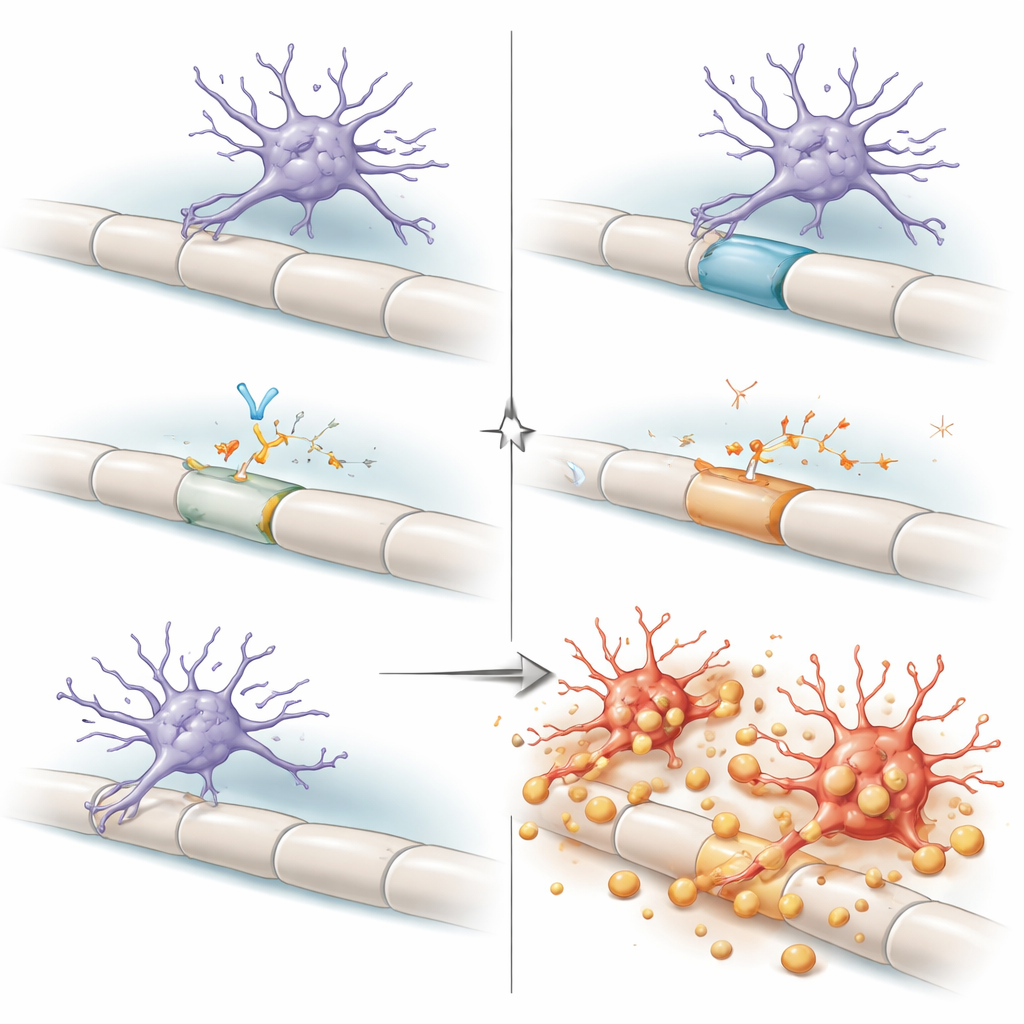
Folgen für das Altern und künftige Therapien
Zusammen betrachtet zeichnen die Befunde den dorsalen Strang als ein hoch belastetes Viertel, in dem alterndes Myelin und überarbeitete Stützzellen die Mikroglia an einen Kipppunkt treiben. Unter normalen Bedingungen hält eine autokrine Schleife — Mikroglia produzieren und wahrnehmen ihr eigenes TGFβ1 — sie in einem „vorbereiteten, aber resilienten“ Zustand, so dass sie mit andauernden Trümmern umgehen können, ohne relativ intaktes Myelin anzugreifen. Wird diese Schleife unterbrochen, schalten die Mikroglia in einen maladaptiven Modus, schälen aggressiv Myelin ab und treiben den neurologischen Abbau voran. Für ein allgemeines Publikum ist die Kernbotschaft: Die Immunzellen des Gehirns sind nicht einfach gut oder schlecht; ihr Verhalten hängt stark von lokalen Verdrahtungsanforderungen und von molekularen Bremsen wie TGFβ ab. Da TGFβ‑blockierende Medikamente für Krebs und einige Hirnerkrankungen entwickelt werden, liefert diese Arbeit eine wichtige Warnung: Die Störung dieses Weges, insbesondere bei älteren Menschen, könnte unbeabsichtigt verletzliche Bereiche des Rückenmarks schädigen, indem sie Mikroglia auf die Isolierung loslässt, die unsere Nerven zum Funktionieren benötigen.
Zitation: Zhu, K., Liu, Y., Min, JH. et al. TGFβ signaling mediates microglial resilience to spatiotemporally restricted myelin degeneration. Nat Neurosci 29, 617–631 (2026). https://doi.org/10.1038/s41593-025-02161-4
Schlüsselwörter: Mikroglia, Myelinalterung, Hinterstrang des Rückenmarks, TGF‑beta-Signalgebung, Neuroinflammation