Clear Sky Science · de
Gerüste mit optimierter quartärer Symmetrie zur de-novo-cryoEM-Strukturbestimmung kleiner RNAs
Die kleinsten Formen der RNA sichtbar machen
In jeder Zelle falten sich kurze RNA-Stränge zu winzigen dreidimensionalen Formen, die Gene an- oder ausschalten, zelluläre Schäden erkennen oder unter dem Mikroskop aufleuchten. Viele dieser RNAs sind so klein, dass gängige Bildgebungsverfahren Schwierigkeiten haben, ihre genaue Architektur aufzudecken. Dieser Artikel stellt einen raffinierten Weg vor, diese schwer fassbaren Moleküle sichtbar zu machen: indem man sie an einen größeren, sich selbst organisierenden RNA-„Rahmen“ befestigt, der mit kryo‑Elektronenmikroskopie—einem leistungsfähigen Verfahren zur Abbildung eingefrorener Biomoleküle—klar erkennbar ist.
Aufbau eines nützlichen RNA‑Rahmens
Die Autoren begannen mit einem RNA‑Abschnitt aus einem Virus, der natürlicherweise dazu neigt, sich paarweise zu verbinden. Sie überarbeiteten dieses Segment so, dass es sich nun nicht mehr nur gelegentlich paart, sondern in Lösung fast immer hochregelmäßige zwei‑teilige oder vier‑teilige Strukturen bildet. Diese sich wiederholenden Anordnungen erzeugen im Grunde einen RNA‑Rahmen oder ein Gerüst mit eingebauter Symmetrie. Symmetrie ist für die kryo‑Elektronenmikroskopie wertvoll, weil identische Wiederholungseinheiten gemittelt werden können, was das finale Bild schärft.
Bekannte RNAs als Testgäste anbringen
Um zu prüfen, ob ihr Gerüst andere RNAs sichtbar machen kann, hefteten die Forschenden gut untersuchte Moleküle an eine Region des Rahmens. Ein Gast war eine bakterielle Transfer‑RNA, eine klassische L‑förmige Einheit, die während der Proteinsynthese Aminosäuren liefert. Ein anderer war Mango‑III, ein kleines, konstruiertes RNA‑Aptamer, das einen Farbstoff bindet und aufleuchtet und häufig als fluoreszierender Marker verwendet wird. In beiden Fällen falteten und paarten sich die kombinierten Moleküle wie geplant, und die kryo‑Elektronenmikroskopie lieferte detaillierte Karten der Gesamtformen. Bei der Transfer‑RNA waren die Bilder scharf genug, um subtile Unterschiede zwischen der hier verwendeten, unveränderten Form und zuvor untersuchten, chemisch modifizierten Varianten zu erkennen. Bei Mango‑III zeigten die Karten, dass das Aptamer deutlich starrer wird, wenn sein Farbstoff gebunden ist, was erklärt, wie die Bindung die Fluoreszenz einschaltet. 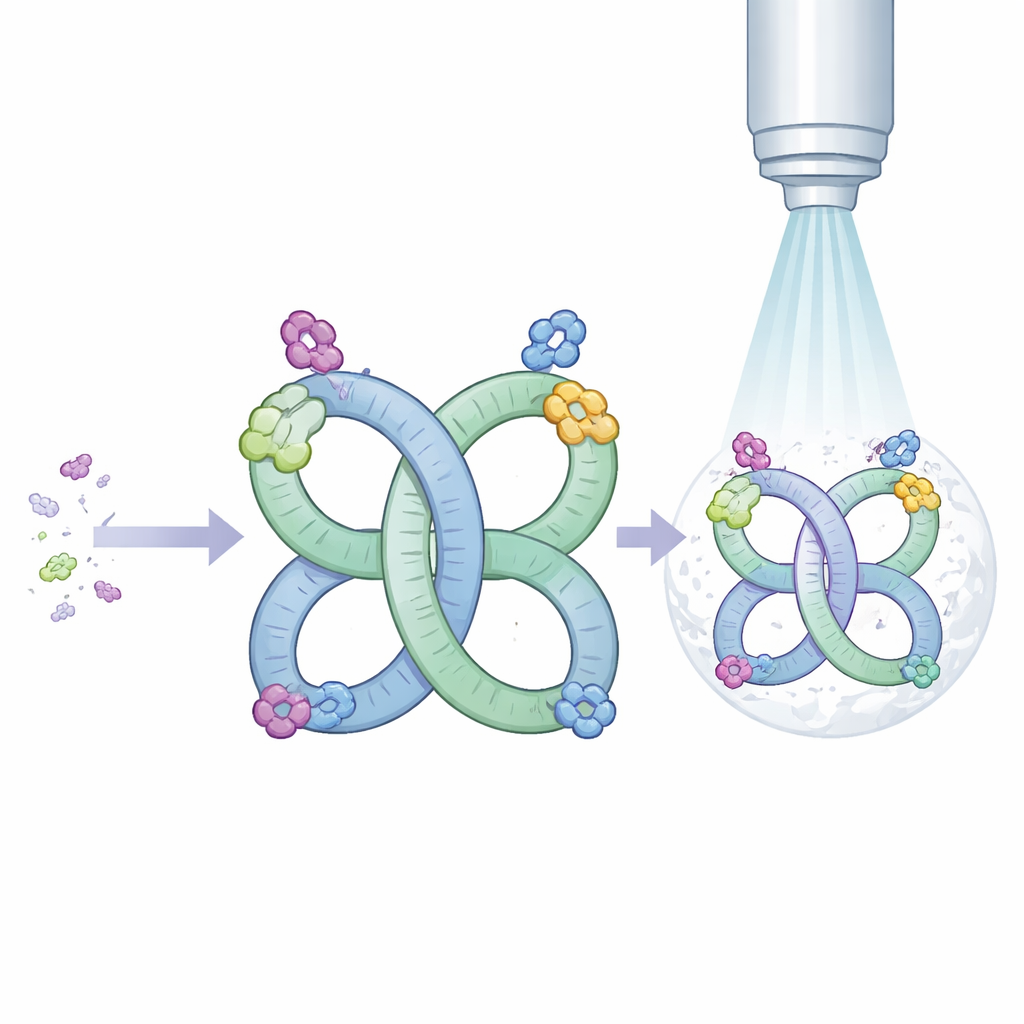
Aufdecken, wie Designer‑RNAs kleine Moleküle fassen
Das Team ging dann über Testfälle hinaus zu RNAs, deren vollständige Strukturen noch nicht gesehen worden waren. Sie befestigten zwei kleine Aptamere—kurze RNAs, die im Labor ausgewählt wurden, um bestimmte kleine Moleküle zu binden—an dem Gerüst. Ein Aptamer erkennt das Medikament Chinin; das andere erkennt 8‑Oxoguanin, eine beschädigte Variante einer genetischen Base, die bei Bakterien auf oxidativen Stress hinweist. Dank des Gerüsts lieferte die kryo‑Elektronenmikroskopie außergewöhnlich hochwertige Karten, fein genug, um jede RNA‑Kette von Ende zu Ende nachzuverfolgen und zu sehen, wo Metallionen und Wassermoleküle sitzen. Im Chinin‑Aptamer umschließt die Bindetasche das Medikament vorwiegend durch enges Stapeln und Formkomplementarität, mit überraschend wenigen direkten Wasserstoffbrücken. Im Gegensatz dazu umgibt das 8‑Oxoguanin‑Aptamer sein Ligand mit einem komplexen Netz aus Wasserstoffbrücken, die fast jede chemisch unterschiedliche Stelle der beschädigten Base kontaktieren, was seine scharfe Unterscheidung zwischen 8‑Oxoguanin und normalem Guanin erklärt.
Flexible Symmetrie für klarere Bilder
Interessanterweise kann dasselbe RNA‑Gerüst je nach Bedingungen und angehängtem Gast entweder zwei‑teilige oder vier‑teilige Strukturen bilden. Wenn eine vierteilige Anordnung entsteht, verbessert die wiederholte Geometrie die Bildqualität weiter. In einem Fall nahm das Gerüst eine vierteilige Form an, obwohl seine Sequenz identisch mit der zweigeteilten Version war, was verdeutlicht, wie kleine Verschiebungen in der Basenpaarung die gesamte Assemblierung umgestalten können. Die Autoren untersuchten außerdem praktische Aspekte der kryo‑Elektronenmikroskopie‑Datenerhebung, etwa wie das Kippen der Platte bevorzugte Orientierungen der Partikel auf dem Gitter überwinden kann und wie die auferlegte Symmetrie während der Bildverarbeitung die resultierenden Strukturen moderat, aber konsistent schärft.
Ein neues Fenster zu winzigen RNA‑Maschinen
Insgesamt zeigt diese Arbeit, dass ein kompakter, symmetrischer RNA‑Rahmen ansonsten unsichtbare kleine RNAs in exzellente Ziele für die kryo‑Elektronenmikroskopie verwandeln kann und in günstigen Fällen Strukturen bis über die atomare Detailhöhe hinaus ermöglicht. Durch das Anbringen einer unbekannten RNA an das Gerüst über einen einfachen helicalen Verbinder können Forschende nun ihre dreidimensionale Faltung bestimmen, genau sehen, wie sie ein kleines Molekül fässt, und geordnete Metallionen und Wassermoleküle erkennen, die ihr Verhalten feinabstimmen. Für ein allgemeines Publikum lautet die Kernbotschaft: Wir verfügen jetzt über ein praktisches Werkzeug, um einige der kleinsten und vielseitigsten RNA‑Maschinen der Natur und Biotechnologie genau zu betrachten, was den Weg für das rationale Design neuer RNA‑basierter Sensoren, Medikamente und molekularer Geräte ebnet. 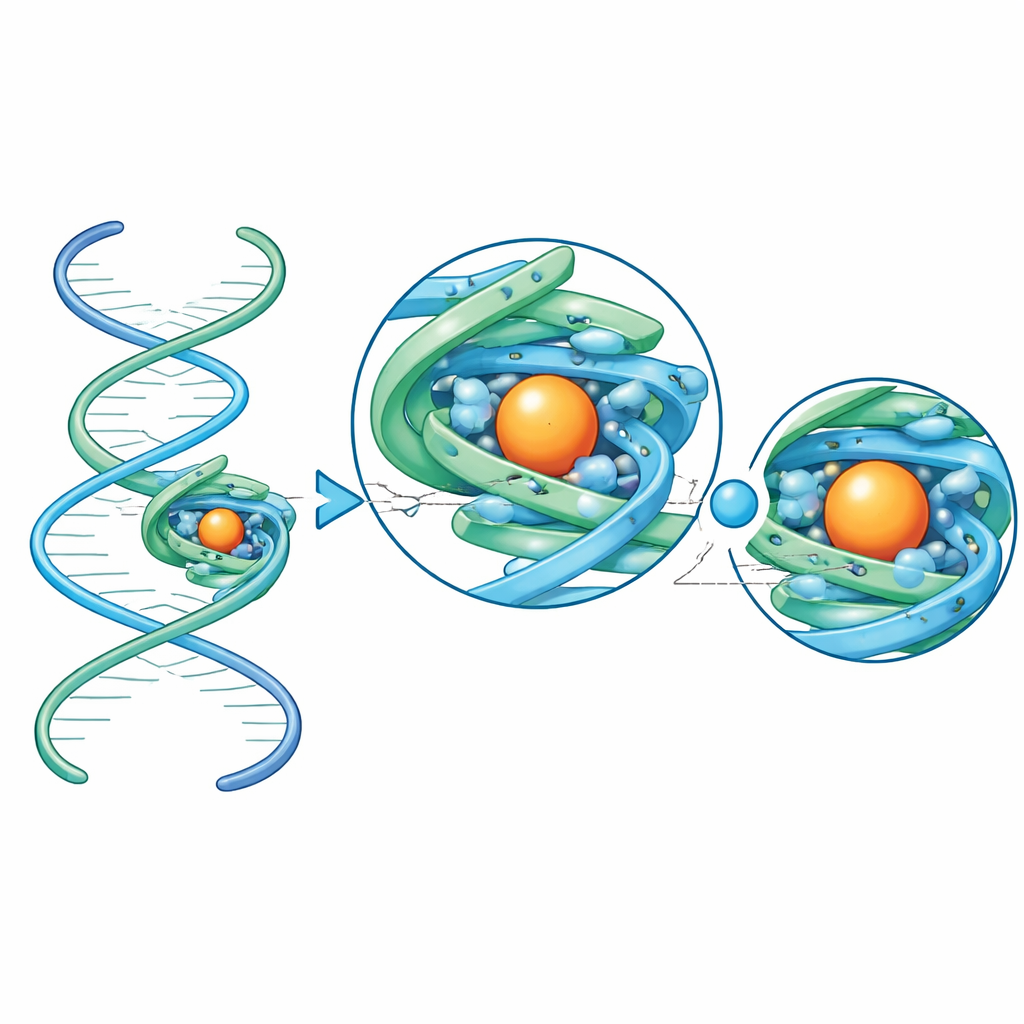
Zitation: Jones, C.P., Ferré-D’Amaré, A.R. Scaffolds with optimized quaternary symmetry for de novo cryoEM structure determination of small RNAs. Nat Methods 23, 609–616 (2026). https://doi.org/10.1038/s41592-026-03016-x
Schlüsselwörter: RNA-Struktur, kryoelektronenmikroskopie, Aptamer, Riboschalter, molekulare Gerüste