Clear Sky Science · de
Nächste Generation mehrfarbiger Indikatoren für die in vivo-Bildgebung von Noradrenalin
Einen verborgenen Boten im Gehirn sichtbar machen
Noradrenalin ist eine chemische Substanz im Gehirn, die stillschweigend beeinflusst, wie wir aufwachen, Aufmerksamkeit steuern, Erinnerungen bilden und auf Stress reagieren. Bis vor kurzem konnten Forschende seine Aktivität nur mit langsamen oder ungenauen Werkzeugen erahnen. Dieser Artikel stellt ein neues Paar leuchtender Marker vor, mit denen Forschende Noradrenalin im lebenden Gehirn in Echtzeit und mit feiner Auflösung verfolgen können. Diese Fortschritte könnten unser Verständnis von Schlaf, Angst, Lernen und neurodegenerativen Erkrankungen vertiefen.
Warum die Verfolgung dieses Signals so schwierig war
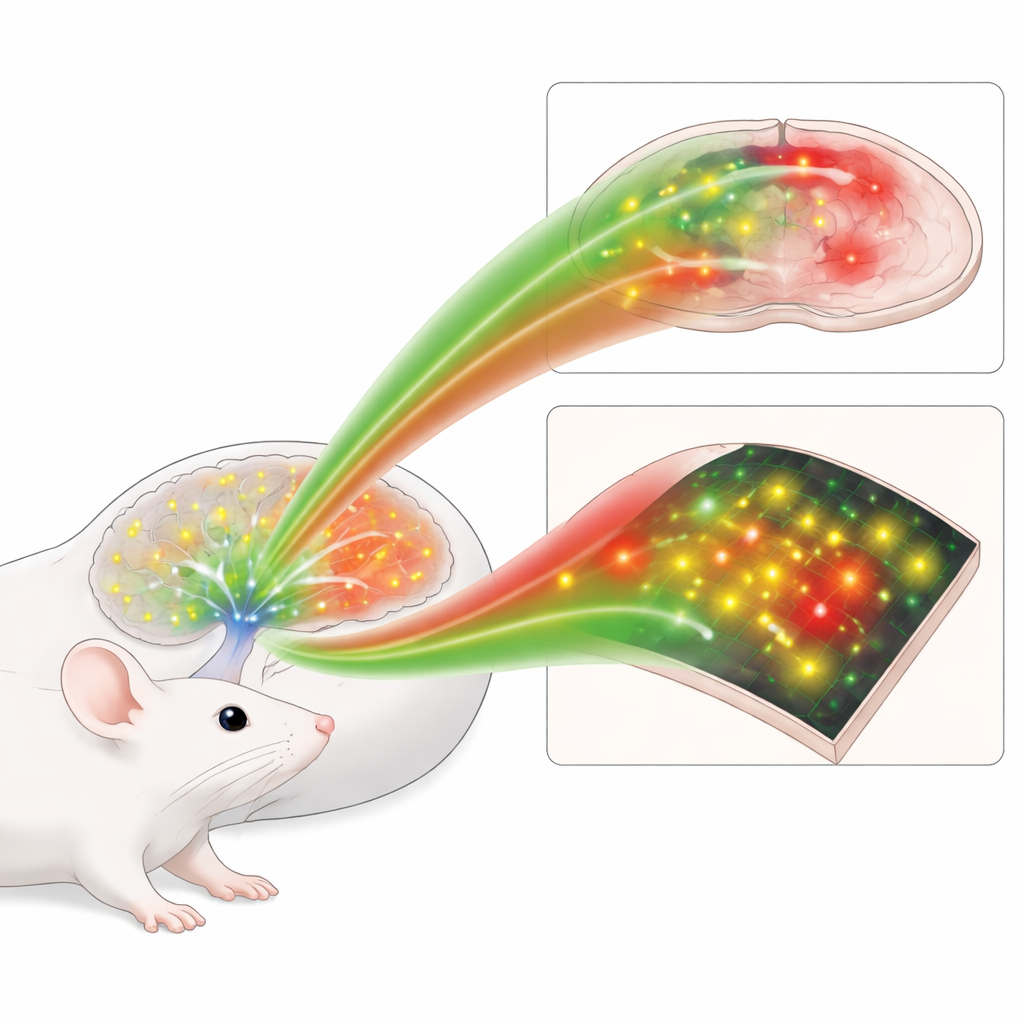
Noradrenalin wird von einer kleinen Gruppe von Hirnstammzellen freigesetzt, die Fasern durch das Gehirn senden und die Funktionsweise von Schaltkreisen verändern, anstatt sie einfach ein- oder auszuschalten. Klassische Messmethoden, wie winzige chemische Sonden oder implantierte Zellen, die auf Noradrenalin reagieren, verwischen Ereignisse über viele Sekunden oder können es nicht sauber von verwandten Molekülen unterscheiden. Eine neuere Strategie verwendet modifizierte zelloberflächenständige Rezeptoren, die heller werden, wenn sie Noradrenalin binden, und so eine lichtbasierte Ablesung ermöglichen. Die Erstgeneration war jedoch vergleichsweise schwach, besonders im roten Spektralbereich, und nicht flexibel genug für Experimente, die mehrere Farben gleichzeitig erforderten.
Bessere grüne und rote Wächter entwickeln
Die Autorinnen und Autoren entwickelten verbesserte grüne und rote Indikatoren, genannt nLightG2 und nLightR2, indem sie Bausteine früherer Dopamin- und Noradrenalin-Sensoren kombinierten und systematisch Dutzende Mutationen testeten. Diese Änderungen machten die Sensoren deutlich heller in Gegenwart von Noradrenalin, ohne ihr Grundleuchten stark zu verändern. In Zellkulturen zeigten die neuen Werkzeuge mehrerefach größere Reaktionen auf Noradrenalin als frühere Versionen, sprachen innerhalb von wenigen zehn Millisekunden an und stellten sich in weniger als einer Sekunde zurück. Sie reagierten zudem kaum auf andere Gehirnchemikalien wie Dopamin und aktivierten nicht die eigenen intrazellulären Signalwege der Zellen — ein wichtiger Sicherheitscheck, um sicherzustellen, dass sie Beobachter und keine Teilnehmer sind.
Ihre Leistungsfähigkeit im Hirngewebe beweisen
Als Nächstes brachten die Forschenden die Sensoren in Schnittpräparate von Mausgehirn ein und verglichen alte und neue Designs mit Zwei-Photonen-Mikroskopie, die tief ins Gewebe blickt. Wenn Noradrenalin auf das Gewebe gepuffert wurde oder lokale Fasern elektrisch stimuliert wurden, um es natürlich freizusetzen, erzeugten nLightG2 und nLightR2 deutlich größere und leichter erkennbare Aufhellungen als frühere Sensoren. Die grünen und roten Werkzeuge arbeiteten ähnlich schnell, sodass die Farbwahl nicht mehr auf Kosten der Geschwindigkeit erfolgen muss. Diese höhere Empfindlichkeit erlaubte es den Forschenden, räumlich zu kartieren, wo Noradrenalin ausbreitete, statt lediglich zu wissen, dass es irgendwo im Sichtfeld freigesetzt worden war.
Gehirnzustände, Angst und Navigation in Aktion beobachten
Das eigentliche Potenzial dieser Werkzeuge zeigt sich bei lebenden Tieren. Mithilfe haarfeiner Glasfasern kombinierten die Autorinnen und Autoren den roten Noradrenalin-Indikator mit einem grünen Calciumsensor, der die Aktivität von Nervenzellen anzeigt. Im Schlafzentrum des Gehirns beobachteten sie, dass aufeinanderfolgende Aktivitätsausbrüche in noradrenalinproduzierenden Zellen während des Tiefschlafs jeweils kurz darauf von lokalen Anstiegen des Noradrenalinspiegels gefolgt wurden. In der Amygdala, einer für Emotionen wichtigen Region, zeigte der grüne Noradrenalin-Sensor, dass ein harmloser Ton nach Paarung mit einem leichten Schock eine anhaltende Erhöhung von Noradrenalin auslöste — ein Abbild der Verstärkung von Angsterinnerungen. Im Hippocampus, der beim Erfassen von Raum hilft, wurde der rote Sensor zusammen mit einem grünen Astrozyten-Calciumsensor während der Durchquerung eines virtuellen Korridors zu Wasserbelohnungen abgebildet. Dort war die Astrozytenaktivität in Belohnungsnähe eng mit lokalen Noradrenalin-Spitzen verknüpft und deutet auf einen Dialog zwischen diesem Neurotransmitter und Stützzellen während belohnender Erfahrungen hin.
Winzige Aktivitätstaschen im visuellen Kortex sichtbar machen
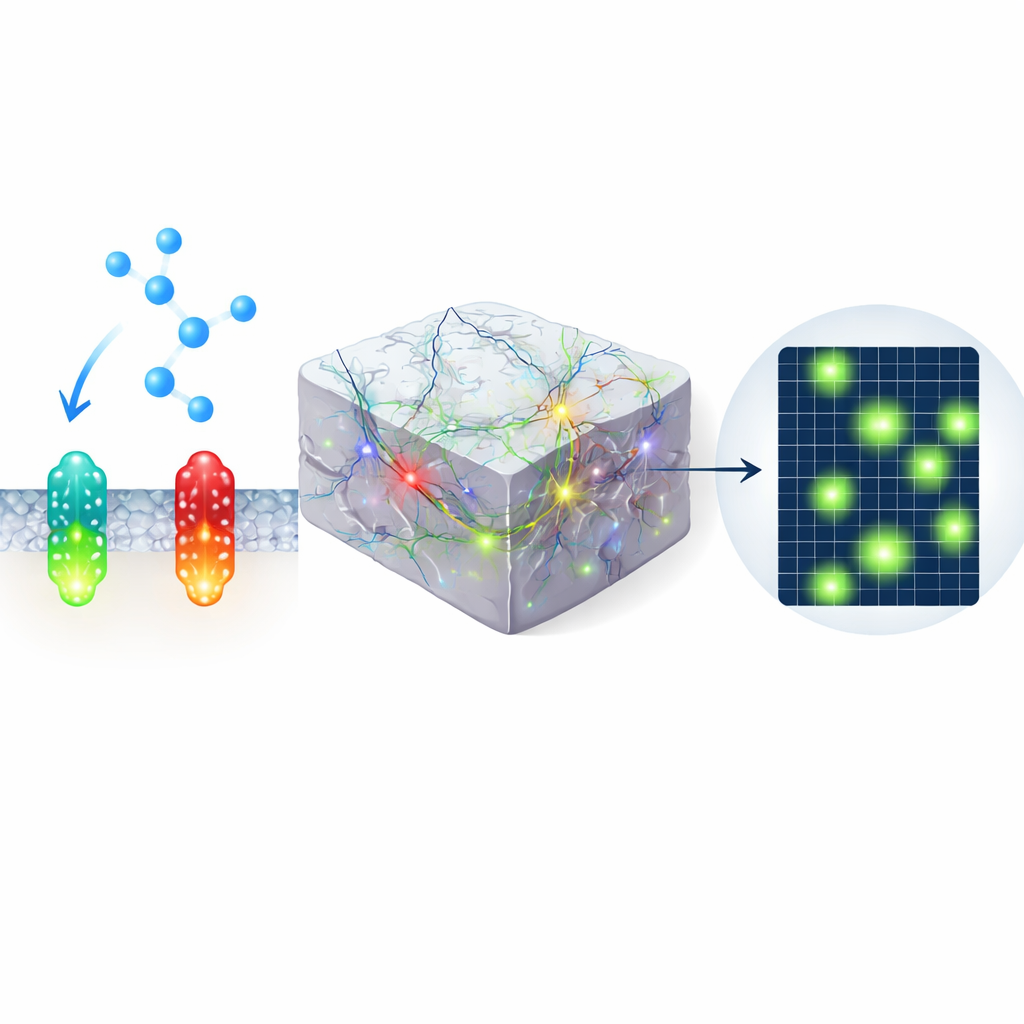
In einer weiteren Experimentreihe exprimierten die Autorinnen und Autoren den grünen Sensor im visuellen Kortex wacher Mäuse und bildeten ihn mit Zwei-Photonen-Mikroskopie ab, während die Tiere bedrohlich herannahende Reize betrachteten und zwischen Ruhe und Laufen wechselten. Statt eines gleichmäßigen Signals fanden sie kurze, hochlokalisierte Fluoreszenz-Patches — Mikrodomänen — verteilt über das Sichtfeld. Einige Mikrodomänen reagierten bevorzugt auf die visuelle Bedrohung, andere auf Bewegung, und viele leuchteten spontan auf. Diese Muster waren mit einem älteren grünen Sensor oder einer mutierten nicht bindenden Kontrolle weitgehend unsichtbar, was die verbesserte Empfindlichkeit von nLightG2 unterstreicht und darauf hindeutet, dass Noradrenalin die Hirnaktivität viel feiner formt, als zuvor angenommen.
Was das für die Hirnforschung bedeutet
Insgesamt zeigen diese Ergebnisse, dass nLightG2 und nLightR2 ein leistungsfähiges Werkzeugset bilden, um Noradrenalin im lebenden Gehirn zu beobachten, über Skalen von einzelnen Mikrodomänen bis hin zu ganzen Verhaltenszuständen. Da sie in unterschiedlichen Farben vorliegen und mit anderen fluoreszenten Reportern kombiniert werden können, können Forschende nun Noradrenalin gleichzeitig mit elektrischen oder Calcium-Signalen in spezifischen Zelltypen während Schlaf, Lernen oder Stress verfolgen. Die Fähigkeit zu sehen, wann und wo dieser wichtige Neuromodulator wirkt, könnte letztlich klären, wie er gesunde Aufmerksamkeit und Gedächtnis unterstützt und wie seine Dysfunktion zu Erkrankungen wie Angststörungen, Depression und neurodegenerativen Leiden beiträgt.
Zitation: Rohner, V.L., Curreli, S., Lamothe-Molina, P.J. et al. Next-generation multicolor indicators for in vivo imaging of norepinephrine. Nat Methods 23, 636–652 (2026). https://doi.org/10.1038/s41592-026-03006-z
Schlüsselwörter: Noradrenalin, Neuromodulation, genetisch kodierte Sensoren, Zwei-Photonen-Bildgebung, Schlaf und Lernen