Clear Sky Science · de
Massenverteilung von Azithromycin und Antibiotikaresistenz im Darm und in der Nasopharynx: eine cluster-randomisierte Studie
Warum eine Tablette für viele Kinder wichtig ist
In Teilen Westafrikas wurde ein einzelnes Antibiotikum, Azithromycin, in Massencampagnen eingesetzt, um die Zahl der an Infektionen sterbenden Kleinkinder zu verringern. Die Strategie wirkt – zugleich wirft sie eine gravierende Frage auf: Züchten wir stillschweigend widerstandsfähigere, medikamentenresistente Keime in den Körpern der Kinder heran? Diese Studie, durchgeführt in Hunderten von Dörfern in Niger, blickt genau in die Därme und Nasen von Kindern, um zu untersuchen, wie wiederholte, gemeinschaftsweite Behandlungen ihre versteckte mikrobielle Welt und die Antibiotikaresistenz verändern.
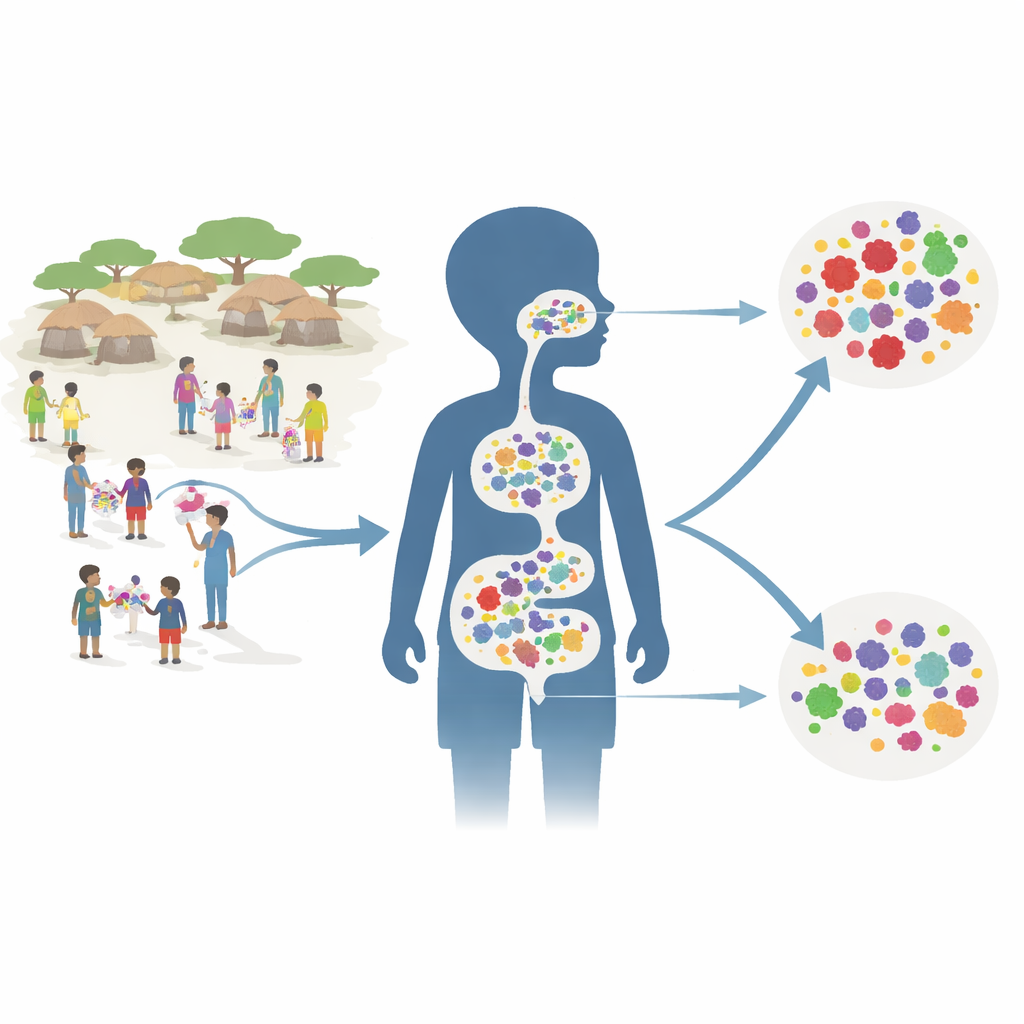
Prüfung eines gemeinschaftlichen Medikamentenplans
Die Forschenden betteten ihre Arbeit in eine große Studie namens AVENIR ein, die bereits gezeigt hatte, dass die Gabe von Azithromycin alle sechs Monate an alle Kinder im Alter von 1 bis 59 Monaten die Sterblichkeit in dieser Altersgruppe senken kann. Für die Resistenzstudie konzentrierten sie sich auf 150 zufällig ausgewählte Dörfer. Jedes Dorf gehörte zu einer von drei Gruppen: alle Kleinkinder erhielten Azithromycin; nur Säuglinge bis 11 Monate erhielten Azithromycin, während ältere Kleinkinder und Vorschulkinder ein Placebo erhielten; oder alle Kinder erhielten Placebo. Zwei Jahre nach Beginn des Programms – sechs Monate nach der vierten Behandlungsrunde – sammelte das Team rektale und tiefe Nasenabstriche von etwa 30 Kindern pro Dorf.
Ein Blick in Darm und Nase
Statt Keime im Labor anzuzüchten, pooled die Wissenschaftler die Proben pro Dorf und nutzten moderne DNA-Sequenzierung. Dadurch konnten sie katalogisieren, welche Bakterien vorhanden waren, und genetische Marker zählen, die auf Resistenz gegenüber verschiedenen Antibiotikagruppen hinweisen. Sie richteten besonderes Augenmerk auf Makrolide – die Wirkstoffgruppe, zu der Azithromycin gehört – und suchten zugleich nach Resistenz gegen viele andere häufig eingesetzte Antibiotikatypen, etwa ß-Laktam-Antibiotika. Darm und Nasopharynx (der obere Teil des Rachens hinter der Nase) wurden untersucht, weil beide wichtige Reservoirs sind, in denen Resistenzgene sich ansammeln und potenziell verbreiten können.
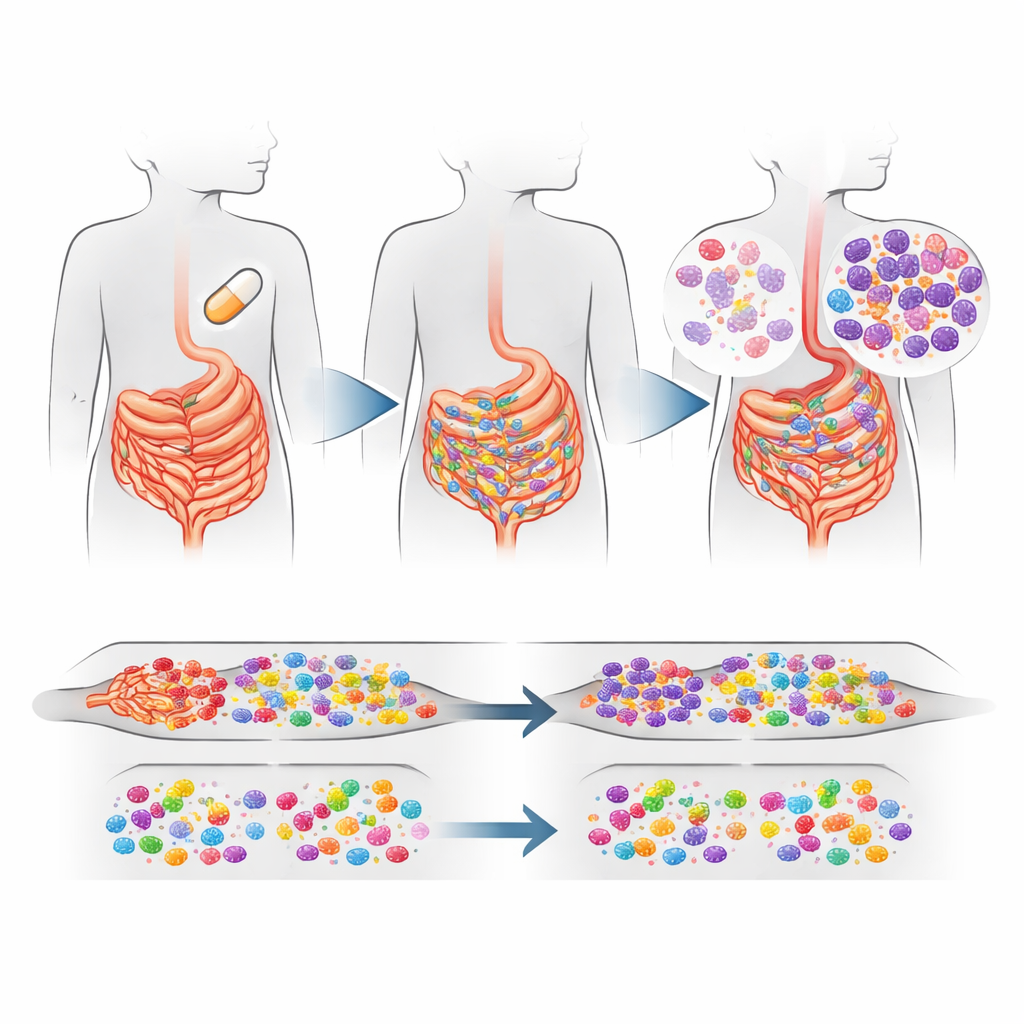
Was sich im Darm der Kinder veränderte
Das klarste Signal kam aus dem Darm. In Dörfern, in denen alle Kinder Azithromycin erhielten, gab es einen moderaten, aber statistisch verlässlichen Anstieg – etwa 16 % höher insgesamt – von Makrolid-Resistenzgenen in den Darmbakterien im Vergleich zu Placebo-Dörfern. Der Anstieg wurde hauptsächlich durch ein Resistenzgen getrieben, das ermF heißt und Bakterien gegen Makrolid-Wirkstoffe schützt. Dieses Gen wird häufig von verbreiteten Darmbakterien wie Bacteroides und Prevotella getragen, die normalerweise harmlos im Darm leben, aber gelegentlich Erkrankungen verursachen können. Interessanterweise nahmen Resistenzgene gegen andere wichtige Antibiotikagruppen nicht zu, und die Gesamtzusammensetzung sowie die Diversität der Darmflora wirkten zwischen den Behandlungsgruppen weitgehend ähnlich, obwohl einige spezifische Arten häufiger oder seltener wurden.
Was in der Nase gleich blieb
Im Gegensatz dazu erzählten die Nasengänge eine ruhigere Geschichte. Die Studie fand keine klaren, statistisch belastbaren Unterschiede in Makrolid-Resistenzgenen zwischen den Behandlungsgruppen in der Nasopharynx-Proben, noch Hinweise darauf, dass dort eine Selektion für Resistenz gegen andere Antibiotikaklassen stattfand. Die typischen Nasenbewohner – Gattungen wie Moraxella, Haemophilus und Streptococcus – blieben dominant. Einige paarungsbezogene Mundbakterien, die mit Zahnfleischerkrankungen in Verbindung stehen, wurden in Azithromycin-behandelten Gemeinden häufiger, und einige davon können ebenfalls Resistenzgene tragen, aber die Gesamtlaste an Resistenzen in der Nase verschob sich nicht so wie im Darm.
Abwägen der heutigen Gewinne gegen die Risiken von morgen
Insgesamt zeigen die Ergebnisse, dass die Gabe von Azithromycin an alle Kleinkinder einer Gemeinschaft Leben retten kann, sie lenkt jedoch die Darmbakterien in Richtung größerer Resistenz gegen diese Wirkstoffgruppe, vor allem durch die Ausbreitung spezifischer Resistenzgene wie ermF. Die Studie fand innerhalb des zweijährigen Beobachtungszeitraums keinen Übergriff auf Resistenz gegen andere Antibiotikatypen und auch keine starken Veränderungen im nasalen Reservoir, doch warnen die Autorinnen und Autoren, dass resistente Darmbakterien und ihre Gene sich über Zeit und zwischen Personen ausbreiten können. Sie plädieren dafür, dass jedes breit angelegte Antibiotikaprogramm zur Senkung der Kindersterblichkeit eine sorgfältige, langfristige Überwachung der Resistenz beinhalten sollte, damit Gesundheitsbehörden den unmittelbaren Nutzen weniger Kindertodesfälle gegen die langsamere, weniger sichtbare Belastung durch zunehmende medikamentenresistente Mikroben abwägen können.
Zitation: Doan, T., Yan, D., Arzika, A.M. et al. Mass azithromycin distribution and antibiotic resistance in the gut and nasopharynx: a cluster-randomized trial. Nat Med 32, 859–868 (2026). https://doi.org/10.1038/s41591-026-04217-9
Schlüsselwörter: Azithromycin, Kindersterblichkeit, Antibiotikaresistenz, Darmmikrobiom, Massenmedikation