Clear Sky Science · de
Einzellzell‑Atlas des sich entwickelnden Kortex bei Trisomie 21
Warum diese Forschung wichtig ist
Das Down‑Syndrom ist die häufigste genetische Ursache geistiger Behinderung, dennoch wissen wir noch wenig darüber, wie es das sich entwickelnde menschliche Gehirn vor der Geburt verändert. Diese Studie fährt bis auf die Ebene einzelner Zellen in den fetalen Kortex heran — dem Hirnareal, das für Denken und Gedächtnis entscheidend ist —, um zu kartieren, was schiefläuft, wann es beginnt und welche molekularen Schalter potenziell ansteuerbar sind.
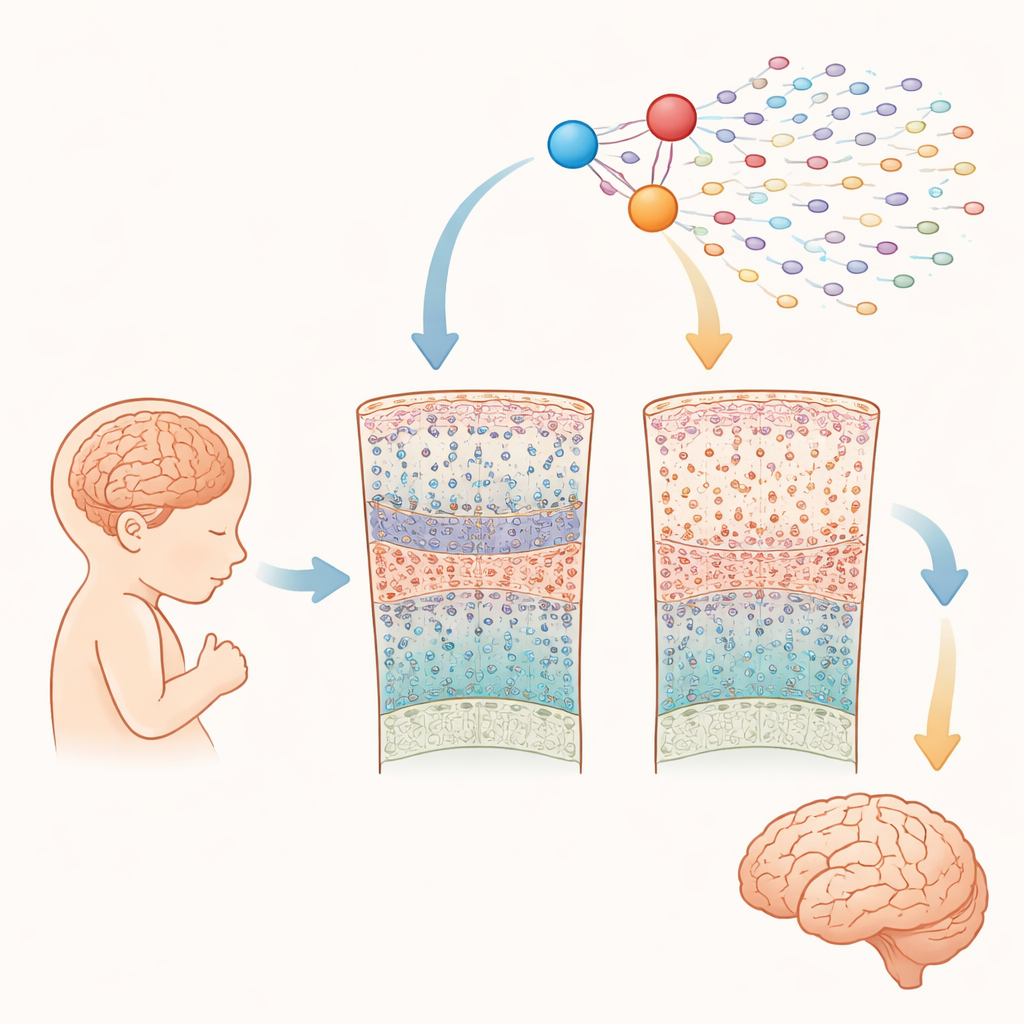
Genauer Blick auf das wachsendes Gehirn
Die Forschenden analysierten fast eine Viertelmillion Zellen aus dem Cerebralkortex von 15 Föten mit Down‑Syndrom und 15 ohne, im Zeitraum von 10 bis 20 Wochen nach der Empfängnis. Mit fortgeschrittenen Single‑Cell‑Methoden maßen sie sowohl, welche Gene in jeder Zelle aktiviert waren, als auch die Zugänglichkeit der DNA. Dadurch konnten sie alle wichtigen Zelltypen identifizieren, die in diesem mittleren Schwangerschaftsabschnitt vorhanden sind — etwa stammzellähnliche Vorläuferzellen, verschiedene Typen exzitatorischer und inhibitorischer Neurone sowie frühe Gliazellen — und deren Häufigkeit und Genaktivität zwischen Down‑Syndrom‑ und typischen Gehirnen vergleichen.
Frühe Veränderungen in Schlüsselneuronen
Die meisten übergreifenden Zellklassen waren in diesem frühen Fenster in beiden Gruppen in ähnlicher Anzahl vorhanden. Auffällig war jedoch ein selektives Defizit eines bestimmten Typs exzitatorischer Neurone, die normalerweise in Schicht 4 des Kortex liegen und wichtig für die Verarbeitung eingehender Informationen sind. Diese Neurone sind durch die Proteine RORB und FOXP1 definiert. Bei Föten mit Down‑Syndrom waren RORB–FOXP1‑Neurone bereits zur Mitte der Schwangerschaft reduziert, insbesondere zwischen der 16. und 20. Woche, während andere Neurontypen relativ verschont schienen. Das deutet darauf hin, dass Störungen in der Entstehung oder Reifung dieser Untergruppe pränatal beginnen und direkt zu späteren kognitiven Beeinträchtigungen beitragen können.
Gestörte genetische Programme und Schaltzentralen
Über die reinen Zellzahlen hinaus zeigte die Studie, dass Hunderte Gene subtil fehlreguliert sind, besonders in exzitatorischen Neuronen und deren Vorläufern. Viele dieser Gene sind an der Bildung des Vorderhirns, der Ausbildung von Neuriten, der Entstehung von Vernetzungen und an höheren Hirnfunktionen beteiligt. Mehr als nur die zusätzlichen Kopien von rund 200 Genen auf Chromosom 21 scheinen betroffen zu sein; die Daten deuten auf ein gestörtes Netzwerk der Genregulation hin. Mit einem Ansatz, der Genaktivität und DNA‑Zugänglichkeit kombiniert, skizzierten die Autoren regulatorische Schaltkreise und hoben drei auf Chromosom 21 codierte Transkriptionsfaktoren — BACH1, PKNOX1 und GABPA — als dosisempfindliche »Hubs« hervor. Diese Moleküle scheinen andere kritische Regulatoren der Kortexentwicklung zu beeinflussen, darunter Faktoren, die schon mit geistiger Behinderung in Verbindung gebracht wurden, und erklären, wie eine moderate 1,5‑fache Erhöhung der Genkopiezahl Entwicklungsprogramme weitreichend stören kann.
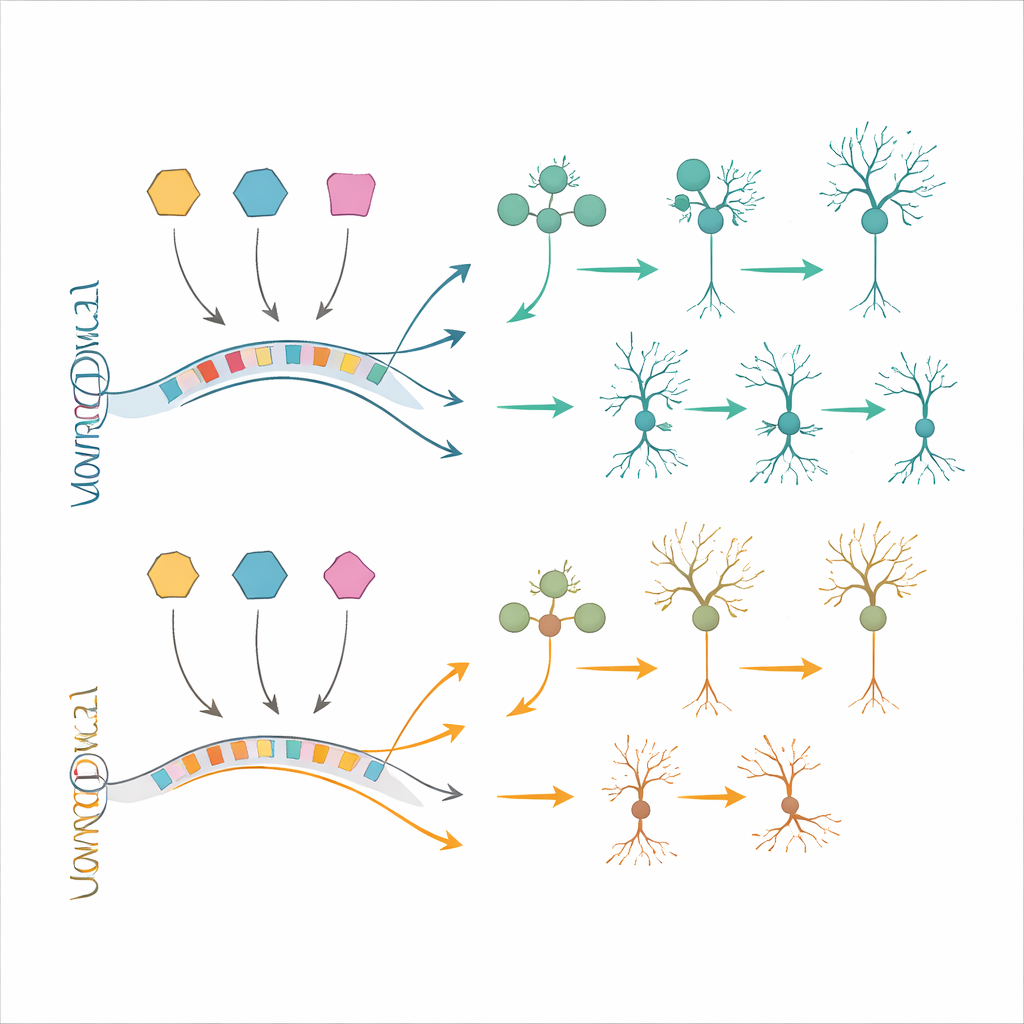
Testen von Rettungsstrategien in Zellen und lebenden Gehirnen
Um zu prüfen, ob sich diese molekularen Veränderungen korrigieren lassen, arbeiteten die Forschenden mit Stammzellmodellen. Sie erzeugten neuronale Vorläuferzellen und Neurone aus induzierten pluripotenten Stammzellen mit Trisomie 21 und aus passenden Kontrollzellen. Viele der in fetalem Gewebe beobachteten Genexpressionsänderungen traten in diesen im Labor gezüchteten Zellen erneut auf, was die Relevanz der Modelle bestätigte. Anschließend setzten sie antisense Oligonukleotide — kurze, gentechnisch veränderte DNA‑ähnliche Stränge — ein, um BACH1, PKNOX1 oder GABPA auf nahezu normale Werte herunterzuregeln. Diese partielle Normalisierung der überexprimierten Transkriptionsfaktoren führte zu einer teilweisen Erholung mehrerer nachgeschalteter Gene, darunter solchen, die mit geistiger Behinderung und neuronaler Differenzierung verknüpft sind. Ergänzend transplantierten sie menschliche trisomie‑21‑neurale Zellen in Mausgehirne und ließen sie in vivo reifen. Diese Transplantate reproduzierten zusätzliche Down‑Syndrom‑ähnliche Merkmale, wie ein verändertes Neuron‑Glia‑Verhältnis und Genänderungen, die in Zellkulturen nicht vollständig abgebildet wurden, und bieten damit einen kraftvollen Prüfstand für künftige Therapien.
Was das für die Zukunft bedeutet
In der Summe liefert die Arbeit einen detaillierten Atlas dazu, wie das Down‑Syndrom die genetische Landschaft des sich entwickelnden Kortex auf Einzelzell‑Auflösung umgestaltet. Für eine allgemeine Leserschaft lautet die Hauptbotschaft: Das zusätzliche Chromosom fügt nicht einfach ein paar problematische Gene hinzu; es verschiebt zahlreiche miteinander verknüpfte molekulare Schalter, was zu frühen und selektiven Mängeln bestimmter denkbezogener Neurone führt. Indem die Studie eine kleine Gruppe von Chromosom‑21‑Transkriptionsfaktoren als zentrale Akteure identifiziert — und zeigt, dass deren Effekte in menschlichen Zellen teilweise umkehrbar sind —, öffnet sie den Weg für gezieltere Strategien zur Verbesserung der Gehirnentwicklung und -funktion bei Down‑Syndrom.
Zitation: Lattke, M., Tan, W.L., Sukumaran, S.K. et al. Single-cell atlas of the developing Down syndrome brain cortex. Nat Med 32, 1061–1072 (2026). https://doi.org/10.1038/s41591-026-04211-1
Schlüsselwörter: Down-Syndrom, fetale Gehirnentwicklung, Single-Cell-Genomik, kortikale Neurone, Transkriptionsfaktoren