Clear Sky Science · de
CD19 CAR-T-Zellen bei therapieresistenten Autoimmunerkrankungen: die Phase-1/2-CASTLE-Basket-Studie
Warum eine Einmalbehandlung wichtig ist
Viele Menschen mit schweren Autoimmunerkrankungen leben auf einem Karussell aus stetiger Medikation: Schub um Schub und zunehmende Nebenwirkungen. Diese Studie untersucht eine radikal andere Idee: eine einmalige Infusion umprogrammierter Immunzellen, um das Immunsystem „neu zu starten“, sodass es aufhört, den eigenen Körper anzugreifen. Für Patientinnen und Patienten mit schwerem Lupus, Verhärtung von Haut und Organen oder Muskelentzündungen, denen die Optionen ausgegangen sind, könnte ein solcher Reset langanhaltende Erleichterung ohne tägliche Medikamente bedeuten.
Drei schwere Erkrankungen, ein gemeinsames Problem
Systemischer Lupus erythematodes, systemische Sklerose und idiopathische entzündliche Myopathien unterscheiden sich äußerlich—sie betreffen Gelenke, Haut, Lunge, Nieren oder Muskeln—teilen aber einen zentralen Defekt: bestimmte Immunzellen, die B-Zellen genannt werden, schießen fehl und treiben die chronische Entzündung voran. Standardbehandlungen, von Steroiden bis zu starken Immunsuppressiva und Antikörperinfusionen, können Symptome dämpfen, beseitigen aber selten die Ursache. Viele Patienten durchlaufen mehrere Therapien, die nur teilweise wirksam sind oder untragbare Nebenwirkungen verursachen, sodass fortschädigende Organschäden und eine eingeschränkte Lebensqualität zurückbleiben.
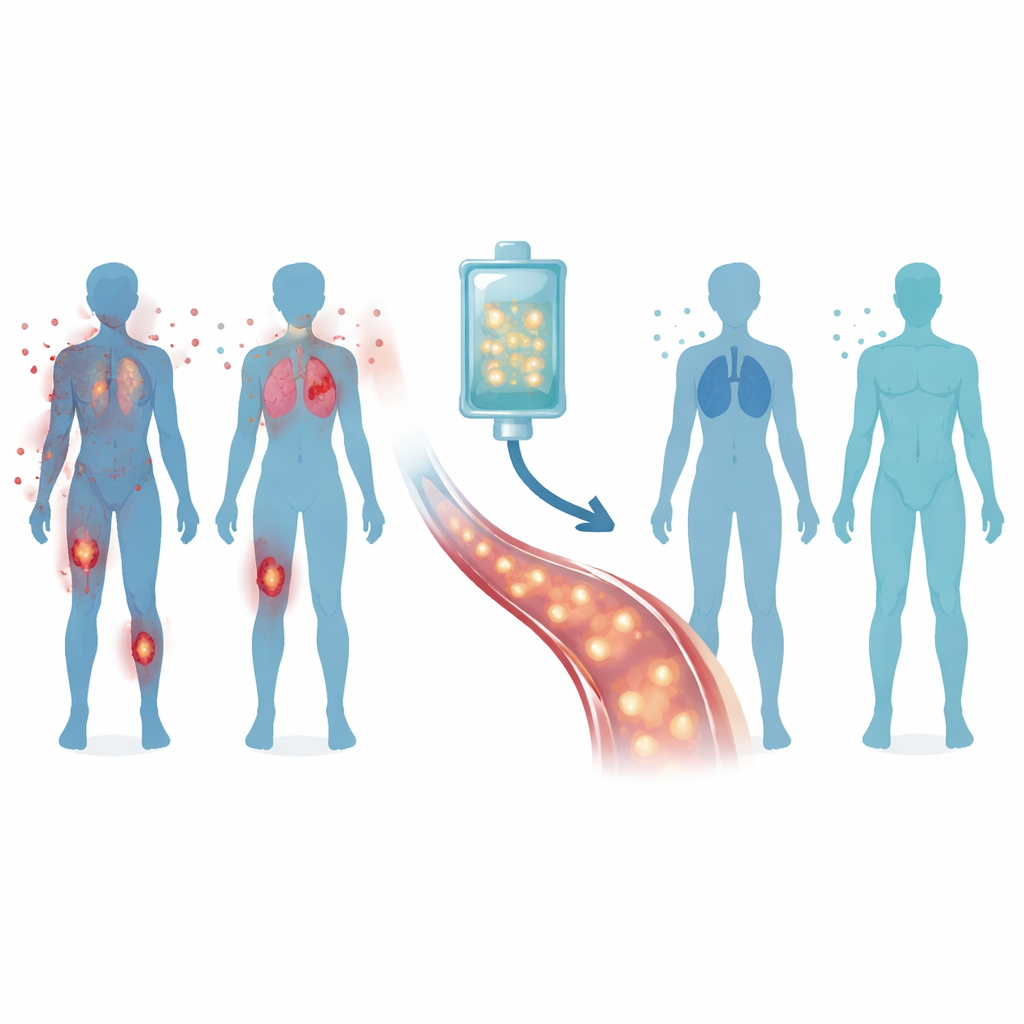
Die Verteidiger des Körpers neu programmieren
Die CASTLE-Studie prüfte eine personalisierte Zelltherapie namens Zorpo-cel bei 24 Erwachsenen mit schweren, therapieresistenten Formen dieser drei Erkrankungen. Ärztinnen und Ärzte entnahmen zunächst die T‑Zellen jedes Patienten, die „Soldaten“ des Immunsystems, und rüsteten sie im Labor mit einem neuen Sensor aus—einem chimären Antigenrezeptor—der ein Molekül namens CD19 erkennt, das auf den meisten B‑Zellen sitzt. Nach einer kurzen Chemotherapie, um im Immunsystem Platz zu schaffen, erhielten die Patienten eine einmalige Infusion dieser modifizierten Zellen, bekannt als CD19 CAR‑T‑Zellen. Die Hoffnung war, dass sie die fehlgesteuerten B‑Zellen aufspüren und entfernen, sodass ein gesünderes Zellensemble nachwachsen kann.
Sicherheit zuerst, dann Anzeichen von Besserung
Da diese Behandlung bei Krebspatienten intensiv sein kann, war das Hauptziel dieser frühen Studie die Sicherheit. Die Forschenden beobachteten genau eine potenziell gefährliche Entzündungsreaktion namens Zytokin-Freisetzungs-Syndrom sowie neurologische Nebenwirkungen. In CASTLE hatten fast drei Viertel der Patienten nur milde, kurzlebige Fieber und Entzündungszeichen; es traten keine schweren Zytokinstürme, keine Hirntoxizität und keine dauerhaften Blutbildstörungen auf. Häufigste Probleme waren vorübergehende Abnahmen der weißen Blutkörperchen und leichte Infektionen, die mit Standardmaßnahmen behandelt wurden. Ein Patient entwickelte eine Nierenschädigung im Zusammenhang mit einer Virusreaktivierung und einem Schub der Grunderkrankung, was strengere Regeln zur Kontrolle der Krankheitsaktivität vor der Infusion nach sich zog.
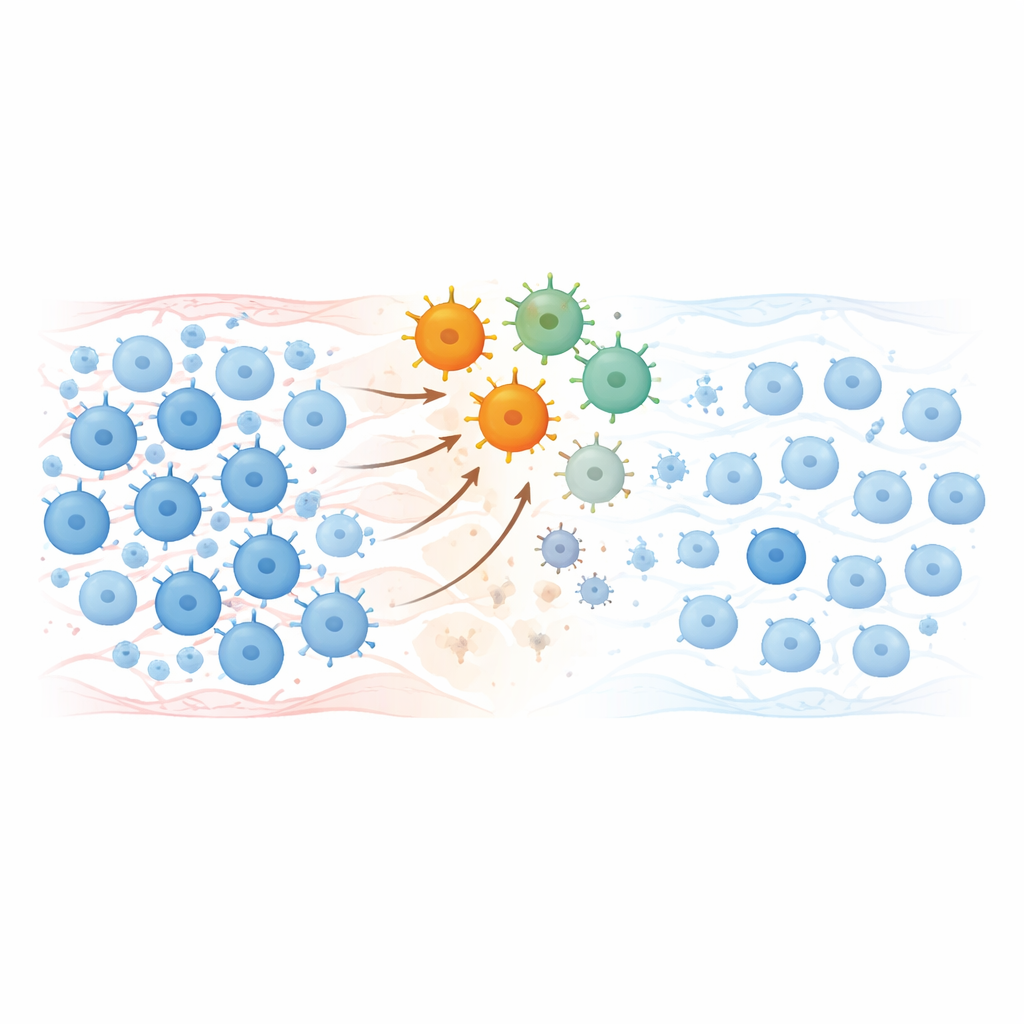
Das Immunsystem zurücksetzen
Obwohl die Sicherheit oberste Priorität hatte, waren die klinischen Verbesserungen auffällig. Nach sechs Monaten erfüllten 22 von 24 Patienten vordefinierte Erfolgskriterien, die an ihre jeweilige Erkrankung angepasst waren: die meisten Lupuspatienten erreichten eine strenge Remissionsdefinition, alle Patienten mit systemischer Sklerose zeigten keine Verschlechterung der Lungenbeteiligung und bessere Lungenfunktion sowie weichere Haut, und die meisten Patienten mit Muskelentzündung gewannen an Kraft und wiesen niedrigere Muskelenzymwerte auf. Wichtig ist, dass alle Teilnehmenden Steroide und andere Immunsuppressiva absetzen konnten und während der sechsmonatigen Studienzeit und darüber hinaus ohne Rückfälle blieben (medianes Follow-up etwa ein Jahr).
Was im Blut passiert
Labortests zeigten, dass sich die infundierten CAR‑T‑Zellen über einige Tage vermehrten, zirkulierende B‑Zellen eliminierten und dann innerhalb von ein paar Monaten allmählich verschwanden. Als B‑Zellen später zurückkehrten, zeigte ihre Zusammensetzung Veränderungen: naive, „frische“ Zellen dominierten, während Gedächtniszellen und antikörperproduzierende Vorläufer, die oft Autoimmunerinnerung tragen, stark reduziert waren. Viele schädliche Autoantikörper sanken auf sehr niedrige oder nicht nachweisbare Werte, während schützende Antikörper aus früheren Impfungen gegen Infektionen wie Masern oder Tetanus weitgehend erhalten blieben—was auf einen gezielten Reset statt eines vollständigen Löschens der Immunerinnerung hindeutet.
Ein Ausblick auf eine neue Behandlungsära
Für Menschen mit schweren Autoimmunerkrankungen schien die Vorstellung einer einmaligen Behandlung, die eine dauerhafte, medikamentenfreie Remission bringt, lange unerreichbar. Diese Studie legt nahe, dass gentechnisch veränderte T‑Zellen fehlgeleitete B‑Zellen bei drei unterschiedlichen Erkrankungen sicher zum Schweigen bringen können und das Immunsystem in einer ruhigeren, weniger selbstschädigenden Form wiederaufgebaut werden kann. CASTLE ist eine frühe, relativ kleine Studie; größere, entscheidende Studien sind nötig, um zu bestätigen, wie lange der Nutzen anhält und welche Patienten am meisten profitieren. Dennoch weist sie in Richtung einer Zukunft, in der das Zurücksetzen des Immunsystems—statt es endlos zu unterdrücken—ein realistisches Ziel werden könnte.
Zitation: Müller, F., Hagen, M., Wirsching, A. et al. CD19 CAR-T cells for treatment-refractory autoimmune diseases: the phase 1/2 CASTLE basket trial. Nat Med 32, 1142–1151 (2026). https://doi.org/10.1038/s41591-025-04185-6
Schlüsselwörter: CAR-T-Zelltherapie, Autoimmunerkrankung, systemischer Lupus erythematodes, systemische Sklerose, B-Zellen