Clear Sky Science · de
Humorale IgG1-Antworten auf Tumorantigene bestimmen klinische Ergebnisse bei Checkpoint-Inhibitoren
Warum das für Krebspatienten wichtig ist
Die Immuntherapie hat die Krebsbehandlung verändert, indem sie dem eigenen Immunsystem hilft, Tumore anzugreifen – dennoch profitieren nur einige Patientinnen und Patienten. Die meiste Aufmerksamkeit galt einer Gruppe von Immunzellen, den T-Zellen, doch diese Studie zeigt, dass eine andere Gruppe, die Antikörper produzierenden B-Zellen, den Unterschied zwischen Erfolg und Misserfolg ausmachen kann. Indem sie aufdeckt, wie eine bestimmte Antikörperantwort, genannt IgG1, mit besseren Ergebnissen einhergeht, weist die Arbeit auf neue Wege, vorherzusagen, wer von Immuntherapie profitiert, und darauf, wie sich diese Behandlungen für mehr Menschen wirksamer machen lassen.
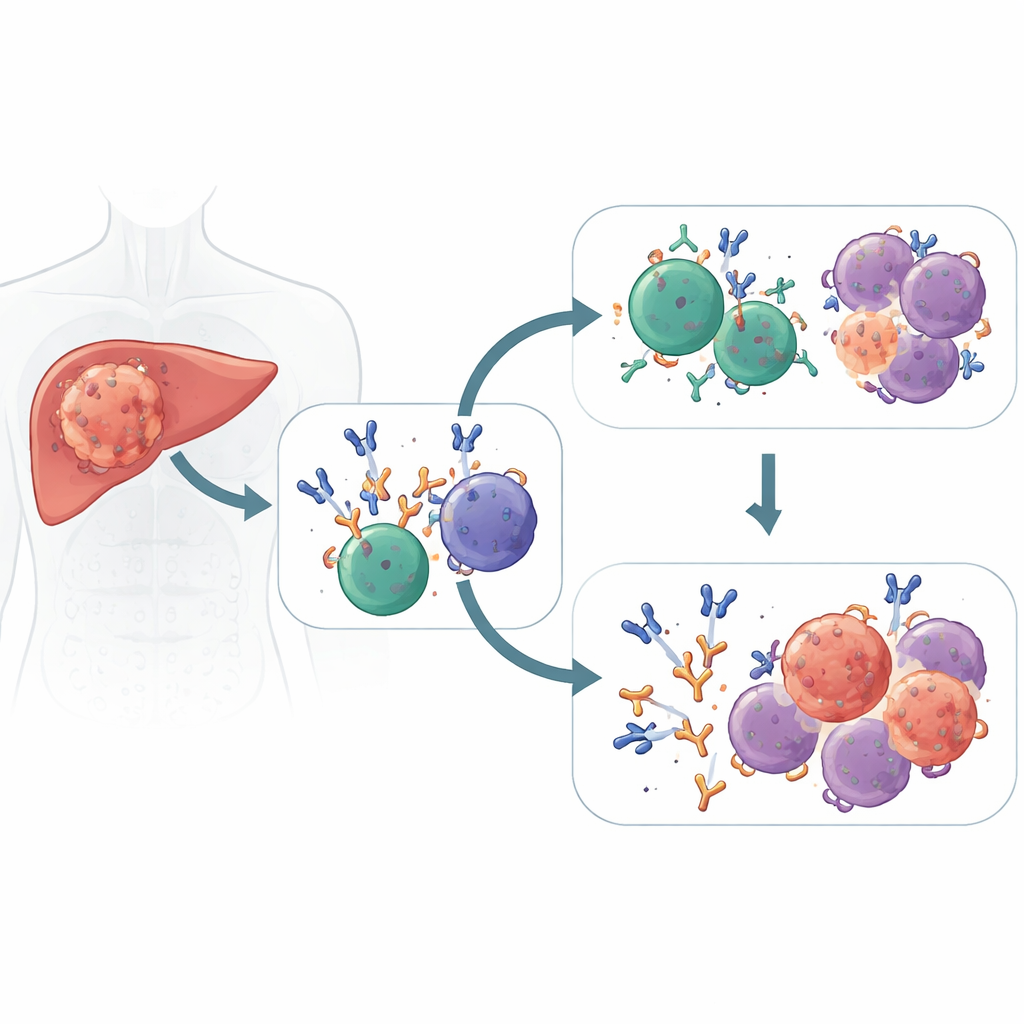
Zwei Verteidigungslinien, die zusammenwirken
Moderne Medikamente, sogenannte Checkpoint-Inhibitoren, lösen die „Bremsen“ an T-Zellen, damit diese Krebszellen erkennen und abtöten können. Die Forschenden untersuchten Menschen mit Leberkrebs, die diese Medikamente vor einer Operation erhielten, und entdeckten, dass gute Ansprechende sich nicht ausschließlich auf T‑Zellen verließen. Ihre Tumoren waren außerdem voller Plasmazellen – ausgereifte B‑Zellen, die wie kleine Antikörperfabriken wirken – welche eine dominante Welle von IgG1-Antikörpern gegen Tumorziele produzierten. Im Gegensatz dazu hatten Patientinnen und Patienten, deren Tumoren nicht schrumpften, mehr ruhende oder dysfunktionale B‑Zellen und weniger dieser spezialisierten Plasmazellen im Tumor.
Der Antikörperspur durch den Körper folgen
Um zu verstehen, woher diese hilfreichen Plasmazellen stammen, kombinierten die Forschenden Einzelzellsequenzierung mit detaillierter Verfolgung der einzigartigen Antikörper‑„Barcode“-Signaturen jeder B‑Zelle. Sie fanden, dass erfolgreiche Patientengruppen Familien eng verwandter IgG1-produzierender Zellen hatten, die sowohl im Tumor als auch in den umliegenden Lymphknoten – den Kommandozentralen des Immunsystems – expandierten. Dieselben klonalen Signaturen tauchten bereits vor der Behandlung auf und vergrößerten sich nach der Therapie, was darauf hindeutet, dass die Checkpoint-Blockade bestehende, tumorbewusste B‑Zellklone verstärkt, statt völlig neue zu erzeugen. Das legt eine koordinierte Zirkulation trainierter Antikörperproduzenten zwischen Lymphknoten und Tumorstandorten nahe.
Wie Antikörper das Tumormikroumfeld umgestalten
Mikroskopische Bildgebung und räumliche Genkartierung zeigten, dass Plasmazellen bei Ansprechenden nicht nur am Tumorrand saßen – sie drangen tief in den Tumor ein, zusammen mit Killer‑T‑Zellen und hilfreichen Makrophagen. Diese Regionen waren reich an Signalen, die die B‑Zellaktivierung und Antikörperproduktion fördern und so immunologische „Nachbarschaften“ bilden, die für einen Angriff optimiert sind. Nicht-Ansprechende sammelten dagegen eher gedächtnisähnliche B‑Zellen und regulatorische Immunzellen in faserigen Stroma‑Nischen an, die effektive Antworten dämpften. In mehreren unabhängigen Patientengruppen und bei verschiedenen Immuntherapie‑Kombinationen markierte eine Verschiebung hin zu IgG1-produzierenden Plasmazellen konsistent eine bessere Tumorkontrolle und ein langsameres Fortschreiten der Erkrankung.
Antikörper, die krebspezifische Markierungen erkennen
Da Plasmazellen Antikörper ins Blut abgeben, fragten die Forschenden, ob sich diese Moleküle in Blutproben nachweisen lassen. Bei vielen Ansprechenden fanden sie hohe Spiegel von IgG1-Antikörpern, die so genannte Cancer/Testis-Antigene anvisieren – Proteine wie NY-ESO-1, die in normalen Geweben meist fehlen, in Tumoren aber wieder auftreten. Patientinnen und Patienten mit diesen Antikörpern zeigten eher auch starke T‑Zellreaktionen gegen dieselben Ziele, was nahelegt, dass Antikörper dabei helfen, Tumorfragmente dem zellulären Immunsystem zu präsentieren. Große Überlebensdaten aus Melanom- und Lungenkrebs‑Kohorten bestätigten, dass Tumoren mit starken IgG1‑Signaturen tendenziell besser auf Checkpoint‑Medikamente ansprechen, während Krebserkrankungen, die hauptsächlich mit Standardchemotherapie behandelt werden, keinen solchen Zusammenhang zeigten.
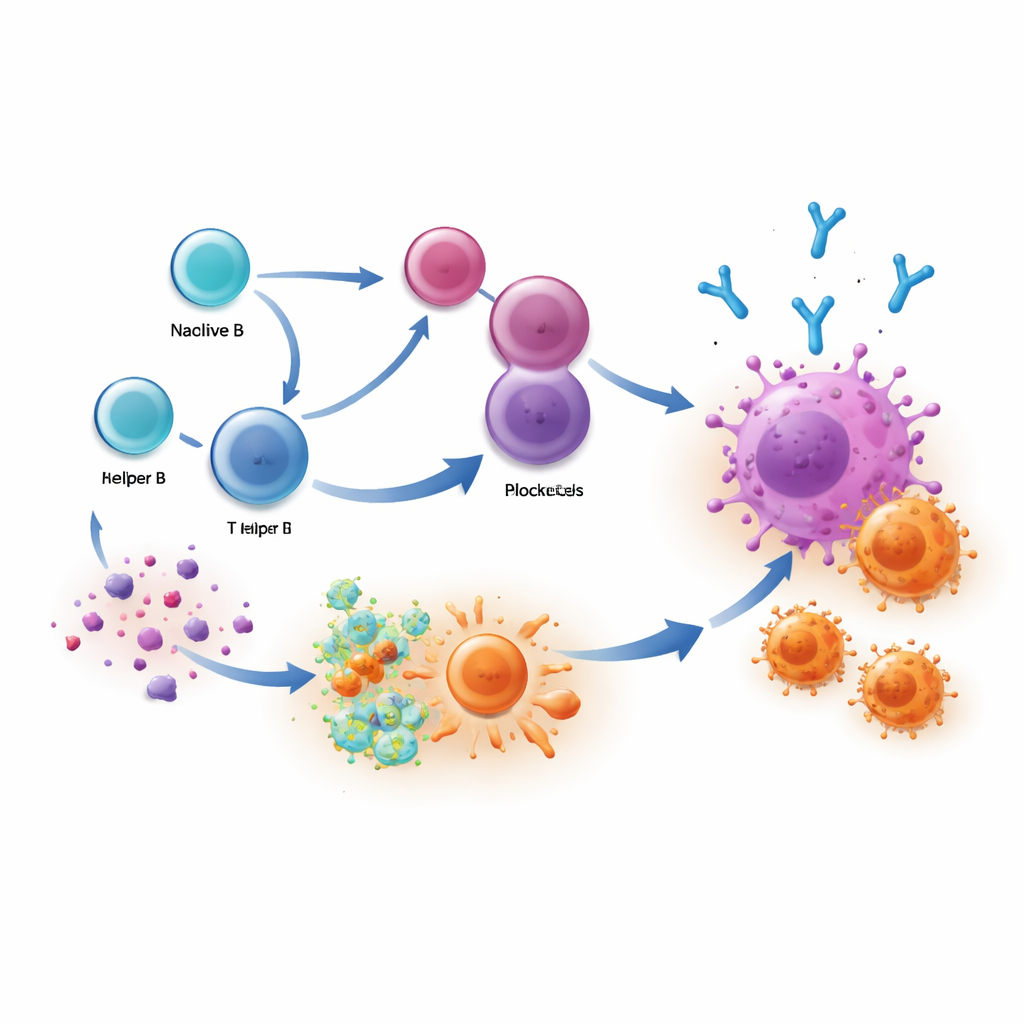
Was das für künftige Behandlungen bedeutet
Kurz gesagt: Am erfolgreichsten sind Patientinnen und Patienten, wenn ihr Immunsystem einen zweigleisigen Angriff fährt: IgG1‑Antikörper aus Plasmazellen markieren Krebszellen, und T‑Zellen rücken zur Zerstörung nach. Die Studie zeigt, dass Checkpoint‑Therapien diese Antikörperantworten verstärken können, besonders wenn hilfreiche B‑Zellklone bereits vor der Behandlung vorhanden sind. Das Messen von IgG1‑reichen Plasmazellen oder ihrer Antikörper in Blut‑ und Tumorproben könnte Ärztinnen und Ärzten helfen, wahrscheinliche Ansprechende zu identifizieren und den Therapieerfolg zu überwachen. Langfristig könnten Impfstoffe oder Medikamente, die B‑Zellen in Richtung der Produktion präziser, tumorgezielter IgG1‑Antikörper lenken, den Nutzen der Immuntherapie verstärken und dauerhaftere Ansprechreaktionen für mehr Menschen mit Krebs ermöglichen.
Zitation: Gonzalez-Kozlova, E., Sweeney, R., Figueiredo, I. et al. Humoral IgG1 responses to tumor antigens underpin clinical outcomes in immune checkpoint blockade. Nat Med 32, 978–991 (2026). https://doi.org/10.1038/s41591-025-04177-6
Schlüsselwörter: Krebsimmuntherapie, B-Zellen, IgG1-Antikörper, Immune-Checkpoint-Blockade, Leberzellkarzinom