Clear Sky Science · de
Multimodaler antigener Fluchtmechanismus gegenüber GPRC5D‑gerichteten T‑Zell‑Engagern beim multiplen Myelom
Wenn Krebs die präzise Immuntherapie überlistet
Neue, potente immunbasierte Medikamente verändern die Behandlung des multiplen Myeloms, einer Blutkrebserkrankung, die für die meisten Patientinnen und Patienten weiterhin nicht heilbar ist. Diese Therapien lenken die körpereigenen T‑Zellen so um, dass sie Tumorzellen erkennen und zerstören, die durch spezifische „Fahnen“ an ihrer Oberfläche markiert sind. Ein vielversprechendes Zielmolekül ist GPRC5D. Doch wie bei vielen zielgerichteten Therapien können Tumoren sich verändern und der Behandlung entkommen. Diese Studie legt auf ungewöhnlich detaillierte Weise dar, wie Myelomzellen die GPRC5D‑Fahne verändern oder verbergen, um hochwirksamen, T‑Zell‑aktivierenden Wirkstoffen zu entgehen.
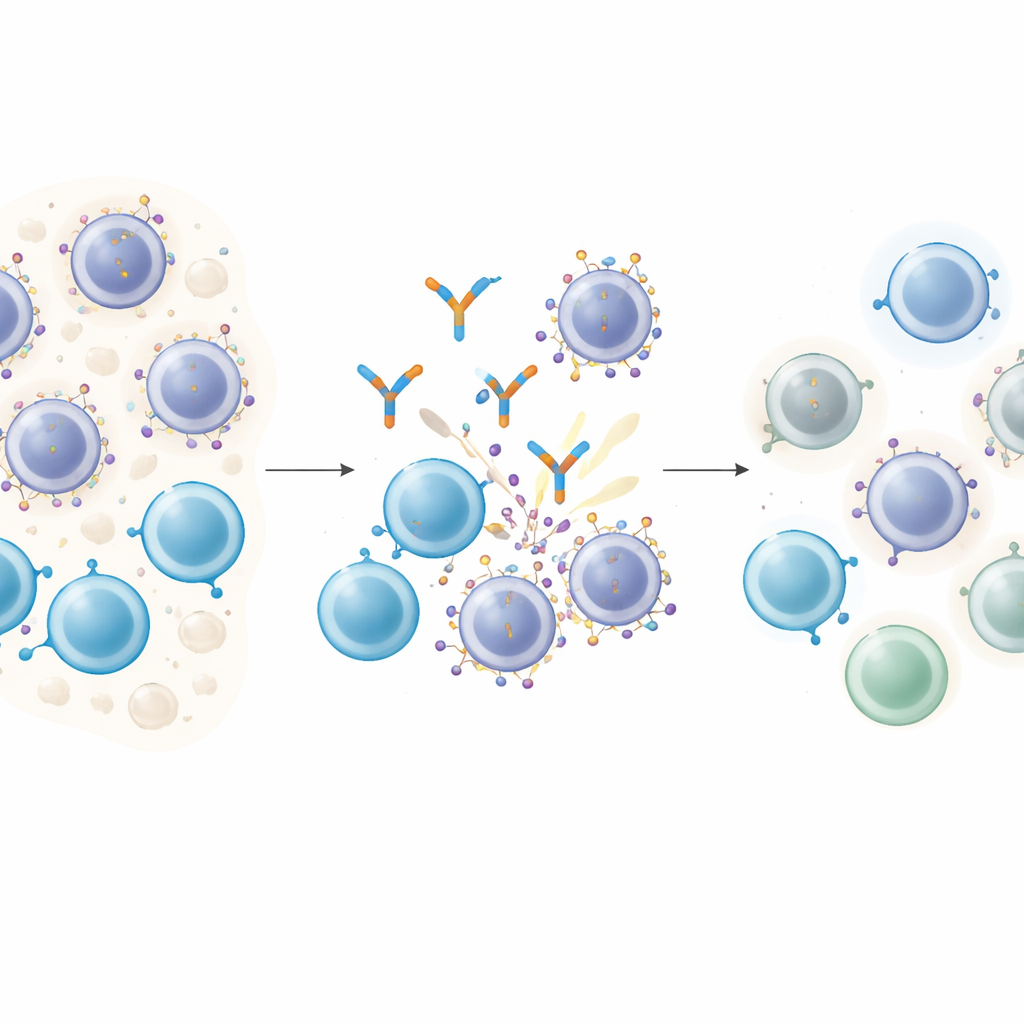
Wie clevere Wirkstoffe an Krebszellen andocken
T‑Zell‑engagierende Antikörper wirken wie molekulare Kuppler: Ein Ende greift eine T‑Zelle, das andere bindet an ein Zielmolekül auf der Krebszelle und bringt beide Zellen in direkten Kontakt, sodass die T‑Zelle die Tumorzelle abtöten kann. Beim multiplen Myelom ist GPRC5D ein attraktives Ziel, weil es auf malignen Plasmazellen reichlich vorhanden, auf den meisten normalen Geweben jedoch selten ist. Patientinnen und Patienten, die mit einem GPRC5D‑gerichteten Wirkstoff namens Talquetamab behandelt werden, erreichen häufig tiefe Remissionen. Fast alle erleiden jedoch schließlich einen Rückfall, weshalb eine entscheidende Frage lautet: Verändern die Krebszellen das Zielmolekül, auf das diese Medikamente angewiesen sind?
Tumorevolution in Echtzeit verfolgen
Die Forschenden begleiteten 21 Menschen mit schwer behandelbarem Myelom, die Talquetamab erhielten. Sie entnahmen Knochenmarkproben vor der Behandlung bei einigen Patientinnen und Patienten und erneut bei Rückfall und untersuchten die Tumorzellen mit multiplen Ebenen der DNA‑, RNA‑ und Chromatinanalyse. Dieser ultra‑detaillierte Blick zeigte, dass sich bei etwa zwei Dritteln der Patienten mit Rückfall GPRC5D auf Arten verändert hatte, die die Wirkung des Medikaments abschwächen oder blockieren würden. Bemerkenswert war, dass oft mehrere unterschiedliche resistente Subklone — genetisch verschiedene Zweige des Tumors — beim selben Menschen koexistierten, was zeigt, dass die Evolution in Richtung Flucht gleichzeitig mehrere Wege beschreiten kann.
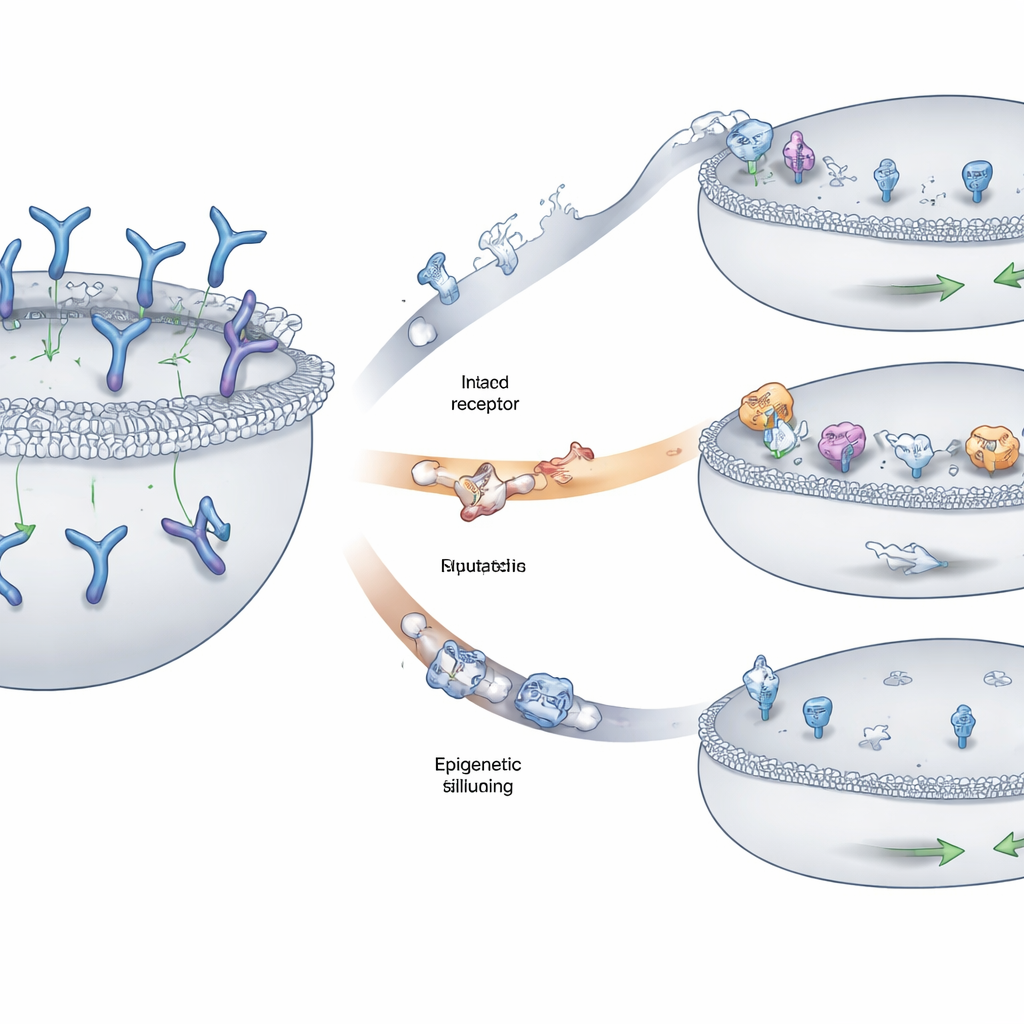
Drei Hauptwege, wie Tumore das Ziel verbergen
Das Team identifizierte drei wiederkehrende Muster, mit denen Myelomzellen der Erkennung entgingen. Bei manchen Patientinnen und Patienten wurden Stücke des Chromosoms, das das GPRC5D‑Gen trägt, auf beiden Kopien deletiert, wodurch die Fahne vollständig von der Zelloberfläche verschwand. Bei anderen führten kleinere Veränderungen — einzelne Basentauschmutationen oder winzige Insertionen und Deletionen — zu Verzerrungen wichtiger Regionen des GPRC5D‑Proteins. Viele dieser Veränderungen störten Bereiche des Proteins, die für den korrekten Transport von innen zur äußeren Membran nötig sind, sodass GPRC5D in einem intrazellulären Kompartiment stecken blieb, statt an der Oberfläche angezeigt zu werden. Ein dritter Mechanismus war epigenetische Stilllegung: Die DNA rund um GPRC5D wurde eng gepackt und chemisch markiert, sodass das Gen kaum abgelesen wurde, obwohl die zugrunde liegende Sequenz weitgehend intakt war. Tumorzellen, die diese Strategie nutzten, produzierten wenig oder gar kein GPRC5D.
Wenn die Fahne vorhanden ist, der Schlüssel aber nicht mehr passt
Nicht alle Fluchtwege entfernten GPRC5D von der Zelloberfläche. In einigen Fällen sah das Protein in Standardtests normal aus, passte dem Medikament aber nicht mehr wie ein Schlüssel ins Schloss. Das Team rekonstruierte spezifische, von Patientinnen und Patienten stammende Mutationen in Laborzelllinien und prüfte, wie gut verschiedene GPRC5D‑gerichtete Antikörper an diese Zellen binden und sie töten konnten. Eine Mutation veränderte subtil genau die Stelle, an der Talquetamab den Rezeptor greift, was die Bindungs- und Abtötungsfähigkeit des Medikaments deutlich verringerte, obwohl der Rezeptor bei Routinefärbungen weiterhin sichtbar war. Interessanterweise blieben andere GPRC5D‑gerichtete Wirkstoffe, die den Rezeptor an zwei Stellen gleichzeitig halten, gegen mehrere dieser Mutanten wirksam, was verdeutlicht, wie das Wirkstoffdesign — etwa multivalente oder multi‑epitopale Bindung — beeinflussen kann, ob resistente Klone überleben.
Jenseits des Ziels: Weitere Grenzen der Immunattacke
Während bei den meisten Rückfällen eine Form des GPRC5D‑Verlusts oder einer Veränderung vorlag, erlitten eine Minderheit der Patientinnen und Patienten einen Rückfall ohne offensichtliche Veränderungen des Zielmoleküls. In diesen Fällen lag das Problem offenbar bei den T‑Zellen: Sie waren weniger leistungsfähig und in Labortests weniger fähig, Krebszellen zu töten, was darauf hindeutet, dass langfristige, kontinuierliche Exposition gegenüber Engager‑Therapien das Immunsystem erschöpfen kann. Die Studie zeigte außerdem, dass ein bestimmter genetischer Subtyp des Myeloms (mit einem Chromosomenumschwung namens t(11;14)) das GPRC5D‑Gen natürlicherweise in einem stärker „geschlossenen“ Chromatinzustand hält und damit eine niedrigere Basalexpression aufweist. Das legt nahe, dass einige Patientinnen und Patienten von vornherein zu schlechteren Antworten predisponiert sein könnten, weil ihre Tumoren mit abgeschwächten Zielpegeln beginnen.
Was das für Patientinnen, Patienten und künftige Therapien bedeutet
Für Patientinnen, Patienten und Behandelnde erklärt diese Arbeit, warum selbst sehr potente, auf GPRC5D zielende Therapien noch keine Heilung darstellen: Myelomzellen können die Fahne, auf die diese Medikamente angewiesen sind, löschen, umschichten, fehlleiten oder ausschalten — und sie tun dies oft auf mehreren Wegen gleichzeitig. Die Ergebnisse deuten darauf hin, dass die Überwachung der Tumor‑DNA, statt nur der Proteinniveaus, wichtig sein wird, um aufkommende Fluchtmutationen zu erkennen, die Standardlabortests übersehen können. Sie weisen auch auf Strategien der nächsten Generation hin — etwa Wirkstoffe, die GPRC5D an mehreren Stellen stärker binden, Kombinationen, die mehr als ein Ziel gleichzeitig angreifen, oder Agenzien, die stillgelegte Gene wieder öffnen — um der Tumorevolution vorauszubleiben. Im Kern kartiert diese Studie die Fluchtrouten des Myeloms, damit künftige Therapien so entworfen werden können, dass sie diese blockieren und T‑Zell‑basierte Behandlungen länger wirksam halten.
Zitation: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
Schlüsselwörter: multiples Myelom, T‑Zell‑Engager, GPRC5D, Antigenflucht, Krebsimmuntherapie