Clear Sky Science · de
BCMA-gerichtete mRNA-CAR-T-Zelltherapie bei Myasthenia gravis: eine randomisierte, doppelblinde, placebokontrollierte Phase-2b-Studie
Warum diese Studie für den Alltag wichtig ist
Myasthenia gravis ist eine chronische Erkrankung, die einfache Tätigkeiten – wie Treppensteigen, Kauen oder das Offenhalten der Augenlider – unerwartet erschwert. Viele Betroffene benötigen über Jahre starke immunsuppressive Medikamente, die schwere Nebenwirkungen haben können. In dieser Studie wurde eine neue Art einmaliger Zelltherapie geprüft, die darauf abzielt, die Krankheit mit nur sechs wöchentlichen Infusionen für mindestens ein Jahr zu dämpfen und so möglicherweise den Bedarf an dauerhafter Medikation zu verringern.
Eine Erkrankung müder Muskeln
Bei Myasthenia gravis greift das Immunsystem fälschlich die «Verbindung» zwischen Nerven und Muskeln an. Antikörper, die von bestimmten Immunzellen gebildet werden, blockieren und schädigen die Andockstellen, über die Nervenimpulse normalerweise Muskelbewegungen auslösen. Mit der Zeit entwickeln Betroffene herabhängende Augenlider, verwaschene Sprache, Schluckstörungen sowie Schwäche in Armen, Beinen und Atemmuskulatur. Standardtherapien dämpfen das Immunsystem breit, was helfen kann, oft bleiben jedoch Beschwerden bestehen und das Risiko für Infektionen, Gewichtszunahme, Stimmungsschwankungen und andere medikamentenbedingte Probleme erhöht.
Eine neue Form personalisierter Zelltherapie
Die hier getestete Therapie, Descartes-08 genannt, verfolgt einen gezielteren Ansatz. Zunächst entnehmen Ärzte dem Patienten eigene T‑Zellen – Immunzellen, die auf bestimmte Ziele trainiert werden können – aus dem Blut. Im Labor werden diese Zellen vorübergehend mit genetischen Anweisungen in Form von mRNA ausgestattet, die sie befähigen, ein Protein namens BCMA auf der Oberfläche der antikörperproduzierenden Zellen zu erkennen, die die Erkrankung antreiben. Im Gegensatz zu herkömmlichen onkologischen Zelltherapien, die permanente virale Veränderungen verwenden und eine vorherige Chemotherapie erfordern, ist dieses Design kurzlebig und benötigt keine Vorbehandlung zur Eliminierung des Immunsystems. Patienten erhalten Descartes‑08 als sechs kurze wöchentliche Infusionen in einer Ambulanz. 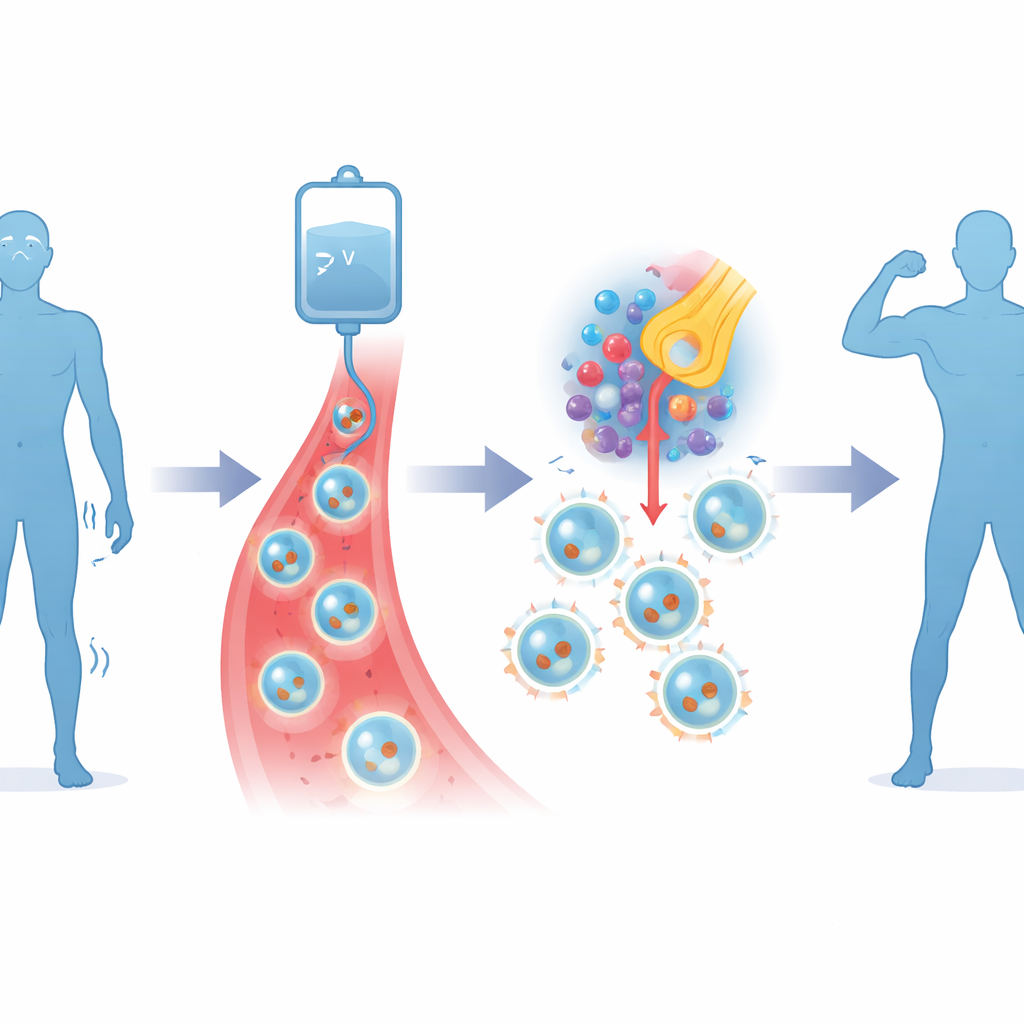
Die Idee auf faire Weise prüfen
Diese Phase‑2b‑Studie schloss erwachsene Patientinnen und Patienten mit generalisierter Myasthenia gravis ein, deren Erkrankung mehr als nur die Augenmuskeln betraf und die bereits Standardbehandlungen erhielten. Die Teilnehmenden wurden zufällig entweder mit Descartes‑08 oder einem äußerlich gleichen Placebo infundiert, und weder sie noch ihre behandelnden Ärzte wussten, welche Zuweisung vorlag. Maßgeblich war ein weithin verwendeter Score, der Patientenangaben zur Alltagsfunktion mit ärztlichen Krafttests kombiniert. Die Fragestellung lautete: Wie viele Personen zeigten drei Monate nach der Behandlung eine Verbesserung um mindestens fünf Punkte – mehr als das, was Expertinnen und Experten als klinisch bedeutsame Veränderung ansehen? Außerdem wurden Dauer der Verbesserungen, mögliche Reduktion der Kortisondosen und Nebenwirkungen über ein ganzes Jahr beobachtet.
Stärkere Muskeln, weniger Symptome
Unter den 26 in der Hauptanalyse berücksichtigten Teilnehmenden waren diejenigen, die Descartes‑08 erhielten, mehr als doppelt so häufig in der Lage, die angestrebte Verbesserung nach drei Monaten zu erreichen wie die Placebo‑Gruppe (etwa zwei Drittel gegenüber einem Viertel). Im Mittel zeigten behandelte Patientinnen und Patienten größere Abnahmen der Symptomschwere und bessere Kraftwerte als die Placebo‑Gruppe; diese Verbesserungen verstärkten sich meist in den ersten vier Monaten und waren noch nach einem Jahr nachweisbar. Etwa ein Drittel der Patientinnen und Patienten erreichte eine «minimale Symptomexpression», das heißt ihr Alltags-Symptomscore lag nahe null, und dies war noch häufiger – bei über der Hälfte – bei Personen, die zuvor nie neuere biologische Medikamente erhalten hatten. Viele mit Descartes‑08 behandelte Patientinnen und Patienten konnten zudem ihre Steroiddosis nach sechs Monaten etwa halbieren, während die Dosen in der Placebo‑Gruppe weitgehend unverändert blieben. 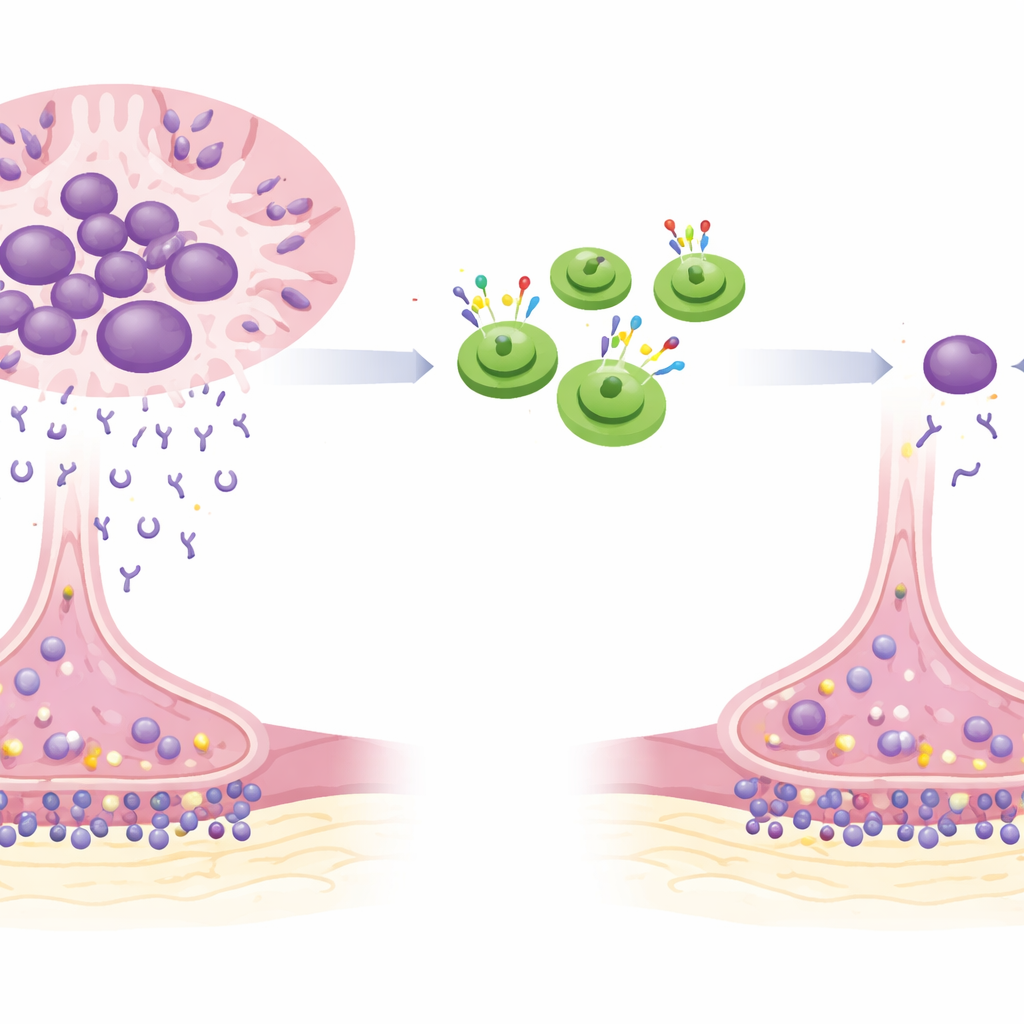
Sicherheit und Vorgänge im Immunsystem
Nebenwirkungen traten in beiden Gruppen häufig auf, waren aber überwiegend mild bis mäßig. Die häufigsten Probleme unter Descartes‑08 waren kurz andauernde Infusionsreaktionen – Fieber, Schüttelfrost, Kopfschmerzen und Muskelschmerzen – die sich meist innerhalb eines Tages ohne spezielle Behandlung zurückbildeten. Schwere Komplikationen wie lebensbedrohliche Immunreaktionen oder größere neurologische Nebenwirkungen, die bei manchen onkologischen Zelltherapien auftreten können, wurden nicht beobachtet. Wichtig ist, dass Bluttests zeigten, dass allgemeine Antikörperspiegel und schützende Impfantworten erhalten blieben, was darauf hindeutet, dass die Therapie vor allem krankheitsverursachende Zellen reduzierte, statt das Immunsystem breit zu beseitigen. Explorative Messungen deuteten darauf hin, dass bestimmte mit Autoimmunität verbundene Entzündungssignale nach der Behandlung zurückgingen, was mit einer präziseren «Neuausrichtung» der fehlgeleiteten Immunantwort vereinbar ist.
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit Myasthenia gravis deuten diese Ergebnisse darauf hin, dass ein kurzer Kurs personalisierter Zellinfusionen eine bedeutsame, langanhaltende Erleichterung bringen und gleichzeitig die tägliche Einnahme immunsuppressiver Medikamente reduzieren könnte. Die Studie war relativ klein, und einige Unterschiede über das primäre Ergebnis hinaus müssen in größeren Studien bestätigt werden, doch das konsistente Muster der Besserung und die insgesamt handhabbaren Nebenwirkungen sind ermutigend. Bestätigen zukünftige Studien diese Befunde, könnte die mRNA‑basierte Zelltherapie eine neue Option werden, die die Erkrankung präziser und bequemer kontrolliert und viele Patientinnen und Patienten näher an ein Leben mit minimalen Symptomen statt dauernder Erschöpfung und medizinischer Belastung bringt.
Zitation: Vu, T., Durmus, H., Rivner, M. et al. BCMA-directed mRNA CAR T cell therapy for myasthenia gravis: a randomized, double-blind, placebo-controlled phase 2b trial. Nat Med 32, 1131–1141 (2026). https://doi.org/10.1038/s41591-025-04171-y
Schlüsselwörter: Myasthenia gravis, Zelltherapie, CAR-T-Zellen, Autoimmunerkrankung, mRNA-Therapeutika