Clear Sky Science · de
Linavonkibart und Pembrolizumab bei gegen Immun-Checkpoint‑Blockade resistenten fortgeschrittenen soliden Tumoren: eine Phase‑1‑Studie
Warum hartnäckige Krebserkrankungen uns alle betreffen
Immuntherapeutika, die dem Immunsystem gewissermaßen die Bremsen lösen, haben die Behandlung vieler Krebsarten verändert. Dennoch profitieren die meisten Patienten entweder gar nicht oder erleben irgendwann erneut Tumorwachstum. Diese Studie prüft einen neuen Antikörperwirkstoff, Linavonkibart, der darauf ausgelegt ist, einen starken Schutzschild zu deaktivieren, den Tumoren nutzen, um sich vor Immunangriffen zu verstecken, und kombiniert ihn mit einem etablierten Immuntherapeutikum, Pembrolizumab. Die Ergebnisse liefern einen frühen Hinweis darauf, dass es möglicherweise möglich ist, die Immunantwort selbst bei Patienten, deren Tumoren bereits auf Checkpoint‑Inhibitoren nicht mehr reagierten, wiederherzustellen, während die Nebenwirkungen beherrschbar bleiben.
Ein verborgener Schutzschild um Tumoren
Viele moderne Immuntherapien wirken, indem sie sogenannte Checkpoint‑Moleküle wie PD‑1 blockieren, die normalerweise T‑Zellen bremsen. Wenn diese Bremsen gelöst werden, können Immunzellen Krebs aggressiver angreifen. Tumoren passen sich jedoch oft an, indem sie eine feindliche Umgebung schaffen, die cytotoxische T‑Zellen fernhält oder diese schwächt, wenn sie eindringen. Ein zentraler Baumeister dieser schützenden Blase ist das Signalmolekül TGFβ1, das sowohl von Krebszellen als auch von benachbarten Stütz‑ und Immunzellen gebildet wird. Frühere Versuche, die gesamte TGFβ‑Familie zu blockieren, zeigten zwar Wirksamkeit, führten aber zu schweren Herz‑ und Blutungsproblemen, weil andere Familienmitglieder für gesunde Gewebe wichtig sind. Linavonkibart wurde so entwickelt, dass es genau diesen Zielkonflikt umgeht: Es neutralisiert selektiv nur die latente, inaktive Form von TGFβ1, bevor sie aktiviert wird, und belässt eng verwandte Moleküle, die der Körper benötigt, ungestört.
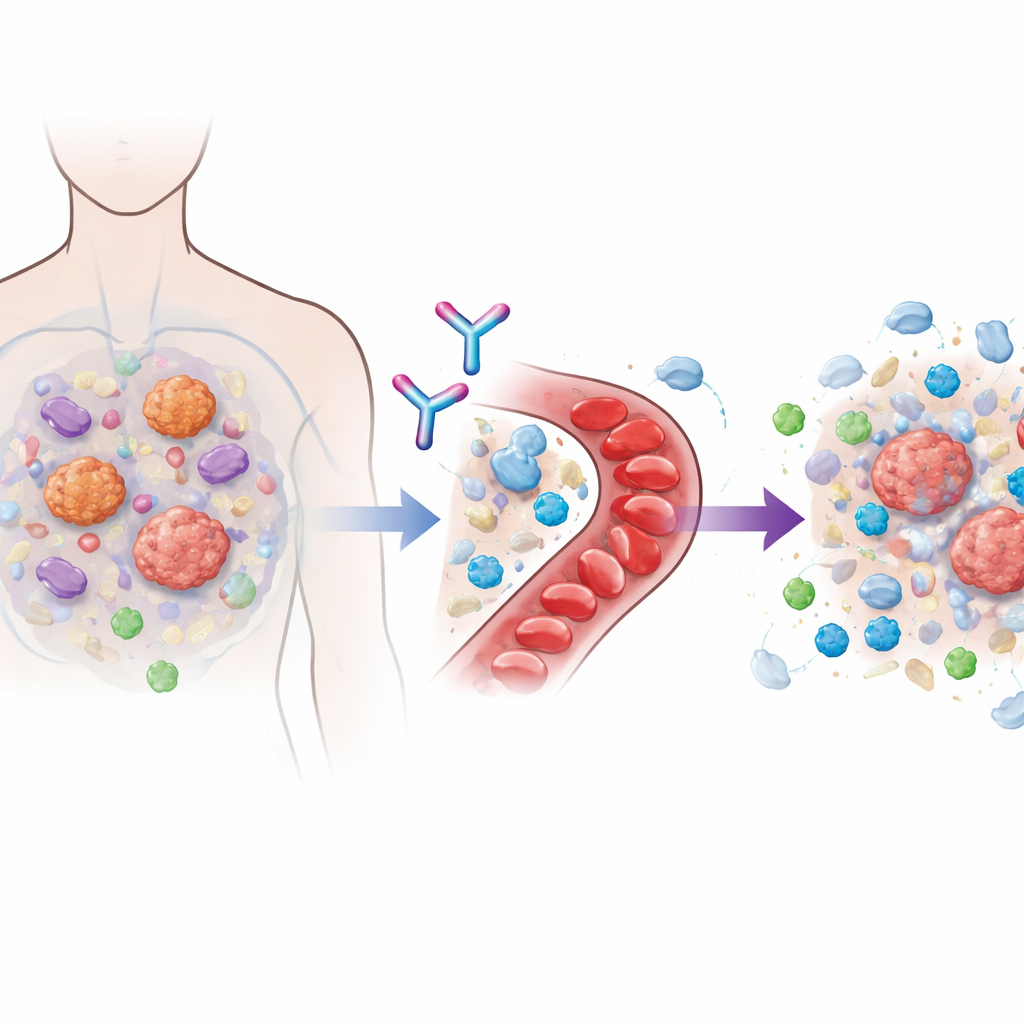
Konzipierung eines vorsichtigen Ersttests am Menschen
Die DRAGON‑Studie war eine multizentrische Phase‑1‑Studie, die an 22 Krankenhäusern in den USA und Südkorea durchgeführt wurde. Eingeschlossen wurden 112 Erwachsene mit fortgeschrittenen soliden Tumoren, die alle nur begrenzte Behandlungsmöglichkeiten hatten. Im ersten Teil der Studie erhielt eine kleine Gruppe von Patienten Linavonkibart allein in stufenweise ansteigenden Dosen oder in Kombination mit ihrer früheren PD‑1‑basierten Therapie. Dieser schrittweise Ansatz diente dazu, Sicherheit, Pharmakokinetik und Pharmakodynamik sowie eine geeignete Dosis für die weitere Prüfung zu ermitteln. Im zweiten Teil erhielten 78 Patienten, deren Tumoren bereits mindestens auf eine PD‑1‑Immuntherapie nicht angesprochen hatten, eine fixe Dosis Linavonkibart zusammen mit Pembrolizumab. Diese Patienten litten an schwer zu behandelnden Tumoren, darunter klarzelliges Nierenkrebs, Melanom, Kopf‑ und Hals‑Karzinome, urotheliale (Blasen‑)Krebsarten und Lungenkrebs, und die meisten hatten mehrere Vortherapien durchlaufen.
Sicherheit zuerst: was mit den Patienten geschah
Das Hauptziel dieser frühen Studie war die Sicherheit, und Linavonkibart zeigte in dieser Hinsicht ermutigende Ergebnisse. Über alle Dosisstufen hinweg wurde keine maximal tolerierte Dosis erreicht, und es traten keine dosislimitierenden oder tödlichen Nebenwirkungen in direkter Verbindung mit dem Wirkstoff auf. Als Linavonkibart in der Phase‑2‑Dosis mit Pembrolizumab kombiniert wurde, erlebten etwa drei Viertel der Patienten behandlungsbedingte Nebenwirkungen, was dem ähnelt, was oft bei Immuntherapien allein beobachtet wird. Hautausschläge und Juckreiz waren die häufigsten zusätzlichen Probleme, und eine kleine Zahl von Patienten entwickelte ernstere Haut‑ oder Lungenentzündungen. Wichtig ist, dass das gefährliche immunologische Überschießen, das sogenannte Zytokinfreisetzungssyndrom, wie es bei einigen Antikörpertherapien vorkommen kann, nicht beobachtet wurde, und das allgemeine Sicherheitsprofil weitgehend jenem von Pembrolizumab allein entsprach.
Hinweise darauf, dass das Immunsystem wiedererweckt werden kann
Obwohl dies keine große, endgültige Wirksamkeitsstudie war, deuteten mehrere Anzeichen darauf hin, dass die Blockade von TGFβ1 helfen könnte, die Reaktion auf PD‑1‑Blockade wiederzubeleben. In der Expansionsphase schrumpften messbare Tumoren unter der Kombination Linavonkibart–Pembrolizumab bei einem bemerkenswerten Anteil von Patienten, die zuvor nicht mehr auf PD‑1‑Medikamente angesprochen hatten. Bestätigte Ansprechraten lagen bei 20 % beim klarzelligen Nierenkrebs, 18,2 % beim Melanom und knapp über 9 % bei Kopf‑Hals‑ und urothelialen Tumoren; ein Nierenkrebspatient erreichte eine vollständige Rückbildung der sichtbaren Erkrankung. Viele dieser Anspreche hielten über Monate an, und Patienten, die reagierten, blieben in der Regel deutlich länger auf der Kombination als auf ihrer vorherigen PD‑1‑Therapie. Biopsien vor und nach der Behandlung lieferten eine biologische Erklärung: Tumoren zeigten eine stärkere Infiltration durch CD8‑„Killer“‑T‑Zellen, höhere Anteile aktivierter T‑Zellen, weniger immunsuppressive regulatorische T‑Zellen und myeloide Zellen sowie insgesamt eine Verschiebung hin zu einer entzündlicheren, angriffsbereiteren Mikroumgebung.
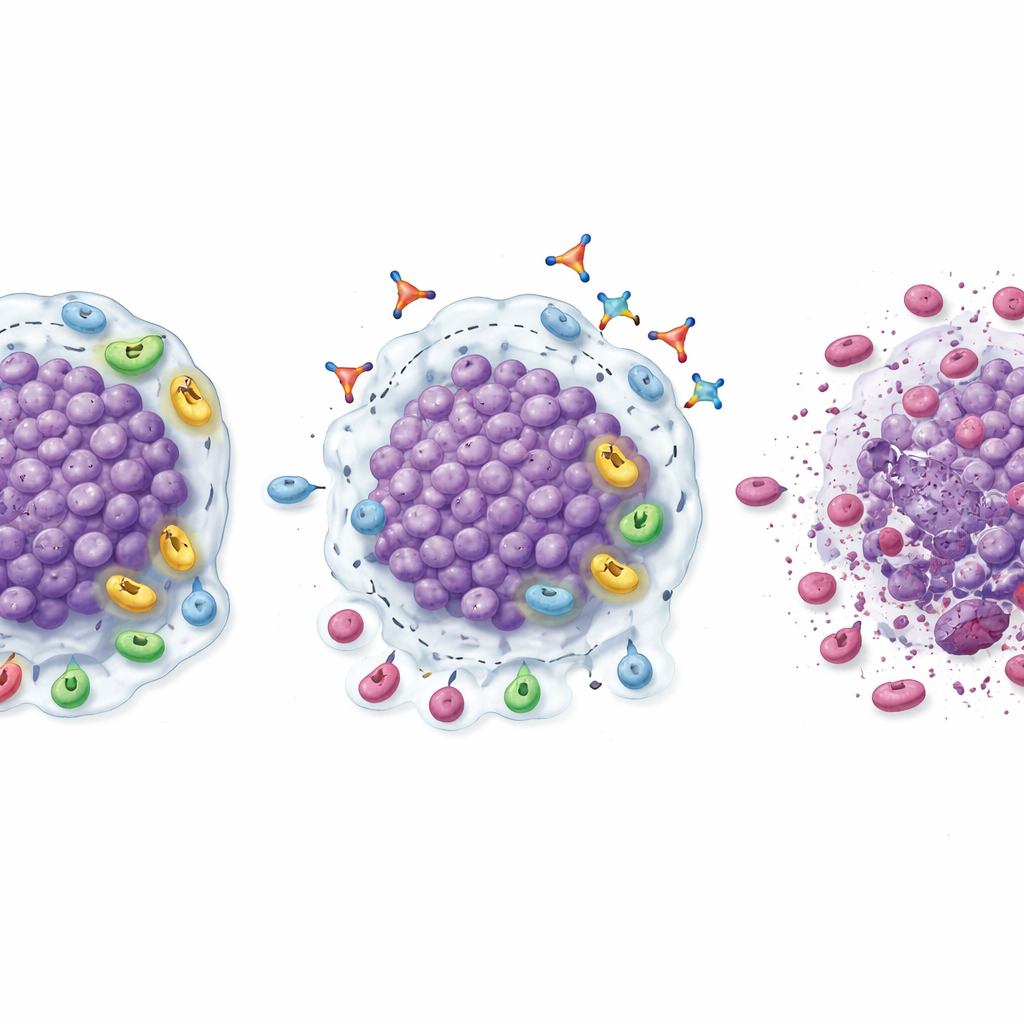
Ermitteln, wer am meisten profitieren könnte
Die Forschenden untersuchten auch, welche Patienten besonders wahrscheinlich ansprechen könnten. Beim klarzelligen Nierenkrebs sprachen Tumoren, die bereits vor Behandlungsbeginn viele CD8‑T‑Zellen enthielten — aber gleichzeitig reich an regulatorischen T‑Zellen waren und hohe TGFβ1‑Spiegel aufwiesen — eher auf die Kombinationstherapie an. In dieser Subgruppe waren Ansprechraten und progressionsfreies Überleben deutlich höher als in der gesamten Nierenkrebs‑Kohorte. Dieses Muster deutet auf einen „Sweet Spot“ hin: Tumoren, die viele Immunsoldaten aufweisen, aber durch TGFβ1‑vermittelte Unterdrückung in Schach gehalten werden, könnten ideale Kandidaten für Linavonkibart plus PD‑1‑Blockade sein. Wenn sich diese Befunde in größeren Studien bestätigen, könnten einfache Gewebetests auf diese Marker Ärzten helfen, Patienten auszuwählen, die am ehesten profitieren.
Was diese Arbeit für die Zukunft bedeutet
Für Menschen mit fortgeschrittenen Krebserkrankungen, die bereits auf Immuntherapie resistent geworden sind, ist die Aussicht, das eigene Immunsystem wieder zu beleben, ohne erhebliche Zusatztoxizität zu verursachen, sehr reizvoll. Diese Erst‑am‑Menschen‑Studie liefert frühe Hinweise, dass die selektive Deaktivierung des TGFβ1‑Schutzschilds mit Linavonkibart sicher möglich ist und in Kombination mit einem PD‑1‑Inhibitor sinnvolle Tumorkontrolle wiederherstellen kann, insbesondere bei bestimmten Nierenkrebsarten. Obwohl die Studie klein und nicht randomisiert war, stützen das Sicherheitsprofil, die biologischen Messwerte und die anhaltenden Anspreche zusammen stark die Durchführung größerer Phase‑2‑Studien. Bestätigen zukünftige Untersuchungen diese Ergebnisse, könnte dieser Ansatz den Kreis der Patienten erweitern, die von Immuntherapien profitieren, und einige derzeit hartnäckige Tumoren wieder verwundbar für die körpereigenen Abwehrkräfte machen.
Zitation: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
Schlüsselwörter: Krebsimmuntherapie, TGFβ1‑Hemmung, Resistenz gegen Immun-Checkpoints, klarzelliges Nierenzellkarzinom, Tumormikroumgebung