Clear Sky Science · de
Angeborene antivirale und immunologische Funktionen, die mit dem Rückgang des HIV-Reservoirs nach Anti-PD-1-Therapie assoziiert sind
Warum diese Forschung wichtig ist
Moderne HIV-Medikamente können das Virus über Jahrzehnte unter Kontrolle halten, aber sie können es nicht vollständig auslöschen. Eine kleine „Reservoir“-Population infizierter Zellen ruht im Körper und kann die Infektion neu entfachen, wenn die Behandlung abgesetzt wird. Diese Studie untersucht, ob eine Art Krebsimmuntherapie, die die „Bremsen“ des Immunsystems löst, auch dazu beitragen kann, dieses versteckte HIV-Reservoir zu verkleinern, und zeigt biologische Hinweise darauf, wer am meisten davon profitieren könnte.
Verstecktes Virus und ein neues Medikament
Menschen mit HIV nehmen heute häufig antiretrovirale Therapie (ART), die das Virus im Blut auf nicht nachweisbare Werte reduziert. Dennoch verbleibt das Virus in einer winzigen Population von Immunzellen, überwiegend Gedächtnis-CD4-T-Zellen, wo es still liegt und für Medikamente unerreichbar ist. Viele dieser Zellen zeigen ein Oberflächenprotein namens PD-1, das Teil eines Bremssystems ist, das normalerweise verhindert, dass das Immunsystem überreagiert. Krebsmedikamente, die PD-1 blockieren, haben die Behandlung mehrerer Tumoren revolutioniert, weil sie Immunzellen wieder aktivieren. Da PD-1 auch auf HIV-tragenden Zellen und auf erschöpften virusbekämpfenden Zellen vorkommt, haben Forschende vermutet, dass dieselben Medikamente helfen könnten, den Griff von HIV zu lockern.
Eine Studie bei Menschen mit HIV und Krebs
In dieser Studie erhielten 30 Erwachsene mit HIV und verschiedenen Krebserkrankungen alle drei Wochen den PD-1-blockierenden Antikörper Pembrolizumab zusätzlich zu ihrer üblichen ART. Die Behandlung war allgemein sicher, und einige Teilnehmende zeigten teilweise oder vollständige Tumoransprechen. Die Forschenden sammelten Blut vor der Behandlung, 24 Stunden danach, eine Woche später und am Ende der Therapie, die sich über viele Monate erstrecken konnte. Sie maßen HIV-DNA in Immunzellen als Marker des latenten Reservoirs, HIV-RNA als Zeichen viraler Aktivität sowie ein umfangreiches Set immunologischer Signale mittels RNA-Sequenzierung, Proteinmessungen und Einzelzellanalysen. 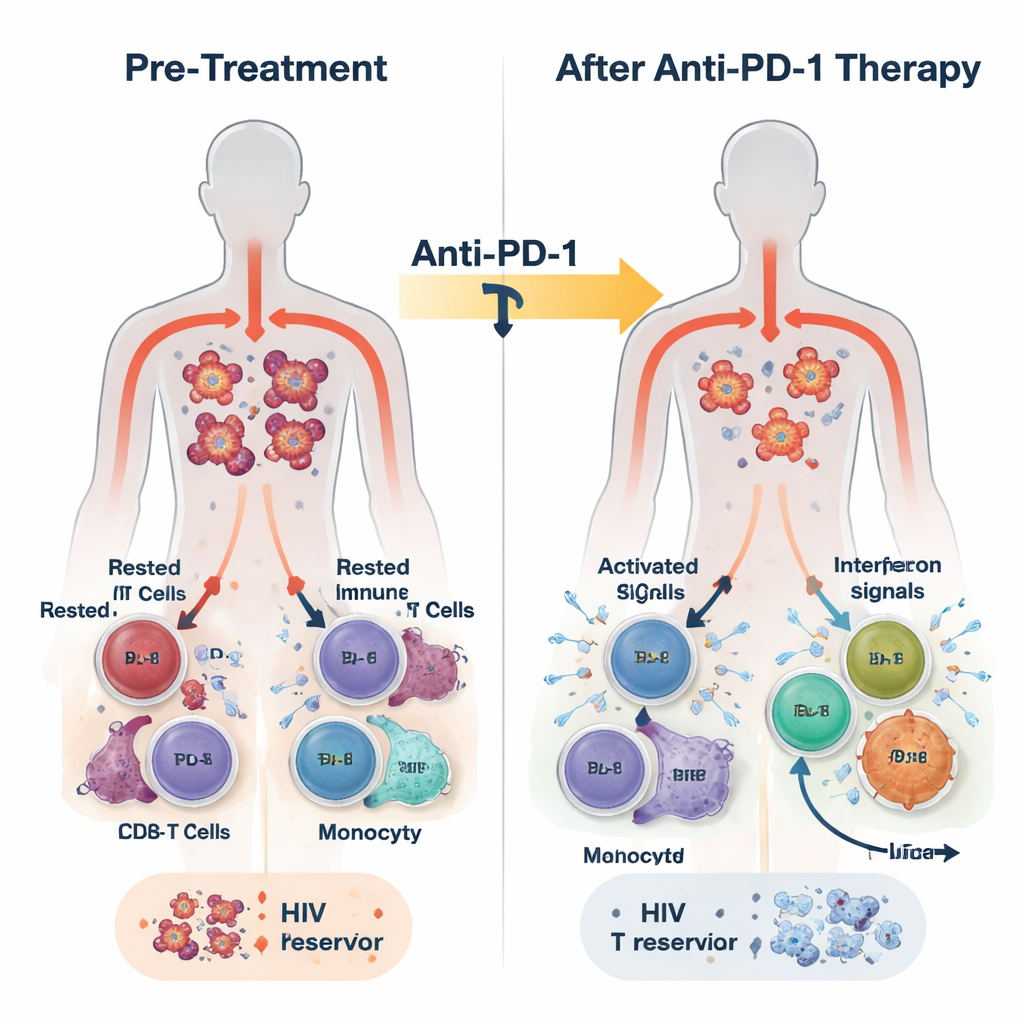
Ein früher antiviraler „Alarm“ bei einigen Teilnehmenden
Bereits 24 Stunden nach der ersten Dosis zeigte das Blut der meisten Teilnehmenden eine Welle angeborener Immunaktivität. Die Werte entzündlicher Botenstoffe wie Interferone (die klassischen antiviralen Alarmmoleküle des Körpers) und IL-6 stiegen, während ein suppressives Molekül namens TGF‑beta sank. Gleichzeitig wurden Genprogramme aktiviert, die mit antiviraler Abwehr, Monozytenaktivität und der Effektorfunktion von CD8-T-Zellen verbunden sind, quer durch die weißen Blutzellen. Eine genauere Analyse zeigte, dass diese Reaktion nicht einheitlich war. Am Ende der Behandlung ließen sich die Teilnehmenden anhand der Stärke und Persistenz der interferon-stimulierten Genaktivität (ISG) in zwei Gruppen einteilen: eine ISG-hoch-Gruppe, die diese antiviralen Programme aufrechterhielt, und eine ISG-niedrig-Gruppe, in der sie verblassten.
Verknüpfung von Immunmustern mit dem Schrumpfen des HIV-Reservoirs
Die ISG-hoch-Teilnehmenden begannen mit geringeren Mengen an HIV-DNA in ihren CD4-T-Zellen als die ISG-niedrig-Gruppe und erfuhren im Verlauf einen weiteren, etwa zweifachen Rückgang dieses latenten Reservoirs. Sie zeigten zudem tendenziell weniger CD4-T-Zellen, die im Laborversuch HIV wieder aktivieren konnten, am Ende der Therapie. Im Gegensatz dazu zeigten Personen der ISG-niedrig-Gruppe wenig bis keine Veränderung der HIV-DNA und hatten oft mehr Zellen, die zur Produktion von HIV-RNA induziert werden konnten. Hochauflösende Einzelzellanalyen lieferten ein mechanistisches Bild: Eine Untergruppe von Monozyten erhöhte rasch die Expression antiviraler Gene; HIV-spezifische CD8-T-Zellen expandierten und wurden proliferativer; und bestimmte CD4-T-Zell-Untergruppen regelten antivirale Abwehrmechanismen hoch, während andere, die mit anhaltender viraler Transkription assoziiert sind, abnahmen. Experimente in Zellen gesunder Spender bestätigten, dass die Stimulierung angeborener Sensoren oder von Interferonwegen sowohl antivirale Proteine in CD4-T-Zellen steigern als auch deren Anfälligkeit für HIV-Infektion verringern kann. 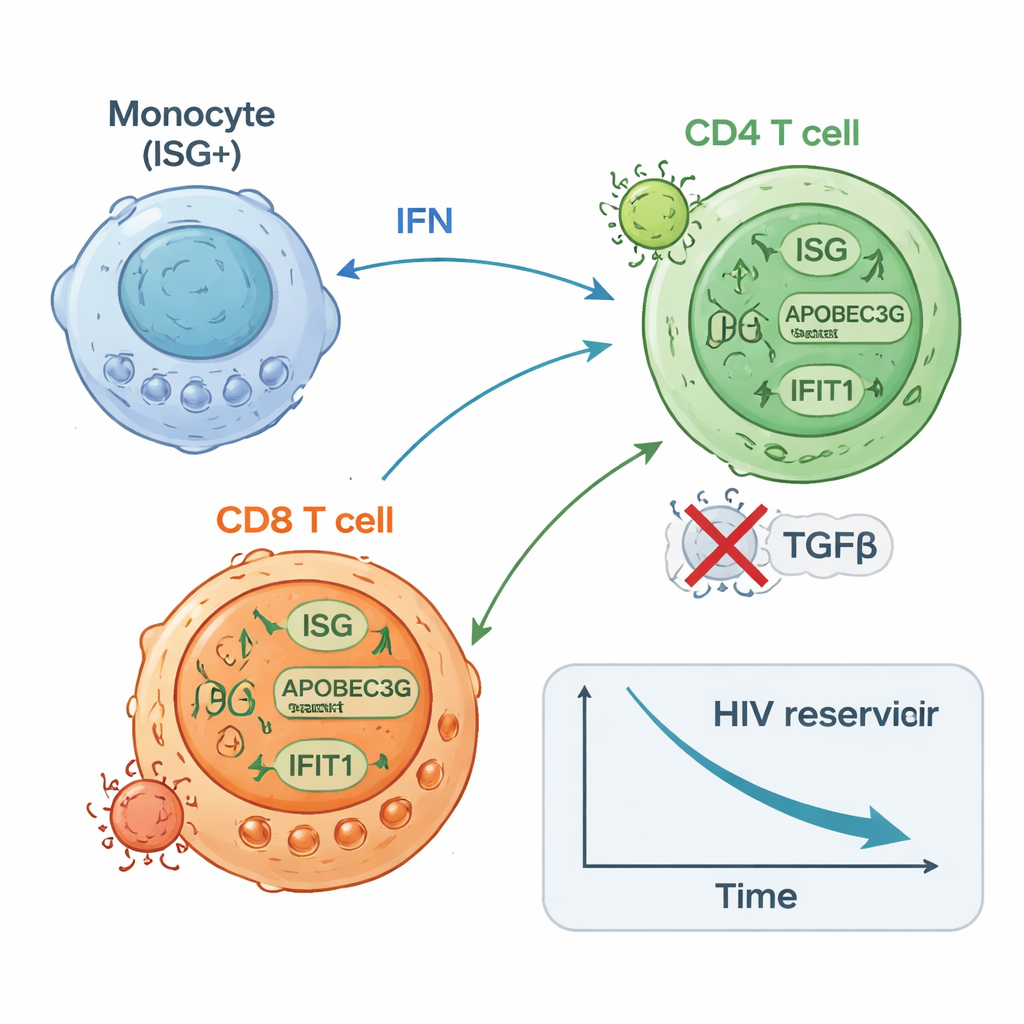
Hinweise zur Auswahl und Verbesserung zukünftiger Therapien
Interessanterweise treten die gleichen antiviralen Genmuster, die in der ISG-hoch-Gruppe gesehen wurden, auch im Blut mancher Menschen mit anderen Krebsarten oder Infektionen auf, was darauf hindeutet, dass ein natürlich „vorbereitzustand“ des Immunsystems bei einer Teilpopulation existieren könnte. In dieser Studie war dieser vorbereitete Zustand — definiert durch starke Interferonprogramme in myeloiden Zellen und T-Zellen und niedrige Aktivität regulatorischer Wege wie WNT-Signalgebung und TGF‑beta — sowohl mit einer sichereren Kontrolle des HIV-Reservoirs als auch mit Merkmalen verknüpft, die in anderen Studien mit besseren Krebsverläufen assoziiert sind. Die Autorinnen und Autoren schlagen vor, PD-1-Blockade mit zeitlich abgestimmten Verstärkungen der Interferonwege oder mit Medikamenten, die TGF‑beta blockieren, zu kombinieren, um die Reduktion des HIV-Reservoirs weiter zu verstärken, ohne die Krebsbekämpfung zu gefährden.
Was das für Menschen mit HIV bedeutet
Diese Arbeit bietet noch keine Heilung, und PD-1-blockierende Medikamente bleiben potente Therapien, die am besten ernsthaften Erkrankungen wie Krebs vorbehalten sind. Sie liefert jedoch den wichtigen Nachweis, dass das kurzzeitige Lösen immunologischer Bremsen eine schnelle, koordinierte antivirale Reaktion auslösen kann, die bei einigen Personen auf ART messbar den Pool HIV-infizierter Zellen verkleinert. Ebenso wichtig ist, dass sie eine Reihe blutbasierter Immunsignaturen beschreibt, die Ärztinnen und Ärzten erlauben könnten, diejenigen zu identifizieren, die am ehesten von solchen Ansätzen profitieren, und Kombinationsstrategien zu entwerfen, die das Immunsystem dazu bringen, mehr von HIVs letzten Verstecken aufzudecken und zu beseitigen.
Zitation: Talla, A., Azevedo, J.L.L.C., Latif, M.B. et al. Innate antiviral and immune functions associated with the HIV reservoir decay after anti-PD-1 therapy. Nat Med 32, 505–517 (2026). https://doi.org/10.1038/s41591-025-04139-y
Schlüsselwörter: HIV-Reservoir, PD-1-Blockade, Interferonantwort, Krebsimmuntherapie, antiretrovirale Therapie