Clear Sky Science · de
Interpretierbare Entzündungslandschaft zirkulierender Immunzellen
Warum Entzündungen im Blut für Sie wichtig sind
Entzündungen stehen im Zentrum vieler Erkrankungen, von Arthritis und Asthma bis zu COVID-19 und Krebs. Ärztinnen und Ärzte tun sich jedoch oft schwer damit, die entzündlichen Signale des Körpers so zu lesen, dass klar wird, was schiefläuft und welche Behandlung am besten wirkt. Diese Studie baut eine umfassende „Karte“ der Immunzellen im Blut auf und zeigt, wie diese Zellen als lebende, leicht entnehmbare Biomarker dienen könnten, um ein breites Spektrum entzündlicher Erkrankungen zu klassifizieren.
Aufbau einer riesigen Karte der Immunzellen
Um diese Landschaft zu kartieren, analysierten die Forschenden mehr als 6,5 Millionen Immunzellen aus dem Blut von 1.047 Personen. Die Probandinnen und Probanden repräsentierten 19 Zustände, darunter Autoimmunerkrankungen wie Lupus und rheumatoide Arthritis, chronische Lungenerkrankungen wie Asthma und COPD, Infektionen wie COVID-19 und HIV sowie mehrere Krebsarten, außerdem gesunde Spender. Mit Einzelzell‑RNA‑Sequenzierung bestimmten sie, welche Gene in jeder einzelnen Zelle aktiviert waren, korrigierten dann mit fortgeschrittenen statistischen Methoden technische Unterschiede zwischen Studien und gruppierten die Zellen in 64 verschiedene Immunzell‑Zustände. Dieser „Inflammation Atlas“ umfasst sowohl bekannte Akteure – etwa T‑Zellen, B‑Zellen und Monozyten – als auch spezialisiertere Subtypen, die sich mit der Krankheit verändern.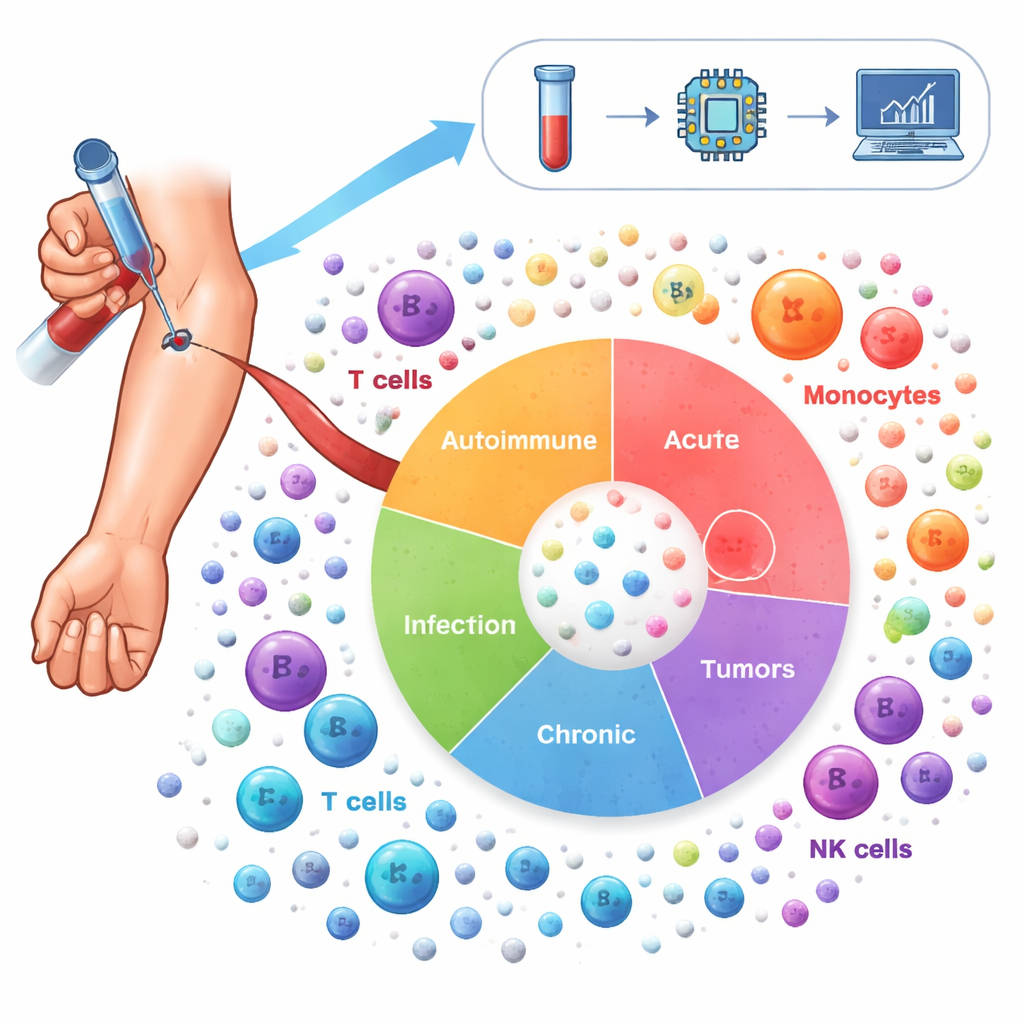
Die entzündlichen Signaturen des Körpers lesen
Das Team konzentrierte sich anschließend auf Gene, die steuern, wie Immunzellen aktiviert werden, sich im Körper bewegen, Antigene präsentieren und auf Signalmoleküle wie Interferone und Tumornekrosefaktor reagieren. Sie fassten diese Gene zu 21 biologischen „Signaturen“ zusammen und verfeinerten sie für jeden wichtigen Zelltyp. Durch den Vergleich von Patientinnen und Patienten mit gesunden Spendern konnten sie erkennen, welche Signaturen in verschiedenen Erkrankungen hoch- oder herunterreguliert waren. Viele immunvermittelte Entzündungskrankheiten zeigten zum Beispiel eine stärkere Aktivität von Adhäsionsmolekülen und antigenpräsentierendem Apparat, während Interferon‑Antworten in den meisten Zelltypen abgeschwächt, aber in bestimmten CD8‑T‑Zellen erhöht waren. Virale Infektionen wie Grippe und COVID‑19 stärkten Interferon‑induzierte Programme, während chronische Infektionen wie HIV und Hepatitis B sie abschwächten.
Hineinzoomen auf Schlüsselfaktoren und Steuerungen
Weil breite Signaturen wichtige Details verbergen, arbeiteten die Forschenden auf Ebene einzelner Gene und deren Regulatoren. In nicht‑naiven CD8‑T‑Zellen stellten sie fest, dass zwei Gene, FGFBP2 und GZMB, in bestimmten Effektor‑Memory‑Subtypen besonders aktiv waren, speziell bei Colitis ulcerosa. Diese Gene wurden mit Schädigungen an Epitheloberflächen in Verbindung gebracht, und ihr starkes Signal im Blut deutet darauf hin, dass diese aggressiven Zellen bereits vor ihrem Eintritt ins Gewebe aktiviert sind. Eine separate Analyse von Genregulationsnetzwerken hob zwei Transkriptionsfaktoren, STAT1 und SP1, als zentrale Steuerungsfaktoren interferon‑induzierter Programme hervor. Deren Aktivitätsmuster unterschieden sich zwischen Erkrankungen und Zelltypen – etwa entgegengesetztes Verhalten in Monozyten versus CD8‑T‑Zellen bei Lupus und Verschiebungen zwischen Schub‑ und Nicht‑Schub‑Phasen – was darauf hindeutet, wie dieselben Signalwege in einem Kontext schützend und in einem anderen schädlich sein können.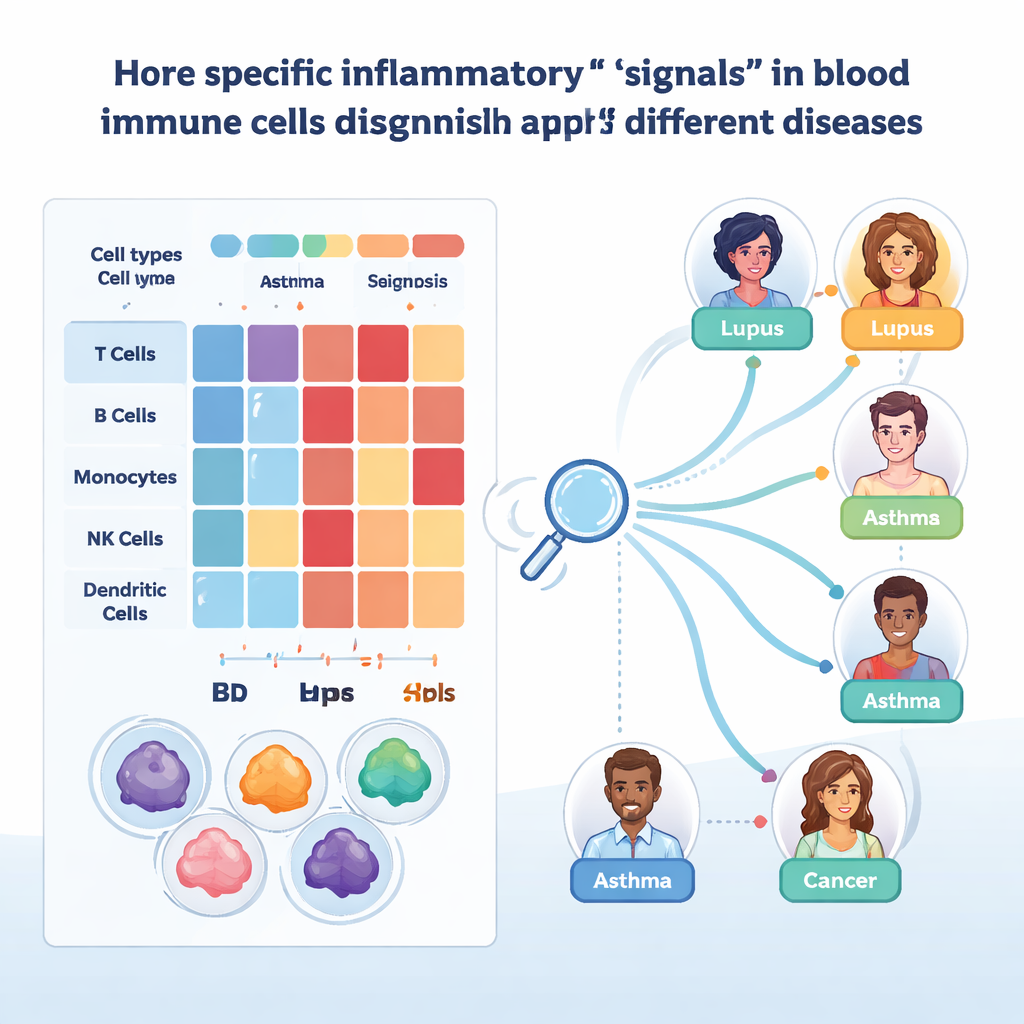
Maschinen trainieren, um Krankheiten aus Blutzellen zu erkennen
Um den Atlas in ein praktisches Werkzeug zu überführen, setzten die Forschenden interpretierbares maschinelles Lernen ein. Sie trainierten gradientenverstärkte Entscheidungsbaum‑Modelle getrennt für jeden großen Zelltyp und ließen die Algorithmen einzelne Zellen anhand ihrer Genexpression der richtigen Erkrankung zuordnen. Diese Modelle erreichten bei Tests an zurückgehaltenen Proben hohe Genauigkeit, besonders nach Korrektur technischer Unterschiede. Mithilfe von SHAP, einer Methode zur Erklärung, welche Gene eine Entscheidung antreiben, konnten die Forschenden Kandidaten für Biomarker identifizieren. Ein Beispiel ist CYBA in Monozyten, dessen Level half, Hauterkrankungen wie Psoriasis von Darmentzündungen wie Morbus Crohn und Colitis ulcerosa zu unterscheiden. Ein anderes ist IFITM1 in bestimmten T‑Zellen und angeborenen lymphoiden Zellen, das Asthma von COPD trennt und unterschiedliche Muster chronischer antiviraler Abwehr nahelegt.
Auf dem Weg zu einem blutbasierten diagnostischen Kompass
Schließlich fragten die Autoren, ob ganze Patientinnen und Patienten – nicht nur einzelne Zellen – anhand ihrer zirkulierenden Immunprofile klassifiziert werden können. Sie projizierten die Daten jeder Zelle in einen komprimierten „Embedding“-Raum, bildeten diese Embeddings pro Zelltyp und Patientin bzw. Patient als Mittelwert und trainierten Klassifikatoren zur Vorhersage der Erkrankung. Wenn neue Patientinnen und Patienten denen der Trainingsdaten ähnelten, war die Leistung ausgezeichnet. Kamen Proben jedoch aus völlig unabhängigen Studien mit anderen Laborverfahren, brach die Genauigkeit stark ein, was die Empfindlichkeit solcher Werkzeuge gegenüber technischer Variabilität offenbart. Ein stärker kontrollierter „zentralisierter“ Datensatz, erzeugt an einem Zentrum mit einer einzigen Sequenzierungschemie, stellte einen Großteil der Leistung wieder her und weist auf die Notwendigkeit standardisierter Protokolle oder sehr großer, heterogener Trainingsdatensätze hin.
Was das für künftige Diagnose und Behandlung bedeutet
Für Laien ist die wichtigste Botschaft: Ihre zirkulierenden Immunzellen tragen einen reichen Fingerabdruck darüber, wie Ihr Körper entzündet ist. Durch das Auslesen dieser Fingerabdrücke Zelle für Zelle zeigt diese Arbeit, dass es möglich ist, viele Erkrankungen zu unterscheiden, Gene zu entdecken, die bestimmte Symptome antreiben könnten, und erste Schritte zur Entwicklung universeller Bluttests zu unternehmen, die entzündliche Erkrankungen klassifizieren. Die Studie ist noch kein fertiger klinischer Test – technische Unterschiede zwischen Studien schränken die Zuverlässigkeit weiterhin ein – aber sie legt das Fundament für künftige „Liquid‑Biopsy“-Werkzeuge, die Ärztinnen und Ärzten helfen könnten, schneller die richtige Diagnose und Behandlung zu finden, basierend auf einer einfachen Blutentnahme.
Zitation: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
Schlüsselwörter: Entzündung, Immunzellen, Einzelzell-RNA-Sequenzierung, Biomarker, Maschinelles Lernen