Clear Sky Science · de
Entzündungshemmende Therapie mit Niedrigdosis‑IL‑2 bei akuten Koronarsyndromen: eine randomisierte Phase‑2‑Studie
Warum es wichtig ist, Gefäßentzündungen zu beruhigen
Viele Menschen, die einen Herzinfarkt oder schwere Brustschmerzen überleben, bleiben trotz Standardmedikamenten wie Statinen und Blutverdünnern einem hohen Risiko für ein weiteres Ereignis ausgesetzt. Ein wesentlicher Grund ist anhaltende Entzündung in den Arterien, die die Gefäßwand reizbar und instabil hält. Diese Studie stellte eine einfache, aber wichtige Frage: Können wir das Immunsystem sicher so beeinflussen, dass diese Entzündung abgeschwächt wird, indem wir sehr niedrige Dosen eines natürlichen Botenstoffs namens Interleukin‑2 (IL‑2) verabreichen? Wenn ja, könnte das einen neuen Weg eröffnen, das Herz zusätzlich zu den herkömmlichen cholesterinsenkenden Medikamenten zu schützen.
Ein neuer Weg, das Immunsystem zu steuern
Die Forscher richteten den Blick auf eine besondere Gruppe weißer Blutkörperchen, die regulatorischen T‑Zellen oder Tregs. Diese Zellen wirken als immunologische „Friedensstifter“: Sie helfen, überschießende Entzündungen abzuschalten und die Heilung zu unterstützen. Frühere Studien zeigten, dass Menschen mit akuten Koronarsyndromen – Herzinfarkten und verwandten Zuständen – weniger und weniger effektive Tregs haben. In hohen Dosen kann IL‑2 aggressive Immunzellen stimulieren und wird in der Krebstherapie eingesetzt; in sehr niedrigen Dosen stärkt IL‑2 hingegen hauptsächlich Tregs. Das Team entwarf die IVORY‑Studie, um zu prüfen, ob Niedrigdosis‑IL‑2, verabreicht nach einem Herzereignis zusätzlich zur üblichen Versorgung, sicher Tregs erhöhen und die Entzündung in den Arterien reduzieren kann.
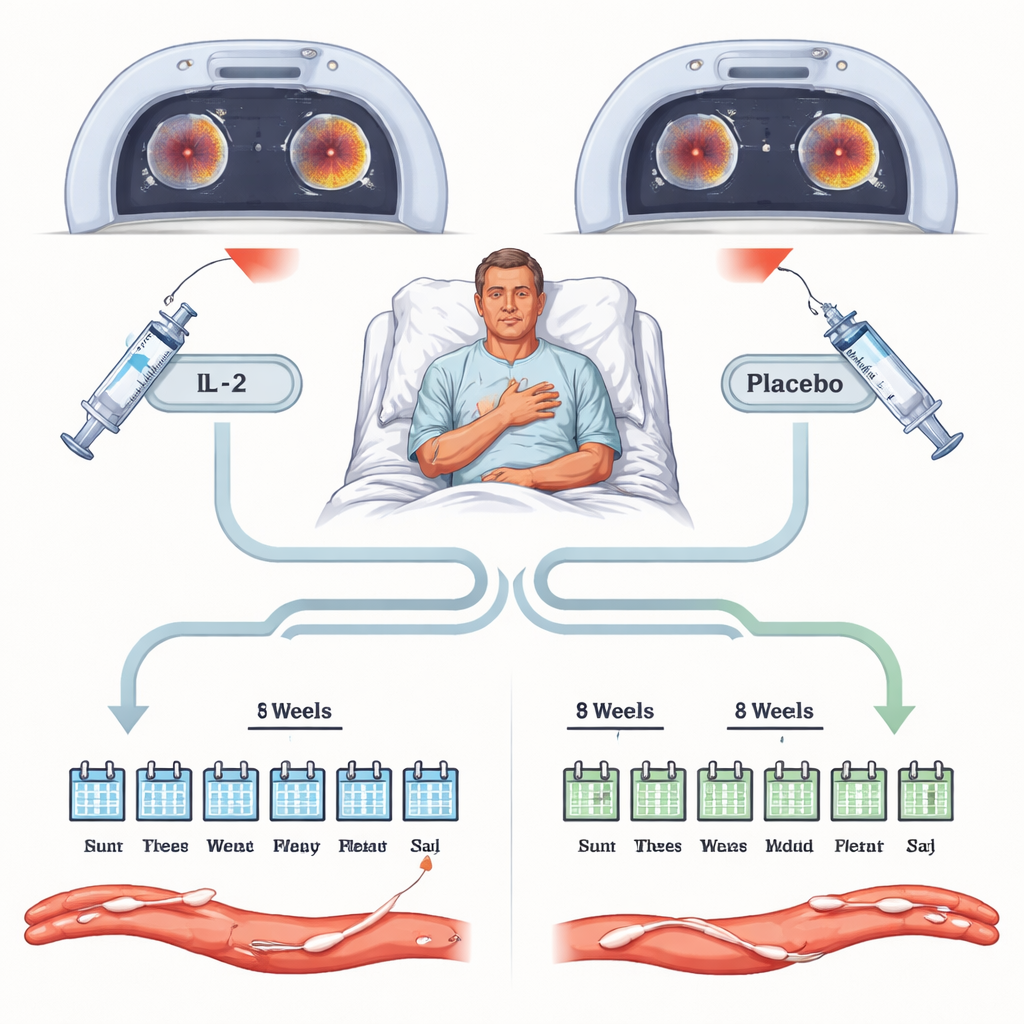
Wie die Studie durchgeführt wurde
Die Studie rekrutierte erwachsene Patienten, die kürzlich wegen eines akuten Koronarsyndroms hospitalisiert worden waren und weiterhin Zeichen einer systemischen Entzündung zeigten, gemessen mit einem Bluttest namens hochsensitives C‑reaktives Protein. 63 Patienten wurden randomisiert und doppelblind einer Behandlung mit entweder Niedrigdosis‑IL‑2 oder einem Placebo für acht Wochen zugeteilt, zusätzlich zu Standardtherapien wie Statinen und Thrombozytenaggregationshemmern. Alle erhielten spezialisierte PET‑CT‑Scans der Hauptbrustschlagader und der Halsschlagadern vor Beginn der Behandlung und erneut nach acht Wochen. Diese Scans messen, wie viel radioaktiver Zucker von der Gefäßwand aufgenommen wird und liefern so eine empfindliche Messgröße für Entzündung. Der primäre Endpunkt war der Unterschied in der arteriellen Entzündung zwischen IL‑2‑ und Placebo‑Gruppen am Ende der Behandlung.
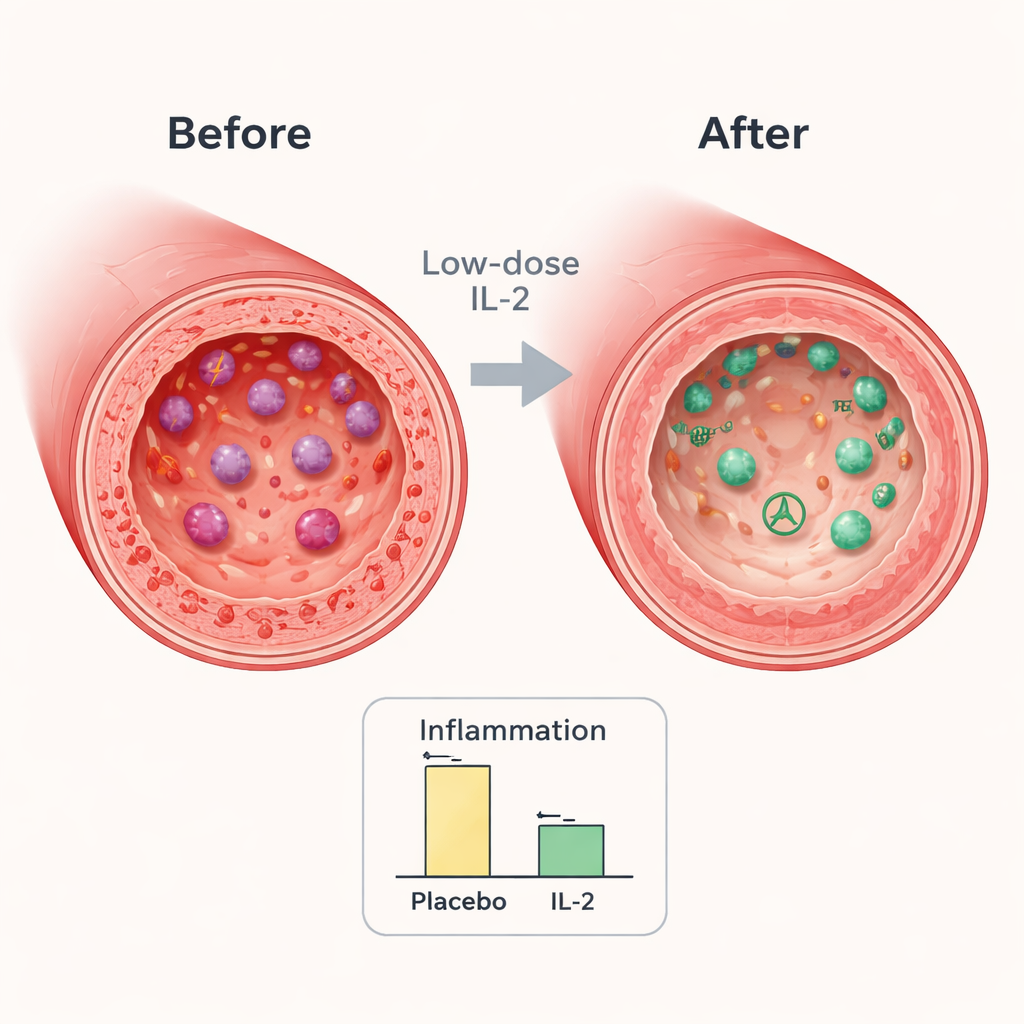
Was sich in den Arterien veränderte
Am Ende der Studie zeigten beide Gruppen eine gewisse Reduktion der arteriellen Entzündung, was zu erwarten ist, da sich Patienten von einem Herzereignis erholen und intensive Standardtherapien erhalten. Der Rückgang war jedoch in der Gruppe, die Niedrigdosis‑IL‑2 erhielt, signifikant größer. In der für jeden Patienten ausgewählten Hauptarterie war die Entzündung in der IL‑2‑Gruppe um etwa 7–8 % niedriger als in der Placebo‑Gruppe. Wenn die Forscher sich auf die am stärksten entzündeten Bereiche der Gefäße konzentrierten, wuchs der Unterschied auf rund 9 %. Diese Reduktionen sind vergleichbar mit denen aus Studien, in denen stärkere cholesterinsenkende Medikamente später zu weniger kardiovaskulären Ereignissen führten, was darauf hindeutet, dass die Veränderung klinisch relevant sein könnte.
Wie das Immunsystem reagierte
Blutuntersuchungen während der Studie zeigten, dass IL‑2 genau das bewirkte, was die Wissenschaftler erwartet hatten. Die Spiegel regulatorischer T‑Zellen stiegen schnell an und blieben während der gesamten Behandlungsdauer um 30–50 % höher als in der Placebo‑Gruppe. Gleichzeitig neigten einige Zelltypen, die mit aggressiveren Immunantworten verbunden sind, darunter bestimmte Helfer‑T‑Zellen und Killer‑T‑Zellen, dazu, abzunehmen oder weniger stark zu steigen. Insgesamt verschob sich das Immunprofil in Richtung eines ruhigeren, stärker regulierenden Zustands. Interessanterweise fiel ein allgemeiner Entzündungsmarker im Blut, das C‑reaktive Protein, unter IL‑2 nicht, was darauf hindeutet, dass das Medikament über einen gezielteren Weg wirkt, der sich nicht unbedingt in breit angelegten Bluttests zeigt, wohl aber in der Gefäßwand sichtbar ist.
Sicherheit und erste Hinweise auf Endpunkte
Sicherheit war ein zentrales Anliegen, denn die Abschwächung von Teilen des Immunsystems kann manchmal das Infektionsrisiko oder andere Komplikationen erhöhen. In dieser Studie wurde Niedrigdosis‑IL‑2 gut vertragen. Die häufigste Nebenwirkung war eine milde Rötung und Juckreiz an der Injektionsstelle, die sich innerhalb von etwa zwei Tagen zurückbildete. Infektionsraten und andere unerwünschte Ereignisse waren zwischen IL‑2‑ und Placebo‑Gruppe ähnlich, und es traten keine behandlungsbedingten schweren Probleme auf. In einer Nachbeobachtung über zwei Jahre erlitten drei Personen in der Placebo‑Gruppe schwerwiegende kardiovaskuläre Ereignisse wie Herzinfarkt, Schlaganfall oder kardiovaskulären Tod, während in der IL‑2‑Gruppe keine derartigen Ereignisse auftraten, wobei diese Zahlen jedoch zu klein sind, um feste Schlussfolgerungen zuzulassen.
Was das für Patienten bedeuten könnte
Für Nicht‑Spezialisten ist die Hauptaussage, dass diese Studie einen frühen, aber ermutigenden Wirkungsnachweis liefert: Durch ein sanftes Anheben der körpereigenen „Bremszellen“ im Immunsystem mit winzigen IL‑2‑Dosen könnten Ärztinnen und Ärzte schädliche Entzündungen in den Arterien nach einem Herzinfarkt vermindern, ohne erhebliche Nebenwirkungen hinzuzufügen. Die Studie ist zu klein, um zu beweisen, dass dieser Ansatz zukünftige Herzinfarkte oder Schlaganfälle verhindert, aber das Ausmaß der entzündungshemmenden Wirkung und das günstige Sicherheitsprofil machen größere Endpunktstudien sinnvoll. Bei Bestätigung könnten Niedrigdosis‑IL‑2 oder ähnliche immunmodulierende Strategien neben Statinen und Blutverdünnern ein neues Instrument werden, um Herzen nach schweren kardialen Ereignissen besser zu schützen.
Zitation: Sriranjan-Rothwell, R.S., Zhao, T.X., Hoole, S.P. et al. Anti-inflammatory therapy with low-dose IL-2 in acute coronary syndromes: a randomized phase 2 trial. Nat Med 32, 624–632 (2026). https://doi.org/10.1038/s41591-025-04090-y
Schlüsselwörter: akutes Koronarsyndrom, arterielle Entzündung, regulatorische T‑Zellen, Interleukin‑2‑Therapie, kardiovaskuläre Immunologie