Clear Sky Science · de
Repotrectinib bei NTRK‑Fusions‑positiven fortgeschrittenen soliden Tumoren: eine Phase‑1/2‑Studie
Neue Hoffnung durch eine zielgerichtete Krebs‑Pille
Krebsbehandlungen werden zunehmend wie präzise Instrumente und weniger wie grobe Werkzeuge entworfen. In dieser Studie geht es um Repotrectinib, eine zielgerichtete Tablette für Patientinnen und Patienten, deren Tumoren seltene genetische Veränderungen namens NTRK‑Fusionen tragen. Obwohl diese Fusionen in weniger als einem von 100 soliden Tumoren vorkommen, können sie in vielen Organen auftreten – von Lunge über Schilddrüse bis zu Weichteilen – und sprechen oft dramatisch auf speziell entwickelte Medikamente an. Das Problem war, dass frühere Wirkstoffe schließlich nicht mehr wirkten. Diese Studie stellt eine einfache Frage mit großer Bedeutung: Kann ein klügeres, nächstgeneratives Medikament Krebs länger unter Kontrolle halten, auch nachdem andere zielgerichtete Therapien versagt haben?
Ein seltener, aber mächtiger Krebs‑Schalter
Manche Krebsarten werden von Fusionen in den Genen NTRK1, NTRK2 und NTRK3 angetrieben. Diese Fusionen wirken wie dauerhaft eingeschaltete Wachstumsschalter in Tumorzellen. Wirkstoffe der ersten Generation, die die daraus resultierenden TRK‑Proteine blockieren, haben bereits vielen Patienten geholfen, doch im Laufe der Zeit findet der Krebs oft Wege, ihnen zu entkommen, indem er neue Mutationen in genau dem Bereich erwirbt, an dem die Medikamente andocken. Repotrectinib wurde so konzipiert, kleiner und kompakter zu sein, damit es auch nach solchen Veränderungen noch in diese Bindungstasche passt. Die internationale TRIDENT‑1‑Studie testete dieses Medikament bei Erwachsenen mit fortgeschrittenen soliden Tumoren, die NTRK‑Fusionen tragen, einschließlich Menschen, die noch nie einen TRK‑Blocker erhalten hatten, sowie solchen, deren Tumor bereits gegen einen oder zwei frühere TRK‑Inhibitoren resistent geworden war.
Was die Studie tat
Die Untersuchung rekrutierte 144 Patienten mit NTRK‑Fusions‑positiven soliden Tumoren an Zentren weltweit; 120 von ihnen bildeten die Hauptgruppe zur Bewertung der Wirksamkeit. Ihre Tumoren umfassten mindestens 18 verschiedene Typen, am häufigsten nicht‑kleinzelligen Lungenkrebs, Schilddrüsenkrebs, Speicheldrüsentumoren und Weichteilsarkome. Alle hatten lokal fortgeschrittene oder metastasierte Erkrankung, und viele hatten bereits mehrere andere Therapien versucht, darunter Chemotherapie, Immuntherapie oder frühere TRK‑Inhibitoren. Die Patienten nahmen Repotrectinib täglich oral nach einem in einer früheren Studienphase erarbeiteten Dosierungsschema. Die Forschenden verfolgten, wie viele Patienten ein Tumorschwinden zeigten, wie lange diese Ansprechen anhielten, wie lange die Patienten lebten, ohne dass die Erkrankung sich verschlechterte, und wie gut das Medikament vertragen wurde.
Starke und anhaltende Ansprechen
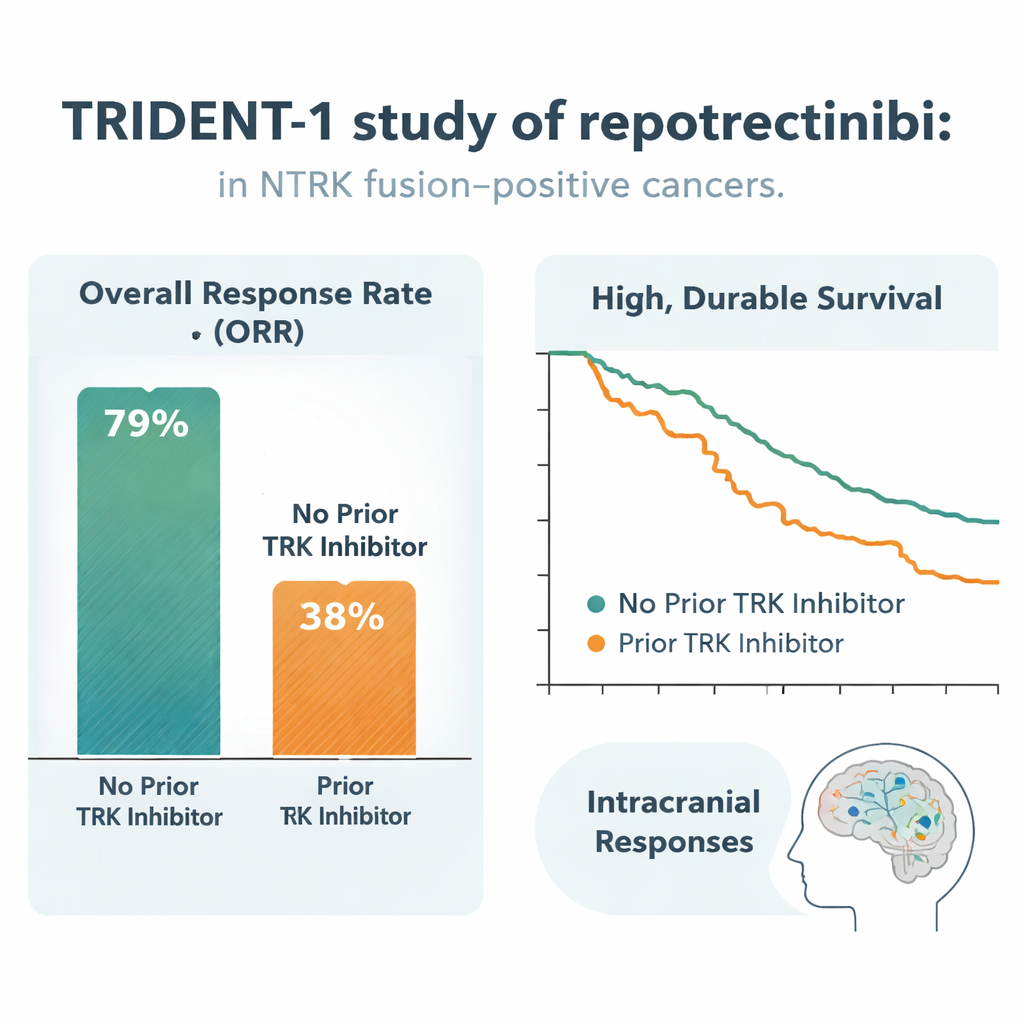
Unter 51 Patienten, die noch keinen TRK‑Inhibitor erhalten hatten, zeigten 59% einen Tumorrückgang, der als objektives Ansprechen zählte, und 16% hatten auf Bildgebung kein nachweisbares Tumorgewebe mehr. Ansprechen traten tendenziell schnell auf — innerhalb von etwa zwei Monaten — und hielten bemerkenswert lange an: nach zwei Jahren profitierten schätzungsweise 85% der Ansprechenden noch, und etwa 60% der gesamten Gruppe hatten noch keinen Krankheitsfortschritt erlebt. Selbst in der stärker vorbehandelten Gruppe von 69 Patienten, deren Tumoren bereits an einem anderen TRK‑Wirkstoff vorbeigegangen waren, sprachen 48% auf Repotrectinib an, mit einer typischen Ansprechdauer von etwa 10 Monaten und etwa einem Viertel der Patienten, die nach einem Jahr noch progressionsfrei waren. Wichtig ist, dass ein Nutzen in vielen Tumortypen sichtbar war und unabhängig davon, welches NTRK‑Gen oder welcher Fusionspartner beteiligt war.
Wirksam gegen resistente Tumoren und Hirnbefall
Eine zentrale Herausforderung für TRK‑Medikamente sind sogenannte Solvent‑Front‑Mutationen, spezifische Veränderungen in der Bindungstasche, die frühere Wirkstoffe blockieren können. In dieser Studie trug fast die Hälfte der vorbehandelten Patienten solche Mutationen zu Studienbeginn. Selbst in dieser schwer zu behandelnden Untergruppe zeigten 53% ein bedeutsames Tumorschwinden unter Repotrectinib, was bestätigt, dass das Medikament zumindest einige Formen der Resistenz überwinden kann. Das Gehirn, ein häufiger Versteckort für Krebs, war ein weiterer Schwerpunkt. Unter Patienten mit messbaren Hirnmetastasen zu Studienbeginn schrumpften bei zwei von drei in der unbehandelten Gruppe und bei vier von sechs in der vorbehandelten Gruppe Tumoren im Gehirn, oft über viele Monate. Bei Patienten ohne initialen Hirnbefall blieben die überwiegende Mehrheit während der Nachbeobachtung frei von neuen Hirnläsionen.
Nebenwirkungen und Bedeutung für Patienten
Bei mehr als 500 mit Repotrectinib behandelten Personen in dieser und verwandten Kohorten waren die häufigsten Nebenwirkungen Schwindel, veränderter Geschmackssinn und Kribbeln, die überwiegend leicht bis mäßig waren. Schwerwiegendere behandlungsbedingte Probleme, wie Anämie oder erhöhte Muskel‑Enzymwerte, waren seltener, und nur etwa 4% der Patienten setzten das Medikament wegen Nebenwirkungen ab. Messungen der allgemeinen Lebensqualität blieben für die meisten Teilnehmenden über viele Behandlungszyklen stabil oder verbesserten sich. Zusammengenommen zeigen die Ergebnisse, dass Repotrectinib eine dauerhafte Kontrolle von NTRK‑Fusions‑positiven Tumoren bieten kann — einschließlich solcher, die gegen frühere TRK‑Wirkstoffe resistent geworden sind und solcher, die ins Gehirn gestreut haben — und dabei insgesamt gut verträglich bleibt. Für Patientinnen und Patienten mit diesen seltenen, aber aggressiven Tumoren stützt die Studie Repotrectinib als wichtige neue Option im wachsenden Instrumentarium der Präzisionsonkologie.
Zitation: Besse, B., Lin, J.J., Bazhenova, L. et al. Repotrectinib in NTRK fusion–positive advanced solid tumors: a phase 1/2 trial. Nat Med 32, 682–689 (2026). https://doi.org/10.1038/s41591-025-04079-7
Schlüsselwörter: zielgerichtete Krebstherapie, NTRK‑Fusion, Repotrectinib, Resistenz gegen TRK‑Inhibitoren, Hirnmetastasen