Clear Sky Science · de
Flt3L-vermittelte Expansion tumorassoziierter cDC1 verbessert die Immuntherapie durch Priming stammzellähnlicher CD8+-T‑Zellen in Lymphknoten
Dem Immunsystem helfen, sich wieder ans Kämpfen zu erinnern
Warum sprechen bei manchen Menschen Tumoren hervorragend auf moderne Immuntherapien an, während andere kaum profitieren? Diese Studie schaut unter die Haube des Immunsystems, um diese Frage zu beantworten. Die Forschenden zeigen, dass durch die Verstärkung einer bestimmten Gruppe von Wachzellen in Tumoren ein Reservoir langlebiger, „stammzellähnlicher“ Killer‑T‑Zellen in den benachbarten Lymphknoten aufgebaut werden kann. Diese Zellen wiederum machen Standard‑Checkpoint‑Medikamente, insbesondere Anti‑CTLA‑4‑Therapie, wirksamer und langfristig beständiger.
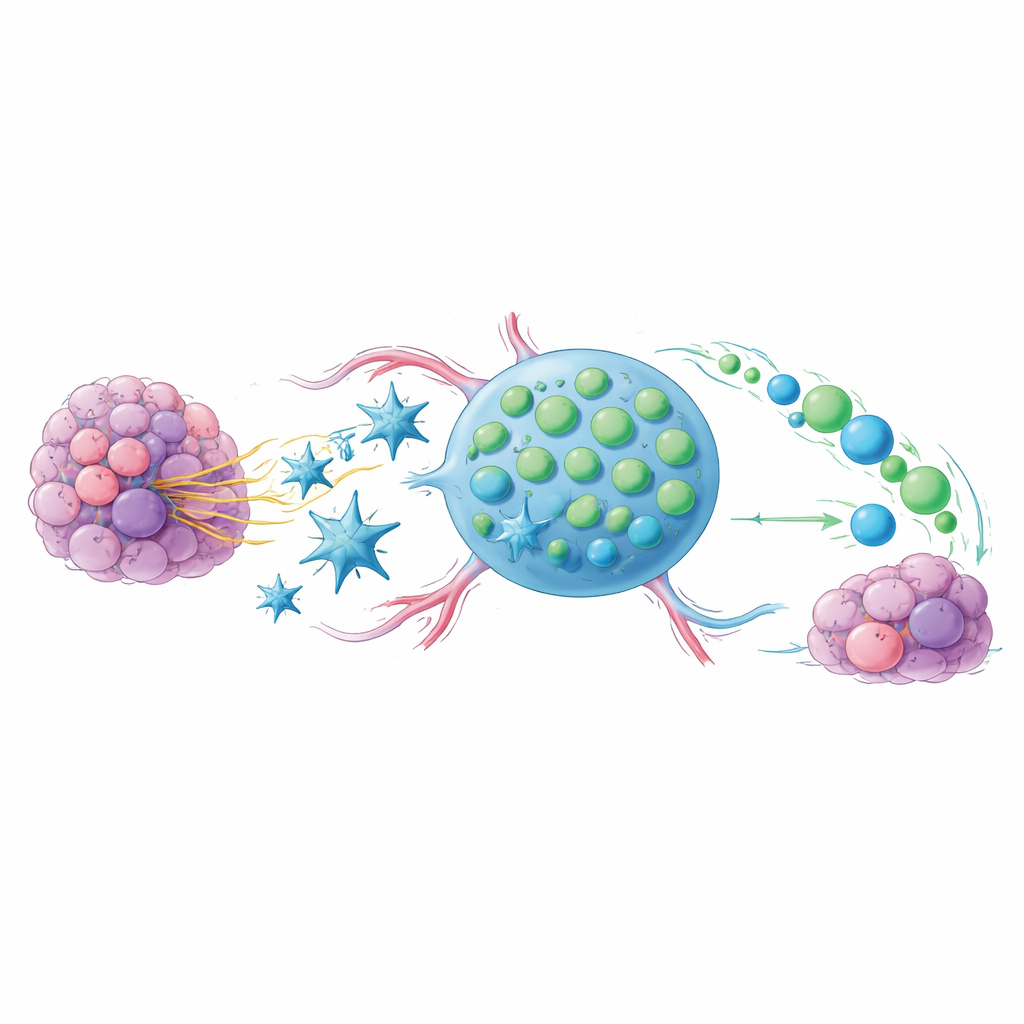
Das Problem ausgelaugter Tumorkämpfer
Checkpoint‑Medikamente wie Anti‑PD‑1 und Anti‑CTLA‑4 setzen Immunzellen gegen Krebs frei, funktionieren aber nur bei einem Teil der Patienten gut. Ein Hinweis liegt im Zustand der CD8‑T‑Zellen, den Hauptmördern infizierter oder tumoröser Zellen. Wenn diese T‑Zellen zu lange und zu stark beansprucht werden, geraten sie in einen erschöpften, „ausgebrannten“ Zustand und vermehren sich nicht mehr effektiv. Eine kleinere Untergruppe bewahrt jedoch einen jugendlicheren, stammzellähnlichen Charakter: Sie teilen sich leicht, erzeugen neue Kämpfer und stehen in starkem Zusammenhang mit guten Antworten bei Patienten, die eine Checkpoint‑Therapie erhalten. Die zentrale Frage dieser Arbeit ist, wie Tumoren und ihre Umgebung so beeinflusst werden können, dass sie diese stammzellähnlichen Zellen den ausgebrannten vorziehen.
Die Wachzellen des Tumors aufladen
Das Team konzentrierte sich auf konventionelle Typ‑1‑dendritische Zellen, eine seltene, aber potente Klasse von Immunwächtern, die besonders gut darin sind, Tumorfragmente T‑Zellen zu präsentieren. Sie nutzten ein Wachstumsignal, den Flt3‑Liganden (Flt3L), um diese Zellen in Maus‑Tumoren zu vermehren, entweder indem sie die Krebszellen so veränderten, dass sie ihn sezernieren, oder indem sie ihn als Arzneimittel verabreichten. Einzelzell‑RNA‑Sequenzierung zeigte, dass Flt3L‑reiche Tumoren deutlich mehr dendritische Zellen und Lymphozyten und weniger Tumorzellen enthielten. Innerhalb der dendritischen Population dehnten sich drei verschiedene Gruppen aus, darunter eine, die hochreif war und auf den Weg in die Lymphknoten vorbereitet schien, wo T‑Zellen erstmals geschult werden. Gleichzeitig verschoben sich die intratumoralen CD8‑T‑Zellen weg von einem terminal erschöpften Profil hin zu einem stammzell‑ oder gedächtnisähnlichen Zustand.
Aufbau eines stammzellähnlichen T‑Zell‑Reservoirs in Lymphknoten
Durch Verfolgen tumorspezifischer T‑Zellen und mithilfe genetischer Werkzeuge zeigten die Forschenden, dass Flt3L‑Behandlung eine Population von CD8‑T‑Zellen fördert, die Oberflächenmarker für stammzellähnliches Potenzial und aktive Teilung tragen. Diese Zellen hingen von XCR1‑positiven dendritischen Zellen ab und von der CCR7‑gesteuerten Migration dendritischer Zellen vom Tumor zum abflussenden Lymphknoten. Wurden dendritische Zellen entfernt oder ihre Migration blockiert, schrumpfte das Reservoir stammzellähnlicher T‑Zellen. Das Blockieren des Lymphozyten‑Austritts aus Lymphknoten hatte einen ähnlichen Effekt, weil die Nachschubversorgung der Tumoren mit erneuerten T‑Zellen abgeschnitten wurde. Molekulares Profiling enthüllte, dass dieser Prozess vom Transkriptionsfaktor Myb abhängig war und Zellen mit relativ schwacher Erkennung tumoraler Zielstrukturen bevorzugte — ein Typ, der zunehmend als wichtig für dauerhafte Krebsbekämpfung erkannt wird.
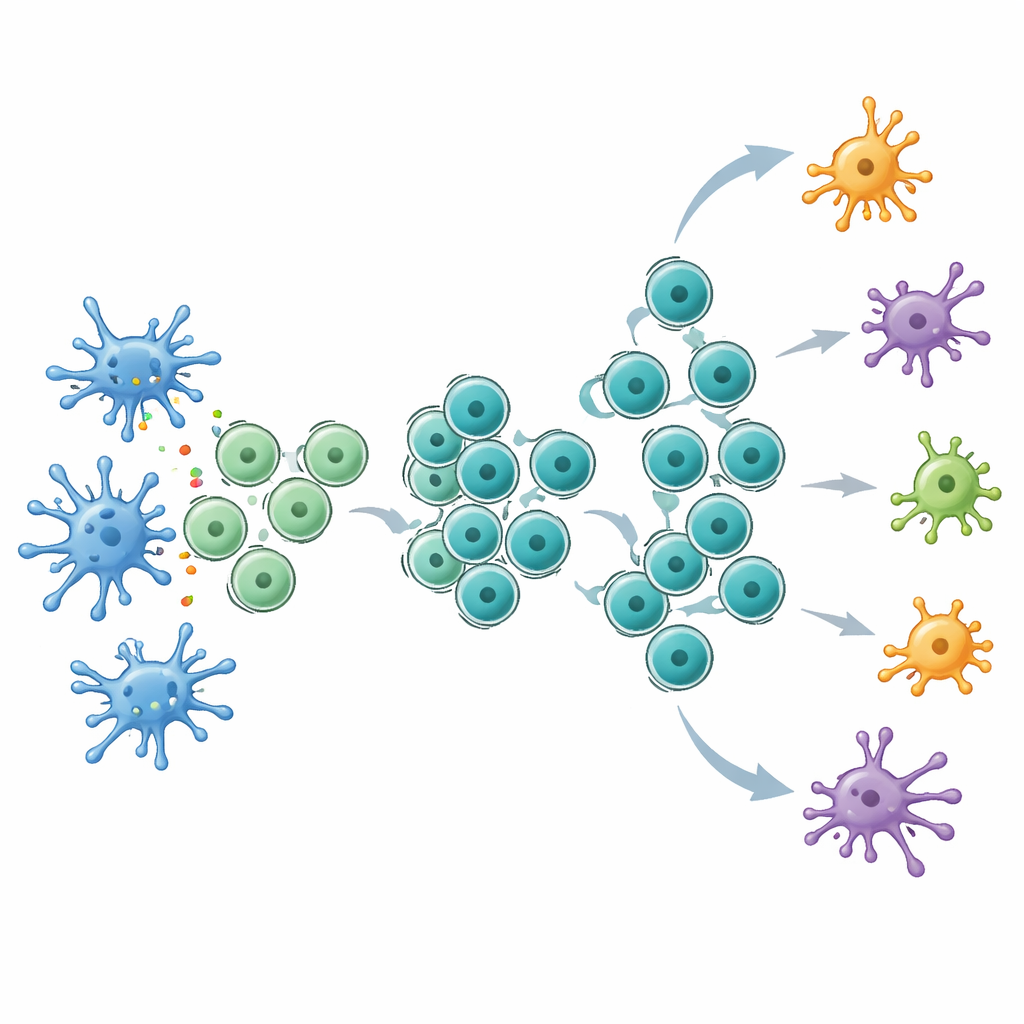
Checkpoint‑Therapie effizienter machen
Mit diesem erweiterten Reservoir stammzellähnlicher T‑Zellen reagierten die Mäuse deutlich besser auf Checkpoint‑Blockade, besonders auf Anti‑CTLA‑4‑Behandlung. Tumoren in Flt3L‑behandelten Tieren schrumpften stärker, das Überleben verbesserte sich, und Blut sowie Lymphknoten enthielten mehr tumorspezifische T‑Zellen. Intratumoral erhöhte Flt3L die Zahl stammzellähnlicher CD8‑Zellen, während nachfolgende CTLA‑4‑Blockade diese Zellen offenbar zur Reifung zu kraftvollen Effektorzellen trieb, die hohe Mengen zentraler antitumoraler Moleküle produzierten. Die Sequenzierung von T‑Zell‑Rezeptoren zeigte, dass die Kombinationstherapie die Bandbreite der expandierenden T‑Zell‑Klone erweiterte, einschließlich vieler subdominanter Klone, was auf einen vielfältigeren Angriff auf den Tumor hindeutet. Detaillierte Einzelzellanalysen identifizierten einen einzigartigen CD8‑T‑Zell‑Cluster, gekennzeichnet durch Expression des Rezeptors für den Immunbotenstoff IL‑21, der sich zwischen stammzellähnlichen und erschöpften Zuständen einordnete und T‑Zell‑Rezeptoren mit sowohl frühen als auch späten Populationen teilte. Das Blockieren der IL‑21‑Signalgebung schwächte die Vorteile der Kombination von Flt3L mit Anti‑CTLA‑4 ab.
Was das für künftige Krebstherapien bedeutet
Für Nichtfachleute lautet die Botschaft: Erfolgreiche Immuntherapie hängt nicht nur davon ab, das Immunsystem stärker anzutreiben, sondern davon, die richtige Art von Zellen dafür bereitzustellen. Diese Arbeit zeigt, dass das Versorgen und Lenken dendritischer Zellen mit Flt3L die benachbarten Lymphknoten mit einem erneuerbaren Pool stammzellähnlicher Killer‑T‑Zellen auffüllen kann. Werden anschließend Checkpoint‑Medikamente wie Anti‑CTLA‑4 eingesetzt, können sie dieses Reservoire nutzen, um Wellen frischer Kämpfer zu erzeugen, die zahlreicher, vielfältiger und besser in der Lage sind, Tumoren zu kontrollieren. Analysen menschlicher Krebsdatensätze deuten darauf hin, dass die mit diesem Weg verknüpften Gensignaturen bessere Patientenergebnisse vorhersagen. Zusammengenommen deuten diese Befunde auf Kombinationstherapien hin, die zuerst mit Agenzien wie Flt3L den richtigen immunzellulären "Stammbestand" aufbauen und diesen anschließend mit Checkpoint‑Medikamenten freisetzen, um eine stärkere und länger anhaltende Krebskontrolle zu erreichen.
Zitation: Lai, J., Chan, C.W., Armitage, J.D. et al. Flt3L-mediated tumor cDC1 expansion enhances immunotherapy by priming stem-like CD8+ T cells in lymph nodes. Nat Immunol 27, 530–542 (2026). https://doi.org/10.1038/s41590-026-02419-4
Schlüsselwörter: Krebsimmuntherapie, dendritische Zellen, stammzellähnliche CD8-T-Zellen, Checkpoint‑Blockade, Flt3‑Ligand