Clear Sky Science · de
CD38 verleiht lokal antigen-spezifischen Treg-Zellen Stressresistenz zur Kontrolle von abgegrenzter Entzündung im ZNS
Warum gehirnschützende Immunzellen wichtig sind
Viele autoimmune Erkrankungen des Gehirns, etwa Multiple Sklerose, gleichen schwelenden Bränden: Eine anfängliche Entzündung flaut ab, aber Schäden können Jahre später wieder aufflammen. Diese Studie stellt eine auf den ersten Blick einfache, doch weitreichende Frage: Was bewahrt nach einem Angriff im zentralen Nervensystem (ZNS) den Frieden – und wodurch kippt das Gleichgewicht zurück in die Krankheit? Die Autorinnen und Autoren konzentrieren sich auf eine kleine Population von Immunzellen, sogenannte regulatorische T-Zellen, die sich nach einer Entzündung im Gehirn und Rückenmark niederlassen, und zeigen, wie ein einziges Oberflächenmolekül ihnen erlaubt, in einer unwirtlichen Umgebung zu überleben und Rückfälle zu verhindern.
Immun-Friedenswächter, die zurückbleiben
Anhand eines Mausmodells, das Aspekte der Multiplen Sklerose nachbildet, verfolgten die Forschenden verschiedene T-Zell-Typen, während die Krankheit ihren Höhepunkt erreichte und dann in eine Erholungsphase überging. Während normale Helfer-T-Zellen, die Entzündungen antreiben, in der Zahl abnahmen, blieben regulatorische T-Zellen – spezialisierte Zellen, die Immunreaktionen dämpfen – im ZNS erhalten. Ihr Anteil am lokalen T-Zell-Pool stieg sogar relativ an, und sie sammelten sich in klar abgegrenzten Nischen rund um Gehirnflüssigkeitsräume und die schützenden Hirnhäute. Durch Kennzeichnung der Herkunft eingehender T-Zellen zeigten die Forschenden, dass nach der Erholung nur sehr wenige neue regulatorische T-Zellen aus Lymphknoten eintrafen. Stattdessen erhielt sich die ZNS-Population überwiegend lokal, was auf eine langfristig residente „Friedenswache“ hindeutet. 
Stressresistente Wächter einer feindlichen Nische
Das postentzündliche ZNS ist alles andere als komfortabel für diese Wächter. Nach der Hauptwelle der Krankheit sinken die Spiegel des Wachstumssignals Interleukin-2 (IL-2) – auf das regulatorische T-Zellen stark angewiesen sind –, weil die meisten konventionellen T-Zellen sich zurückgezogen haben. Gleichzeitig ist das Gewebe reich an dem Stoffwechselmolekül NAD+, das Zelltod auslösen oder wichtige Oberflächenrezeptoren abschwächen kann, wenn es von einem spezifischen Enzym modifiziert wird. Durch genetisches Markieren und Verfolgen einzelner regulatorischer T-Zellen unterschieden die Autorinnen und Autoren „stabile“ Zellen, die ihre Identität bewahrten, von „instabilen“, die ihr charakteristisches Foxp3-Programm verloren. Stabile Zellen zeigten ein deutlich stärkeres IL-2-Signalprofil und höhere Mengen an IL-2-Rezeptoren, was nahelegt, dass die Fähigkeit, knappes IL-2 wahrzunehmen, zentral für das Überleben in dieser Stressumgebung ist.
Lokale Kontrolle von Rückfällen aus dem Inneren des Gehirns
Um zu prüfen, ob diese residenten regulatorischen T-Zellen tatsächlich für die langfristige Krankheitskontrolle wichtig sind, entfernten die Forschenden sie selektiv aus dem ZNS mithilfe eines Toxins, das direkt in die Gehirnflüssigkeit verabreicht wurde, während die meisten systemischen regulatorischen T-Zellen im restlichen Körper intakt blieben. Innerhalb weniger Tage entwickelten zuvor genesene Mäuse schwere Rückfälle mit erneuter Lähmung. Im Gegensatz dazu löste die Entleerung regulatorischer T-Zellen lediglich im Körper, bei Schonung der ZNS-Zellen, keine Aufflammungen aus. Der Rückfall beinhaltete eine rasche Reaktivierung und Expansion von Effektorzellen, die bereits im ZNS verblieben waren, selbst wenn deren Rekrutierung aus dem Blut blockiert war. Das demonstriert, dass lokale regulatorische T-Zellen, und nicht zirkulierende, essenziell sind, um verbleibende aggressive Zellen zu zähmen, die nach dem akuten Angriff zurückbleiben.
Wie ein Enzym regulatorische Zellen schützt
Bei tiefergehenden Untersuchungen suchten die Autorinnen und Autoren nach Molekülen, die stressresistente ZNS-regulatorische T-Zellen kennzeichnen. Ein Schlüsselakteur zeichnete sich ab: CD38, ein Enzym an der Zelloberfläche, das extrazelluläres NAD+ abbaut. Im entzündeten ZNS erhöhten regulatorische T-Zellen stark ihre CD38-Expression, während konventionelle T-Zellen keinen vergleichbaren Wechsel zeigten. Als das Team myelinreaktive regulatorische T-Zellen ohne CD38 in Mäuse übertrug, erreichten diese Zellen zwar das ZNS, konnten die Krankheit jedoch nicht kontrollieren, im Gegensatz zu ihren normalen Gegenstücken. In chimären Mischtieren, in denen nur die residenten regulatorischen T-Zellen CD38-defizient waren, reichte das Entfernen des CD38-fähigen Anteils aus, um Rückfälle zu provozieren, was zeigt, dass CD38 intrinsisch in der Zelle wirkt, um effektive Kontrolle zu ermöglichen.
Schutz des lebenswichtigen Signals
Mechanistische Experimente enthüllten, wie CD38 diese Resilienz vermittelt. Hohe NAD+-Spiegel im ZNS können chemische Modifikationen von Oberflächenproteinen durch das Enzym ARTC2.2 fördern. Ein empfindliches Ziel ist die hochaffine Untereinheit des IL-2-Rezeptors, die regulatorische T-Zellen sehr stark exprimieren, besonders wenn sie Gehirnantigene erkennen. In CD38-defizienten regulatorischen T-Zellen, die NAD+ ausgesetzt wurden, wurden die meisten IL-2-Rezeptoren modifiziert, was zu schwächerer Aktivierung des nachgeschalteten Botenproteins STAT5 und zu verminderter Reaktionsfähigkeit auf IL-2 führte. Im Gegensatz dazu senkten CD38-exprimierende Zellen lokal das NAD+ in ihrer Umgebung, begrenzten diese schädliche Modifikation und bewahrten ein starkes IL-2-Signal. In lebenden Mäusen tötete die Injektion von NAD+ ins Gehirn selektiv die meisten regulatorischen T-Zellen über diesen Pfad, während konventionelle T-Zellen verschont blieben – ein Hinweis darauf, wie prekär die Nische ohne dieses schützende Enzym ist. 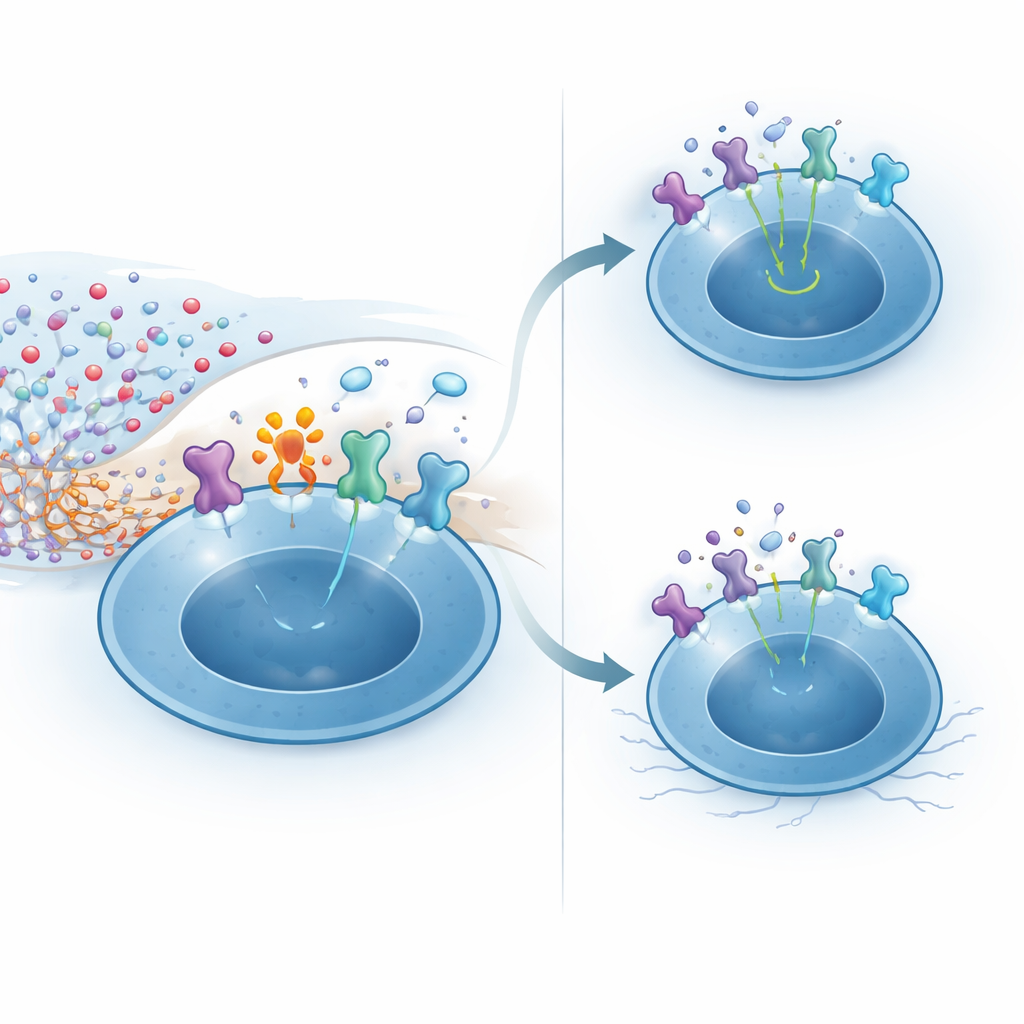
Was das für chronische Autoimmunerkrankungen des Gehirns bedeutet
Diese Arbeit zeichnet das Bild chronischer ZNS-Autoimmunität als eine compartmentalisierte Auseinandersetzung: Kleine Cluster verbleibender aggressiver T-Zellen sitzen im Gehirn und Rückenmark und werden von ebenso spezialisierten lokalen regulatorischen T-Zellen in Schach gehalten. Diese Wächter sind „stressresistent“, weil CD38 ihnen ermöglicht, hohe NAD+-Spiegel zu überstehen und weiterhin winzige IL-2-Mengen zu erkennen, wodurch sie ihre Identität und unterdrückende Funktion bewahren. Für nichtfachliche Leser ist die wichtigste Schlussfolgerung, dass die langfristige Kontrolle von Krankheiten wie Multipler Sklerose womöglich weniger vom zirkulierenden Immunsystem abhängt als davon, diese residenten Friedenswächter im Gehirn zu pflegen und zu schützen – etwa durch Eingriffe, die CD38-Funktionen oder die IL-2-Empfindlichkeit regulatorischer T-Zellen stärken.
Zitation: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
Schlüsselwörter: regulatorische T-Zellen, Multiple Sklerose, Entzündung des zentralen Nervensystems, CD38-Enzym, Immuntoleranz