Clear Sky Science · de
BACH2-Dosis legt die Hierarchie der Stammzell-Eigenschaften fest und justiert die antitumorale Immunität in CAR-T-Zellen
Warum diese Forschung für die künftige Krebsbehandlung wichtig ist
Ingenieurmäßig veränderte Immunzellen namens CAR-T-Zellen haben die Behandlung einiger Blutkrebserkrankungen revolutioniert, doch viele Patientinnen und Patienten erleiden Rückfälle, und die Wirksamkeit gegen solide Tumoren bleibt begrenzt. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenschwere Frage: Kann man an einem einzigen molekularen Stellrad innerhalb von CAR-T-Zellen drehen, damit sie sich mehr wie langlebige, sich selbst erneuernde Stammzellen und weniger wie kurzlebige, erschöpfte Kämpfer verhalten? Die Antwort der Autoren ist: ja — und dieses Stellrad ist ein Protein namens BACH2.
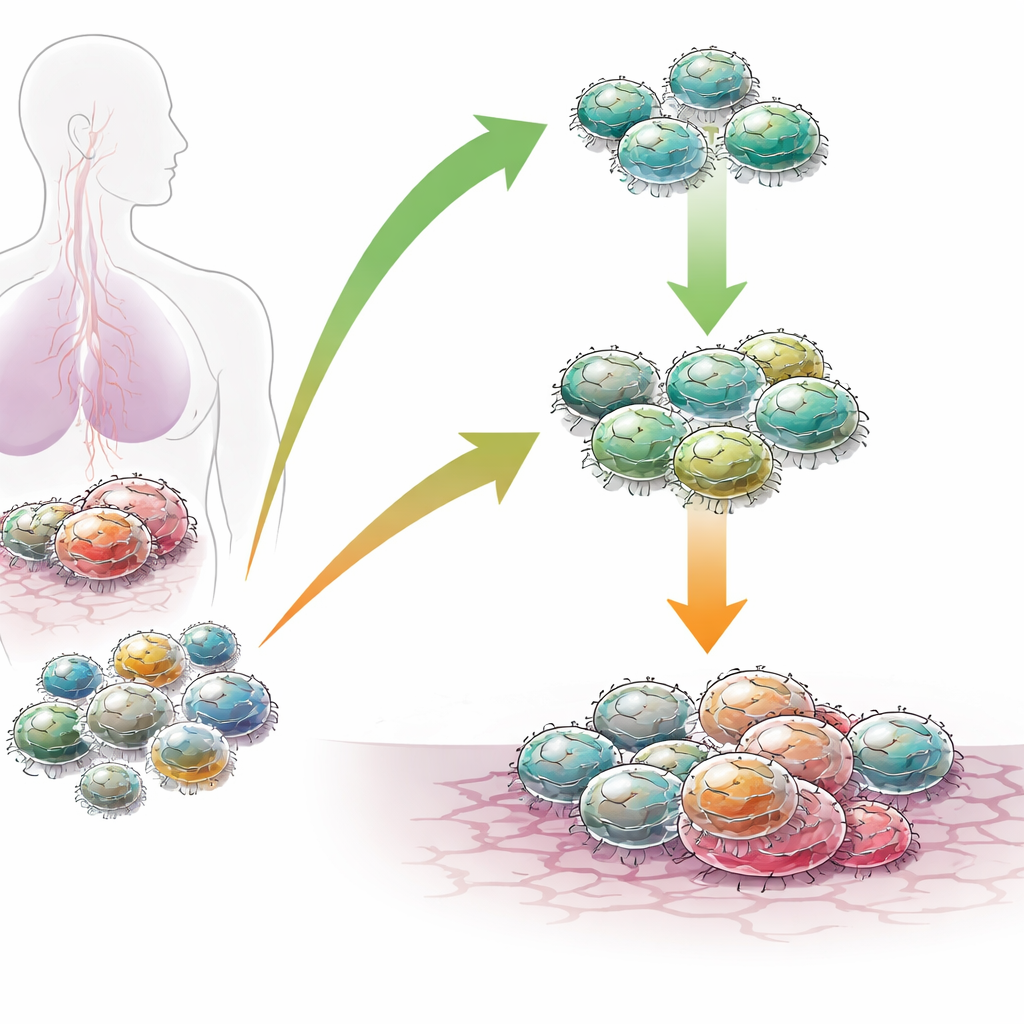
Eine verborgene Rangordnung in krebsbekämpfenden T-Zellen
Nicht alle CAR-T-Zellen sind gleich. In einem Infusionspräparat existiert eine Hierarchie von Zellen mit unterschiedlichen Graden an „Stammzell-Eigenschaften“ — ihrer Fähigkeit zur Selbsterneuerung, zum Verbleib im Körper und zur wiederholten Produktion frischer Wellen tumorbekämpfender Zellen. An der Spitze dieser Hierarchie stehen langfristige, stammzellähnliche T-Zellen, die ausdauern und Gedächtnis bilden können. Mit Einzelzell-genomischen Methoden in Mäusen kartierten die Forscher diese Hierarchie und entdeckten eine Untergruppe von CAR-T-Zellen, deren DNA-Packung und Genaktivität diesem langlebigen Zustand stark entsprach. Diese Elitezellen zeigten geöffnete Regionen in Genen, die mit Gedächtnis und Überleben verbunden sind, und geschlossene Regionen in Genen, die mit terminaler Differenzierung und Erschöpfung assoziiert werden. Kennzeichnend war außerdem eine starke Aktivität von BACH2, einem Protein, das T-Zellen in einem flexiblen, stammzellähnlichen Zustand hält.
Die besseren CAR-T-Zellen tragen bereits ein BACH2-Signatur
Die Gruppe prüfte dann, ob diese langfristigen, stammzellähnlichen Zellen tatsächlich bessere Leistungen gegen Tumoren zeigen. In Mausmodellen von Leukämie und Neuroblastom vermehrten sich CAR-T-Zellen, die für einen Oberflächenmarker der langlebigen Untergruppe angereichert waren, stärker, widerstanden dem Zelltod, zeigten weniger Erschöpfungssignale und kontrollierten Tumoren wirksamer als ihre reiferen Gegenstücke. Bei der Analyse von Human‑Daten aus 40 Personen, die mit CD19-CAR-T-Zellen gegen B‑Zell-Lymphome behandelt wurden, werteten die Autoren Einzelzell-RNA-Profile der Infusionsprodukte neu aus. Patientinnen und Patienten, die in eine komplette Remission gingen, hatten CD8-T-Zellen mit höherer Expression von BACH2 und anderen Genen, die für langfristige, stammzellähnliche Eigenschaften stehen, verglichen mit denen, die keine Remission erreichten. Das deutet darauf hin, dass ein höherer Anteil an BACH2-markierten, stammzellähnlichen Zellen im Präparat die Wahrscheinlichkeit dauerhafter Ansprechraten erhöhen kann.
Ein Schalter, der T-Zellen jugendlich hält
Um von Korrelationen auf Kausalität zu schließen, entfernten die Forscher gezielt BACH2 in murinen CAR-T-Zellen. Ohne dieses Protein vermehrten sich die Zellen schlecht, verloren rasch stammzellähnliche Marker und regten Erschöpfungsmoleküle wie PD‑1, TIM3 und den Regulator TOX stärker an. Ihre Fähigkeit, Tumoren zu kontrollieren und bei erneutem Auftreten des Krebses eine starke „Erinnerungs“-Antwort zu zeigen, war beeinträchtigt. Genomische Bindungsexperimente zeigten, dass BACH2 an DNA-Regionen sitzt, die die Aktivität anderer Faktoren wie JunB einschränken, die bekanntermaßen Erschöpfung antreiben. Effektiv wirkt BACH2 als Wächter, der die Zellen in einem bereiten, langlebigen Zustand hält und ein vorzeitiges Ausbrennen verhindert.
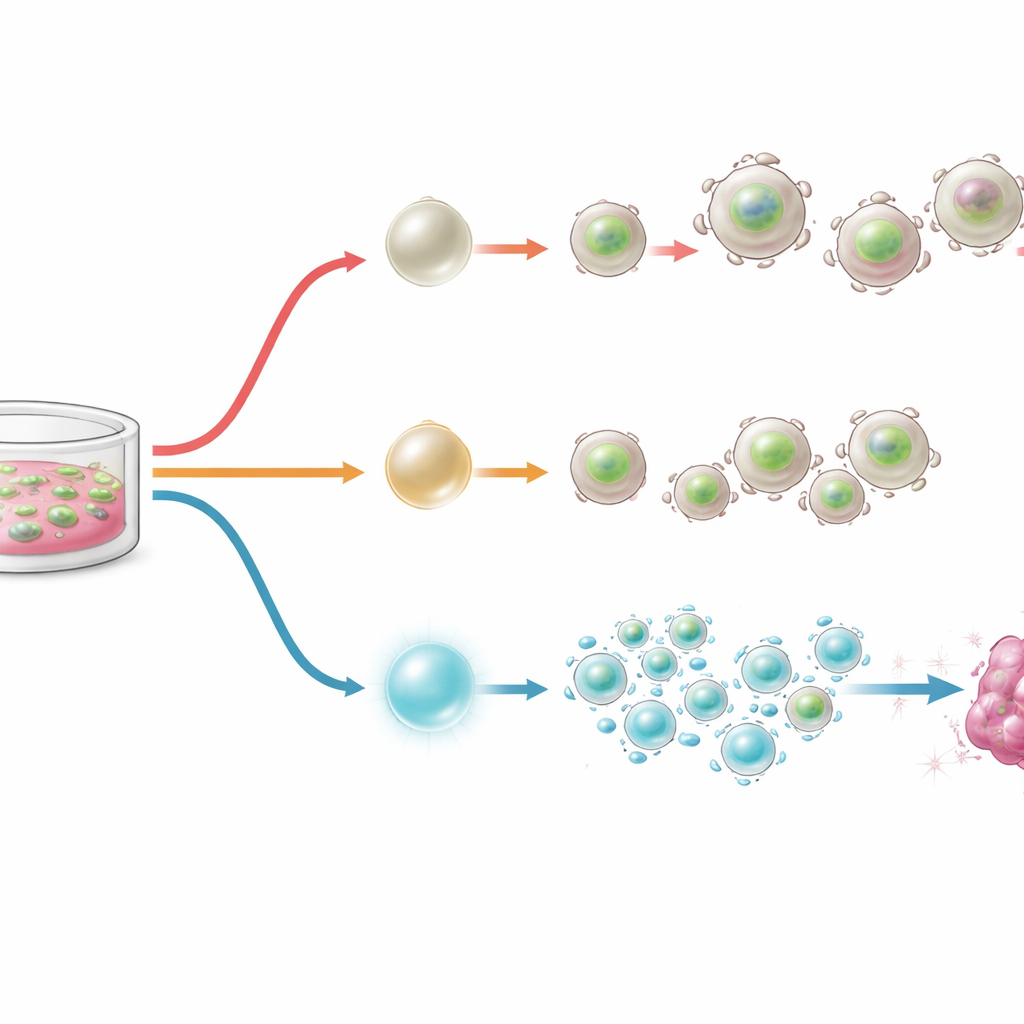
BACH2 hoch- und runterdrehen mit Designer-Schaltern
Mit diesem Wissen konstruierten die Autoren molekulare Schalter, mit denen sie BACH2-Spiegel während der CAR-T-Herstellung fein regulieren konnten. In einem Konstrukt war BACH2 an ein Tag gekoppelt, das es instabil macht, solange nicht ein kleines Molekül, Shield‑1, hinzugefügt wird; mehr Shield‑1 führt zu mehr BACH2-Protein. In einem anderen Design war BACH2 mit einer hormonempfindlichen Domäne verbunden, die das Protein nur in den Zellkern bringt, wenn ein dem Tamoxifen verwandtes Medikament zugeführt wird. In Kulturmodellen von CAR-T-Zellen, die zu chronischer Aktivierung neigen, erhöhte eine schrittweise Steigerung von BACH2 den Anteil stammzellähnlicher Zellen und verringerte Erschöpfungsmarker dosisabhängig. Bemerkenswert war, dass schon eine kurze Aktivierung von BACH2 während der Herstellung einen anhaltenden Fingerabdruck hinterließ: Nach Entfernung des Wirkstoffs behielten die Zellen mehr stammzellähnliche Eigenschaften und weniger Erschöpfungsmerkmale.
Erprobung abgestimmter CAR-T-Zellen gegen solide Tumoren
Der ultimative Test war, ob diese molekulare Feinabstimmung in lebenden Tieren einen praktischen Unterschied macht. Wenn Mäusen mit schwer zu behandelndem solidem Neuroblastom CAR-T-Zellen gegeben wurden, bei denen BACH2 während der Herstellung aktiviert worden war, kontrollierten diese Zellen die Tumoren besser als Standard‑CAR-T-Zellen. Ähnliche Strategien funktionierten auch mit humanen CAR‑T‑Zellen im Labor: Chemisch induziertes BACH2 steigerte Gedächtnismarker und reduzierte Erschöpfungssignale. Diese Ergebnisse zeigen, dass BACH2 nicht nur ein Marker erwünschter Zellen ist, sondern ein Hebel, an dem Forscher drehen können, um das Verhalten von CAR‑T‑Zellen zu formen.
Was das für Patientinnen und Patienten bedeuten könnte
Für Menschen mit Krebs deutet diese Arbeit auf eine Zukunft hin, in der CAR‑T‑Therapien nicht einfach an- oder ausgeschaltet, sondern sorgfältig abgestimmt werden. Durch Anpassung der Dosierung und des Timings eines einzelnen Regulators, BACH2, während des Herstellungsprozesses könnten Kliniker langlebigere, stammzellähnliche CAR‑T‑Zellen anreichern, die durchhalten, sich anpassen und Tumoren unter Kontrolle halten — insbesondere solide Tumoren, die heute schwer zu behandeln sind. Zwar ist noch viel klinisch zu prüfen, doch die Studie liefert einen Entwurf dafür, wie man durch dynamische Steuerung interner Programme smartere, haltbarere Zelltherapien herstellen kann, die entscheiden, ob eine T‑Zelle jugendlich bleibt oder zu früh ausbrennt.
Zitation: Hu, T., Zhu, Z., Luo, Y. et al. BACH2 dosage establishes the hierarchy of stemness and fine-tunes antitumor immunity in CAR T cells. Nat Immunol 27, 425–435 (2026). https://doi.org/10.1038/s41590-025-02388-0
Schlüsselwörter: CAR-T-Zellen, BACH2, T-Zell-Erschöpfung, Krebsimmuntherapie, stammzellähnliche T-Zellen