Clear Sky Science · de
Räumliche Muster der TGFβ‑Signalgebung in Fibroblasten als Grundlage für Therapieresistenz bei rheumatoider Arthritis
Warum hartnäckige Gelenkschmerzen relevant sind
Viele Menschen mit rheumatoider Arthritis nehmen moderne Medikamente, die das Immunsystem dämpfen, doch ihre Gelenke bleiben schmerzhaft und steif. Diese Studie fragt, warum einige Patientinnen und Patienten nicht besser werden, obwohl die Entzündung im Gelenk zu schwinden scheint. Durch genaues Betrachten, wo und wie bestimmte Stütz‑/Bindegewebszellen im Gelenk Narbenprogramme aktivieren, entdecken die Forschenden eine verborgene Form von Gewebeschaden, die anhaltende Schmerzen erklären und auf neue Behandlungsstrategien hinweisen könnte.
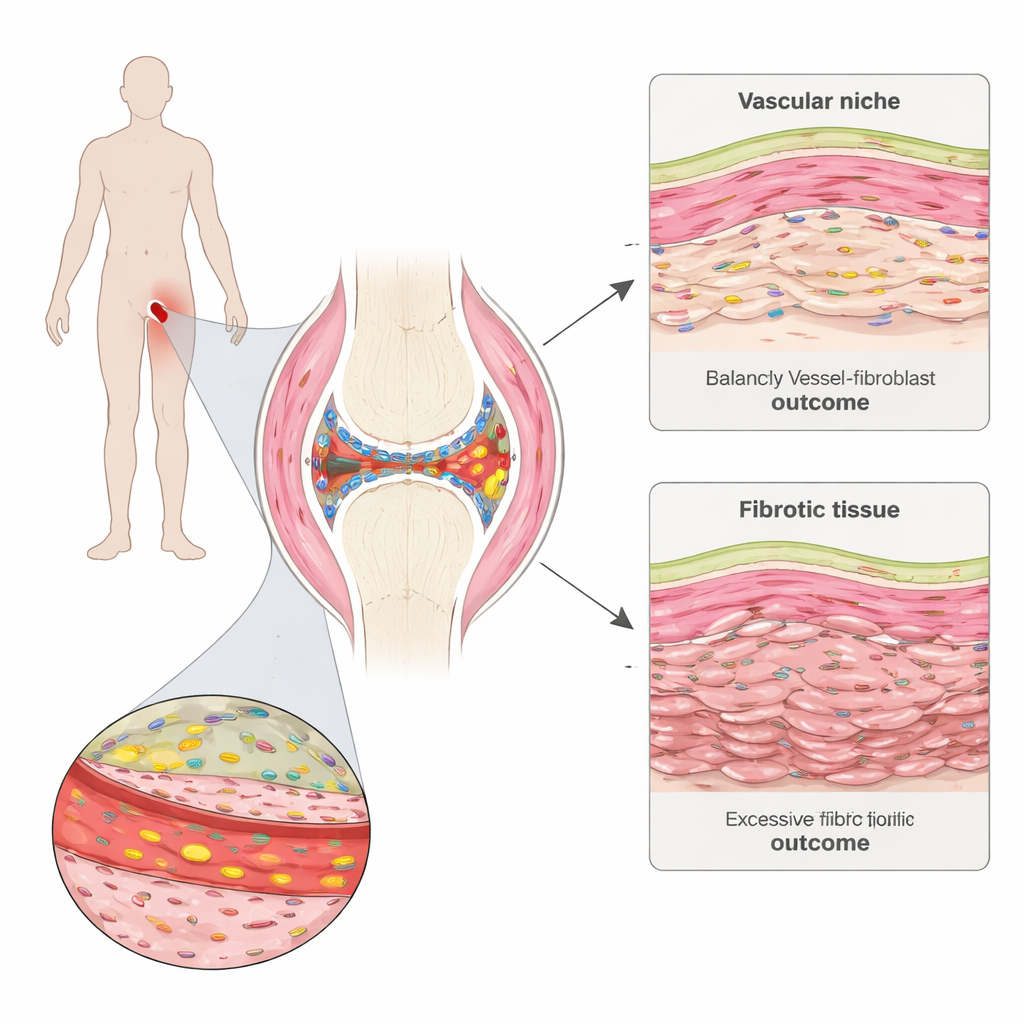
Ein genauerer Blick ins schmerzende Gelenk
Rheumatoide Arthritis greift die Synovialmembran an, ein dünnes Gewebe, das Gelenke auskleidet und schmiert. Das Team entnahm kleine Synovialbiopsien von Menschen mit frühem Krankheitsverlauf vor Therapiebeginn und erneut sechs Monate später. Mit fortschrittlicher räumlicher Genkartierung konnten sie sehen, welche Gene in Tausenden einzelner Zellen aktiv waren und gleichzeitig deren Lage im Gewebe erhalten. Sie identifizierten unterschiedliche „Nachbarschaften“ in der Synovialmembran, darunter Immunzellcluster, fettreiche Bereiche, die dünne Innenauskleidung und Regionen, die dicht mit Blutgefäßen und strukturellen Zellen namens Fibroblasten besetzt sind.
Narbenbildende Zellen und Therapieresistenz
Im Vergleich zwischen Patientengruppen, die später in Remission gingen, und solchen, die dies nicht taten, zeigte sich ein auffälliges Muster: Vor der Behandlung hatten die nicht‑remittierenden Patienten bereits stärkere Signale für Gewebefibrose. Ein bestimmtes Fibroblastenprogramm, gekennzeichnet durch hohe Produktion eines extrazellulären Matrixproteins namens COMP, war bei diesen Patienten vermehrt. Diese COMP‑reichen Fibroblasten zeigten Gemeinsamkeiten mit narbenbildenden Zellen, wie sie bei Lungen‑ und Hautfibrose vorkommen, und standen am stärksten im Zusammenhang mit schlechtem Therapieansprechen. Im Verlauf wurden Regionen, die von diesen Zellen dominiert waren, tendenziell dicht mit Bindegewebe durchsetzt, aber relativ zellarm — ein Hinweis darauf, dass sie eine steife Matrix ablagern, die bestehen bleiben kann, selbst wenn die Entzündung nachlässt.
Blutgefäße als verborgene Dirigenten
Die fibrogenen Fibroblasten waren nicht zufällig verteilt. Sie gruppierten sich um Blutgefäße und bildeten geschichtete perivaskuläre Zonen. Die innerste Schicht, dicht an der Gefäßwand, exprimierte andere Gene als die äußere Schicht. Die Forschenden zeigten, dass Gefäßendothelzellen Notch‑Signale an nahegelegene Fibroblasten senden, die wiederum beeinflussen, wie diese auf die pro‑narbigen Signale der TGF‑beta‑Familie reagieren. In unmittelbarer Nähe des Gefäßes fördert Notch die TGF‑beta‑Produktion in Fibroblasten, senkt aber gleichzeitig die Zahl der TGF‑beta‑Rezeptoren auf ihrer Oberfläche und hält so deren Empfindlichkeit in Schach. Weiter entfernt, wo der Notch‑Einfluss nachlässt, tragen Fibroblasten mehr Rezeptoren und werden hochreaktiv, verwandeln sich in COMP‑reiche Zellen und treiben die Fibrose voran.
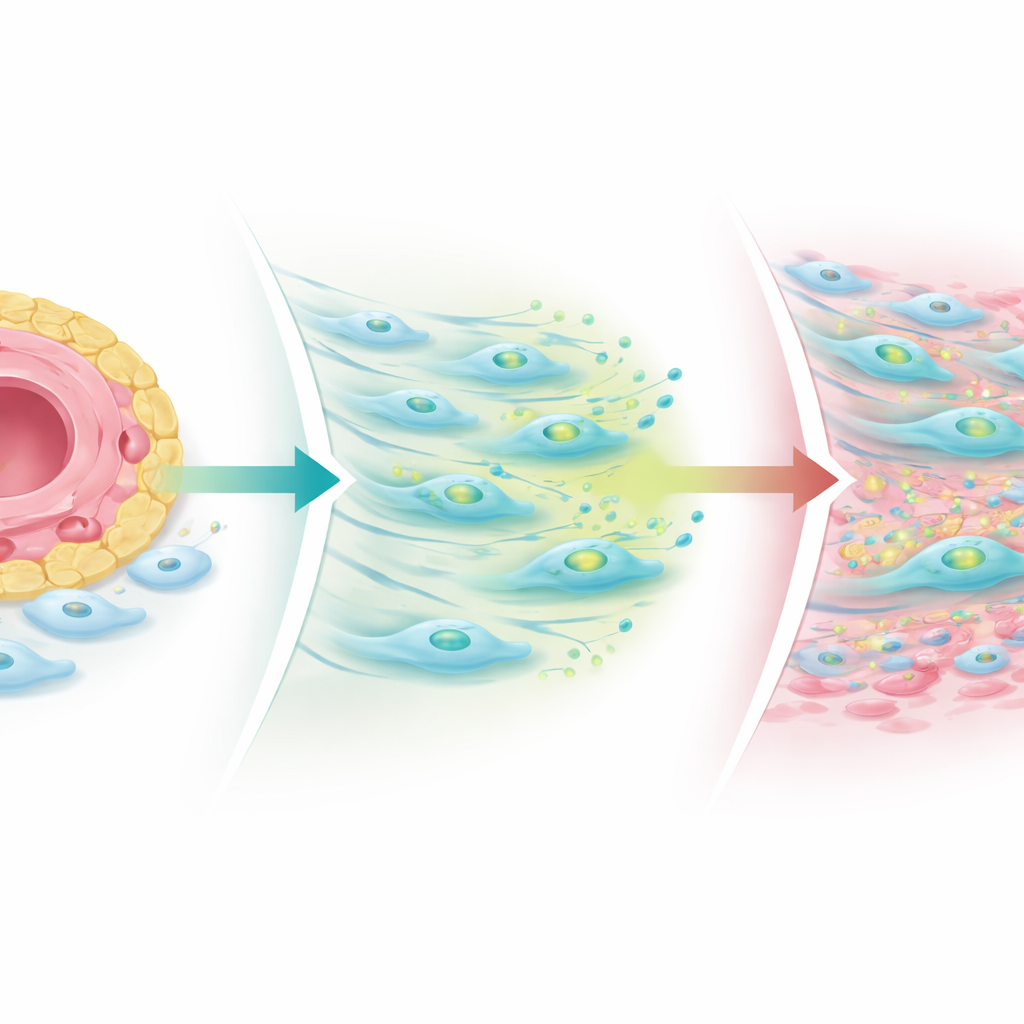
Was passiert, wenn das Gleichgewicht gestört ist
Die Forschenden bauten vereinfachte Gelenkmodelle in Zellkulturen und dreidimensionale Organoide aus Patientengewebe, um diesen Mechanismus zu untersuchen. Wenn sie Notch‑Signale von Endothelzellen verstärkten, produzierten Fibroblasten mehr TGF‑beta, reduzierten jedoch die Rezeptorzahl, wodurch die Narbenbildung begrenzt wurde. Wenn sie Notch blockierten oder sein gleichmäßiges Muster störten, gewannen Fibroblasten TGF‑beta‑Rezeptoren zurück — insbesondere einen Co‑Rezeptor namens TGF‑beta‑Rezeptor III — und COMP‑positive fibrogene Zellen breiteten sich von den Gefäßen weg aus. In Patientenbiopsien, die nach der Behandlung entnommen wurden, schrumpften Immunzellcluster bei fast allen, doch fibrogene Nischen, insbesondere COMP‑reiche Regionen, wuchsen häufig weiter, vor allem bei denen mit anhaltenden Gelenkschmerzen. Das legt nahe, dass Standard‑Antientzündungsmedikamente das immunologische „Feuer“ löschen können, dabei aber einen narbigen Prozess im Gewebe zurücklassen oder sogar freilegen, der Gelenke steif und schmerzhaft hält.
Neue Wege, hartnäckige Gelenke zu beruhigen
Schließlich prüfte das Team, ob die Störung dieses fibrogenen Kreislaufs therapeutisch sinnvoll sein könnte. In patientenabgeleiteten Organoiden reduzierten Wirkstoffe, die Notch hemmen oder die TGF‑beta‑Signalgebung blockieren, die Produktion von COMP, anderen narbenassoziierten Proteinen und wichtigen Kollagenen und veränderten die Genaktivität in perivaskulären Zonen. Für eine allgemein verständliche Schlussfolgerung lautet die Botschaft: Nicht jeder Schaden bei rheumatoider Arthritis beruht auf sichtbarer Entzündung — ein Teil ist in den Stütz‑ und Gefäßzellen des Gelenks „hart verdrahtet“. Durch gezieltes Eingreifen in das Notch–TGF‑beta‑Gespräch, das steuert, wie Fibroblasten Narbengewebe ablagern, könnten künftige Behandlungen eine hartnäckige, fibrotische Form der Erkrankung verhindern oder umkehren, die den heutigen immune‑fokussierten Medikamenten widersteht.
Zitation: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
Schlüsselwörter: rheumatoide arthritis, Fibrose, Fibroblasten, TGF‑Beta‑Signalgebung, Notch‑Weg