Clear Sky Science · de
Identifizierung eines potenten, V3-Glykan-gerichteten breit neutralisierenden Antikörpers, der ein N332-gp120-Glykan-unabhängiges Epitop erkennt
Auf der Suche nach neuen Wegen, HIV zu entwaffnen
Seit mehr als vier Jahrzehnten weigert sich HIV hartnäckig, sich unseren besten Bemühungen um einen Impfstoff oder eine einfache, dauerhafte Heilung zu beugen. Eine vielversprechende Strategie besteht darin, seltene Antikörper von Menschen zu nutzen, deren Immunsystem das Virus von Natur aus in Schach hält, und diese Moleküle in Medikamente oder Vorlagen für Impfstoffe zu verwandeln. Diese Studie beschreibt einen solchen Antikörper, genannt 007, der eine Schwachstelle auf der äußeren Hülle von HIV auf ungewöhnliche Weise erkennt und damit neue Möglichkeiten für Prävention, Therapie und vielleicht funktionelle Heilungsstrategien eröffnet.
Ein kraftvoller Antikörper von einem ungewöhnlichen Spender
Die Forscher begannen damit, das Blut von mehr als zweitausend Menschen mit HIV zu screenen, um „Elite-Neutralisierer“ zu finden – Personen, deren Antikörper eine breite Palette von Virusvarianten ausschalten können. Ein Spender aus Tansania, bezeichnet als EN01, fiel durch außergewöhnlich breite und potente virushemmende Aktivität auf. Aus den B-Zellen dieser Person isolierte das Team Dutzende von Antikörpern und identifizierte eine Familie, genannt 007, die Viren aus mehreren HIV-Subtypen kraftvoll neutralisierte. Im Gegensatz zu einigen früheren Antikörpern, die manchmal körpereigenes Gewebe erkannten, zeigte 007 in Standard-Sicherheitsassays keine nachweisbare Selbstreaktivität, was ihn zu einem starken Kandidaten für die weitere Entwicklung machte.
Eine verborgene Schwachstelle in der Virushülle treffen
HIV schützt sich durch einen dichten Wald aus Zuckerresten, die seine äußere Hüllprotein bedecken und dem Virus helfen, den meisten Antikörpern zu entgehen. Viele der am besten untersuchten breit neutralisierenden Antikörper heften sich an eine Region nahe der Basis einer Schleife dieses Proteins, bekannt als die V3-Region, und sind stark von einer bestimmten Zuckerstelle namens N332 abhängig. Der Antikörper 007 bricht jedoch diese Regel. Mithilfe hochauflösender Kryo-Elektronenmikroskopie zeigen die Autoren, dass 007 eine lange Schleife von seiner Bindungsfläche in eine konservierte Rinne der V3-Region einführt, präzise Kontakte mit einer kurzen Aminosäuresequenz dort macht und sich dabei auf Zucker an zwei benachbarten Positionen stützt. Entscheidenderweise ist er überhaupt nicht auf das übliche N332-Glykan angewiesen, was bedeutet, dass Viren, die den gängigen Fluchttrick anwenden, dieses Glykan zu verändern oder zu entfernen, gegenüber 007 weiterhin verwundbar bleiben.
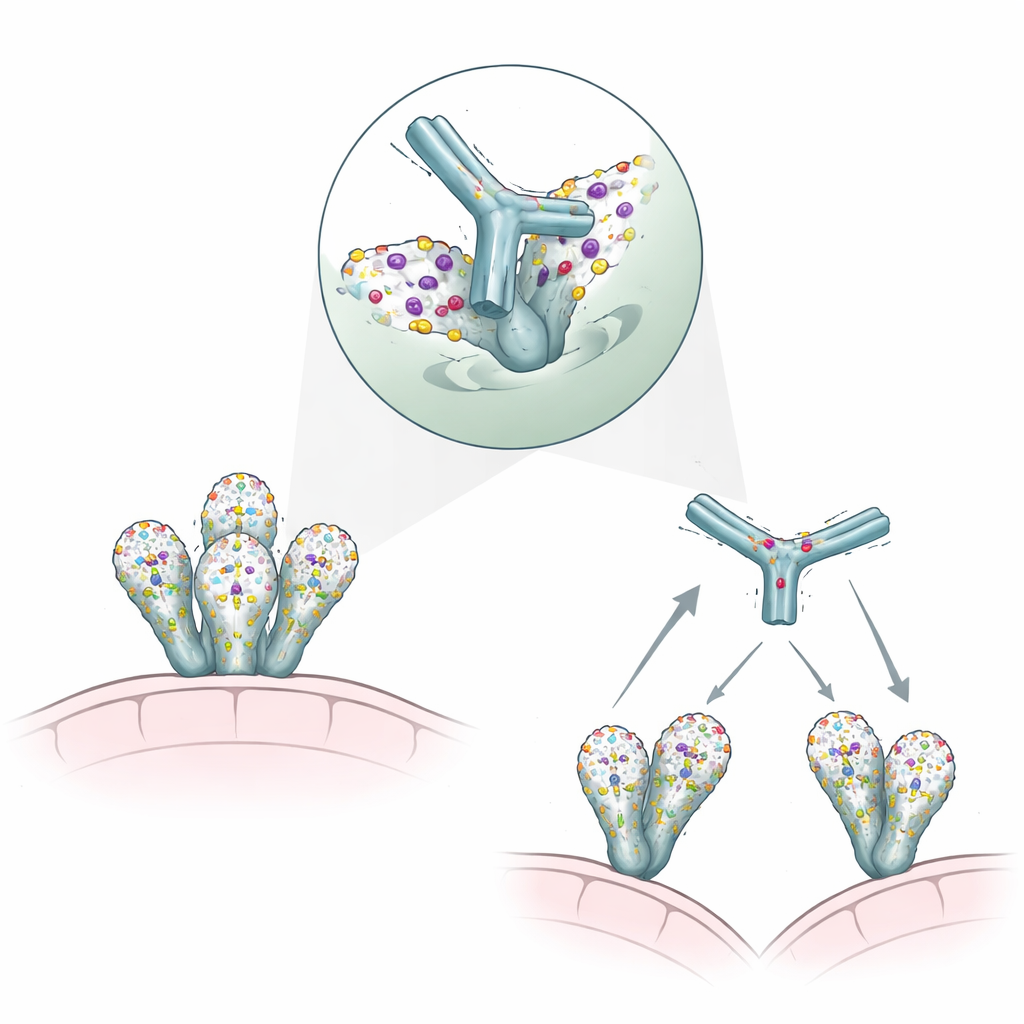
Wie 007 durch beidhändiges Binden zusätzlichen Halt gewinnt
Als das Team einen einzelnen „Arm“ von 007, genannt Fab-Fragment, testete, band dieser nur schwach an lösliche Versionen des HIV-Hüllspikes. Doch der komplette Antikörper mit zwei Armen war bemerkenswert potent bei der Neutralisierung lebender Viren. Detaillierte Bindungs- und Neutralisationsmessungen zeigten, dass 007 stark davon profitiert, beide Arme gleichzeitig zu verwenden, ein Phänomen, das als Avidität bekannt ist. Strukturelle Untersuchungen mit dem intakten Antikörper und trimeren Hüllproteinen zeigten, dass drei Kopien von 007 zwei virale Spikes zu einer symmetrischen dimerähnlichen Anordnung vernetzen können, was darauf hindeutet, dass der Antikörper Spikes auf demselben oder benachbarten Partikeln überbrücken kann. Dieses beidhändige Engagement scheint eine mäßige Einzelarm-Affinität auszugleichen und hilft zu erklären, weshalb 007 so effektiv darin ist, resistente, klinisch relevante Virusstämme zu inaktivieren.
Hervorstechend im Vergleich zu anderen HIV-Antikörpern
Um zu verstehen, wie sich 007 gegenüber bekannten HIV-Antikörpern verhält, testeten die Autoren ihn gegen große Panels vielfältiger Virusstämme, einschließlich schwer zu neutralisierender Varianten aus vielen Teilen der Welt. Über diese Panels zeigte 007 hohe Breite und Potenz und übertraf oft klassische, auf V3 zielende Antikörper und setzte sich klar gegen einen kürzlich beschriebenen Antikörper durch, der eine ähnliche Region erkennt. Bemerkenswerterweise blieb 007 gegen viele Viren wirksam, die bereits einem führenden V3-Antikörper durch Veränderung der N332-Stelle entkommen waren. Umgekehrt wurden Viren, die gegen 007 resistent waren, häufig von diesen klassischen Antikörpern neutralisiert. Als das Team Kombinationen modellierte und experimentell testete, passte 007 besonders gut zu dem Antikörper 10-1074 und erzielte deutlich verbesserte Abdeckung und geringere für die Neutralisation benötigte Konzentrationen.
007 in lebenden Organismen auf die Probe gestellt
Die Forscher prüften anschließend, ob 007 eine Infektion in vivo kontrollieren kann. In humanisierten Mäusen, chronisch mit HIV-1 ADA infiziert, führte die Behandlung mit 007 zu einem raschen Abfall der Viruslast im Blut, gefolgt von einem späteren Wiederanstieg, als das Virus mutierte. Genetische Analysen zeigten, dass das Entkommen vor 007 Veränderungen in Regionen um seine neuartige Bindungsstelle beinhaltete, statt der üblichen N332-Zuckerstelle. Wichtig ist, dass Viren, die vor 007 entkamen, weiterhin empfindlich gegenüber 10-1074 blieben, und umgekehrt. Wenn beide Antikörper zusammen verabreicht wurden oder einer hinzugefügt wurde, nachdem Resistenzen gegen den anderen aufgetreten waren, hielt die Virussuppression länger an und erforderte, dass das Virus mehrere Mutationen in seiner Hülle akkumulierte, wahrscheinlich zu einem gewissen Fitnessverlust.
Warum diese Arbeit für die zukünftige HIV-Prävention wichtig ist
Indem ein Antikörper entdeckt wurde, der die V3-Region von HIV anvisiert, ohne auf das standardmäßige N332-Glykan angewiesen zu sein, erweitert diese Studie die bekannte Landschaft verwundbarer Stellen des Virus. Antikörper 007 vereint breite und potente neutralisierende Aktivität mit einem eigenständigen Fluchtmuster und kraftvoller beidhändiger Bindung und stellt damit eine vielversprechende Ergänzung für Antikörpercocktails zur Prävention, Therapie oder für funktionelle Heilungsstrategien dar. Für Impfstoffentwickler hebt 007 ein zuvor wenig genutztes Ziel auf der Virushülle hervor, das nachgeahmt werden könnte, um das Immunsystem zur Produktion ähnlicher Antikörper zu trainieren. Zusammen deuten diese Befunde darauf hin, dass ein Aufweichen unseres Fokus von einem einzigen Zucker-Hotspot hin zu einem gleichzeitigen Anvisieren benachbarter Regionen ein Schlüssel sein könnte, um HIVs Fluchtmechanismen endgültig in die Enge zu treiben.
Zitation: Gieselmann, L., DeLaitsch, A.T., Rohde, M. et al. Identification of a potent V3 glycan site broadly neutralizing antibody targeting an N332gp120 glycan-independent epitope. Nat Immunol 27, 572–585 (2026). https://doi.org/10.1038/s41590-025-02385-3
Schlüsselwörter: HIV breit neutralisierende Antikörper, V3-Glykan-Epitop, Antikörper 007, HIV-Impfstoffdesign, Antikörper-Kombinationstherapie