Clear Sky Science · de
Ingenieurbiologie der Xylosyltransferase zur Manipulation von Proteoglykanen in Säugerzellen
Warum Zellmäntel wichtig sind
Jede Zelle in unserem Körper trägt einen molekularen „Mantel“, der ihr hilft, mit Nachbarn zu kommunizieren und ihre Umgebung wahrzunehmen. Ein wesentlicher Teil dieses Mantels besteht aus Proteoglykanen — Proteinen, die mit langen Zuckerketten verziert sind und als winzige Antennen für Wachstumsfaktoren, Immun‑Signale und strukturelle Hinweise fungieren. Geht diese Zuckerdekoration schief, kann die Entwicklung gestört werden und Gewebe wie Knochen und Muskeln stark betroffen sein. Dennoch war es für Forscher schwierig, genau zuzuordnen, welche Proteine diese Ketten tragen und wie einzelne Komponenten des Mantels das Zellverhalten beeinflussen. Diese Studie stellt eine präzise chemische Strategie vor, um diese Zuckerketten an lebenden Säugerzellen zu markieren und neu aufzubauen und eröffnet damit die Möglichkeit, die auf ihren Oberflächen kodierten Informationen zu lesen und umzuschreiben. 
Die erste Stufe der Zuckeranlagerung umgestalten
Der Aufbau von Proteoglykanen beginnt, wenn eine spezielle Enzymfamilie, die Xylosyltransferasen XT1 und XT2, den ersten Zucker an ein Protein anfügt und damit die Stelle markiert, an der eine lange Kette wachsen wird. Da beide Enzyme diesen gleichen ersten Schritt ausführen können, war es schwierig zu unterscheiden, an welchen Proteinen jeweils gearbeitet wird. Die Autoren nutzten ein „Bump‑and‑hole“-Design — ein in der modernen chemischen Biologie gebräuchlicher Ansatz — um dieses Problem zu lösen. Sie formten die aktive Stelle von XT1 leicht um und schufen so zusätzlichen Raum (das „Loch“) und führten einen passenden, minimal voluminöseren Zuckerbaustein ein, 6AzGlc (der „Bump“). Die gentechnisch veränderte XT1 kann nun diesen modifizierten Zucker verwenden, während das natürliche Enzym dies nicht kann, sodass Forscher nur jene Proteine markieren können, die vom umgestalteten Enzym beeinflusst werden.
Ein Designer‑Zucker in die Zelle schmuggeln
Damit dieser Ansatz in lebenden Zellen funktioniert, musste das Team den gebumpten Zucker in einer Form liefern, die der zellulären Verstoffwechslung zugänglich ist. Anstatt sich auf normale Zuckeraufnahmewege zu verlassen — die mit Xylose‑Analoga schlecht zurechtkommen — bauten sie eine „vershlossene“ Version von 6AzGlc mit einer versteckten Phosphatgruppe. Einmal im Zytosol, machen zelluläre Enzyme diese Gruppe frei und wandeln das Molekül in UDP‑6AzGlc um, die aktivierte Form, die die ingenieurbiologischen Xylosyltransferasen benötigen. Sorgfältige Chromatographie bestätigte, dass Zellen, die mit der korrekt konfigurierten verschlossenen Verbindung behandelt wurden, beträchtliche Mengen des aktivierten Designerzuckers produzierten, während eine Spiegelbild‑Kontrolle nahezu nichts erzeugte. 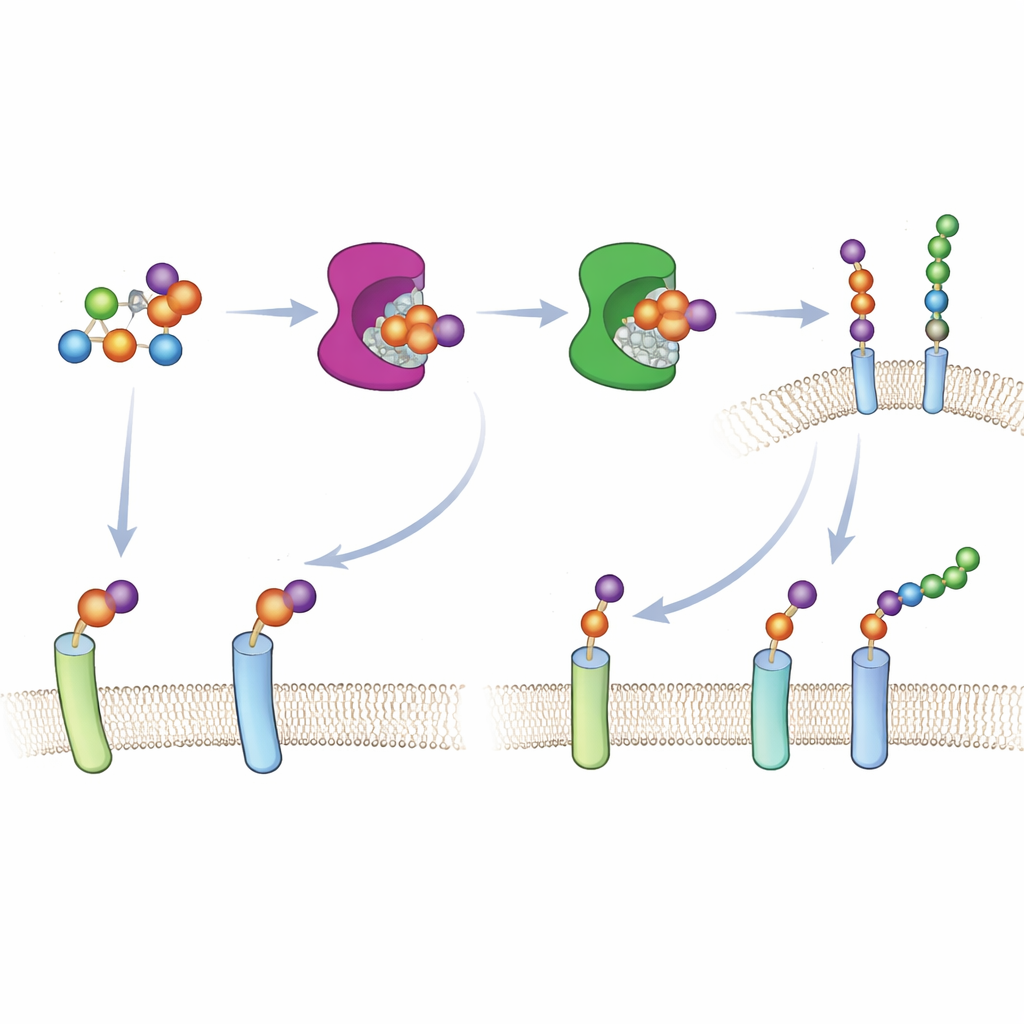
Die verborgenen Akteure markieren und identifizieren
Mit sowohl dem modifizierten Enzym als auch dem aktivierten Zucker zeigten die Forscher, dass nur Zellen, die die ingenieurbiologische XT1 oder XT2 exprimierten, das 6AzGlc‑Tag in ihre Oberflächen‑Proteoglykane einbauten. Die Azidgruppe an 6AzGlc dient als winziger chemischer Griff, der mittels Click‑Chemie an fluoreszierende Farbstoffe oder Biotin gekoppelt werden kann, was die Visualisierung und Anreicherung markierter Proteine ermöglicht. Massenspektrometrie an angereicherten Proben offenbarte eine umfangreiche Sammlung bekannter Proteoglykane — darunter Decorin, mehrere Glypicans, Syndecan‑4, CD44 und Versican — und bestätigte, dass das System echte zuckertragende Proteine markiert. Wichtig ist, dass die ingenieurbiologischen Enzyme die gleichen Sequenzpräferenzen wie ihre natürlichen Gegenstücke beibehielten; das bedeutet, dass das chemische Tag an authentischen Anlagerungsstellen installiert wird und nicht an neuen, künstlichen Positionen.
Designer‑Proteoglykane aufbauen
Ein unerwarteter Bonus des 6AzGlc‑Tags ist, dass es im Unterschied zum natürlichen Startzucker nicht von nachgeschalteten Enzymen zu einer voll‑langen Kette erweitert werden kann. Dadurch wird die Kette effektiv abgekappt und die Molekülstruktur, die per Massenspektrometrie analysiert werden muss, vereinfacht. Die Autoren nutzten dieses Merkmal als Werkzeug: Nachdem XT1 6AzGlc an einer natürlichen Anlagerungsstelle eingebracht hat, verwenden sie Click‑Chemie, um synthetische Heparin‑Fragmente anzukoppeln und so „Designer‑Proteoglykane“ mit präzise definierten Zuckerketten zu erzeugen. In Brustkrebszellen, die ihr eigenes Syndecan‑1 nicht besitzen, stellte das Hinzufügen solcher Designer‑Versionen das normale Ausbreiten auf einer Protein‑beschichteten Oberfläche wieder her und zeigte, dass das chemisch rekonstruierte Proteoglykan funktionell für das natürliche substituieren kann.
Was das für Biologie und Medizin bedeutet
Diese Arbeit liefert einen mächtigen Werkzeugkasten, um selektiv die Zuckerketten zu markieren und zu manipulieren, die steuern, wie Zellen kommunizieren. Indem man die Rollen von XT1 und XT2 auftrennt und nur deren direkte Ziele markiert, können Forscher nun kartieren, welche Proteoglykane in bestimmten Geweben und Krankheitszuständen aktiv sind. Die Fähigkeit, das natürliche Kettenwachstum zu stoppen und es durch maßgeschneiderte Zucker zu ersetzen, erlaubt es zudem, zu untersuchen, wie viel der Funktion eines Proteoglykans vom Proteinrückgrat gegenüber seinem Zuckermantel getragen wird. Langfristig könnte eine solche präzise Ingenieurarbeit helfen, komplexe Signalvorgänge an der Zelloberfläche zu entschlüsseln und Therapien zu inspirieren, die fehlerhafte zelluläre Mäntel bei Entwicklungsstörungen, Krebs und anderen Erkrankungen reparieren oder umprogrammieren.
Zitation: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
Schlüsselwörter: Proteoglykane, Glykosaminoglykane, Xylosyltransferase, chemische Biologie, zelloberflächen‑Signalgebung