Clear Sky Science · de
Eine einzige allosterische Stelle vereint Aktivierung, Modulation und Inhibition in TRPM5
Wie ein winziger Torwächter Geschmack und Stoffwechsel formt
Welche Nahrungsmittel wir genießen und wie unser Körper Zucker verarbeitet, hängt von mikroskopischen „Torwächter“-Proteinen in unseren Zellen ab. Einer dieser Torwächter, ein Kanal namens TRPM5, hilft uns, süße, bittere und herzhafte Aromen wahrzunehmen, und unterstützt die Bauchspeicheldrüse bei der Insulinausschüttung. Diese Studie zeigt, wie eine einzelne kleine Tasche auf TRPM5 wie ein Hauptregler wirken kann: sie schaltet den Kanal ein, justiert seine Empfindlichkeit und kann ihn sogar abschalten — Einsichten, die künftige Behandlungen von Diabetes, Fettleibigkeit und Darmstörungen leiten könnten.
Ein Kanal im Kreuzungspunkt von Geschmack und Blutzucker
TRPM5 sitzt in den Membranen der Geschmackszellen auf der Zunge, der hormonproduzierenden Zellen im Darm und der insulinfreisetzenden Zellen der Bauchspeicheldrüse. Wenn der Calciumspiegel in diesen Zellen steigt, öffnet sich TRPM5 und lässt positiv geladene Ionen einströmen, was kurzzeitig die Zellspannung verändert. In den Geschmacksknospen signalisiert dieses elektrische Signal dem Gehirn, dass etwas Süßes, Bitteres oder Umami auf der Zunge ist. In der Bauchspeicheldrüse hilft es, Insulinstöße nach einer Mahlzeit feinzujustieren. Menschen und Tiere mit gestörter TRPM5-Funktion zeigen Probleme bei der Insulinausschüttung und der Blutzuckerregulation, was nahelegt, dass Medikamente, die TRPM5 ansprechen, eines Tages Stoffwechselerkrankungen helfen könnten. Bis vor Kurzem fehlten den Forschern jedoch präzise Werkzeuge, um diesen Kanal gezielt ein- oder auszuschalten.
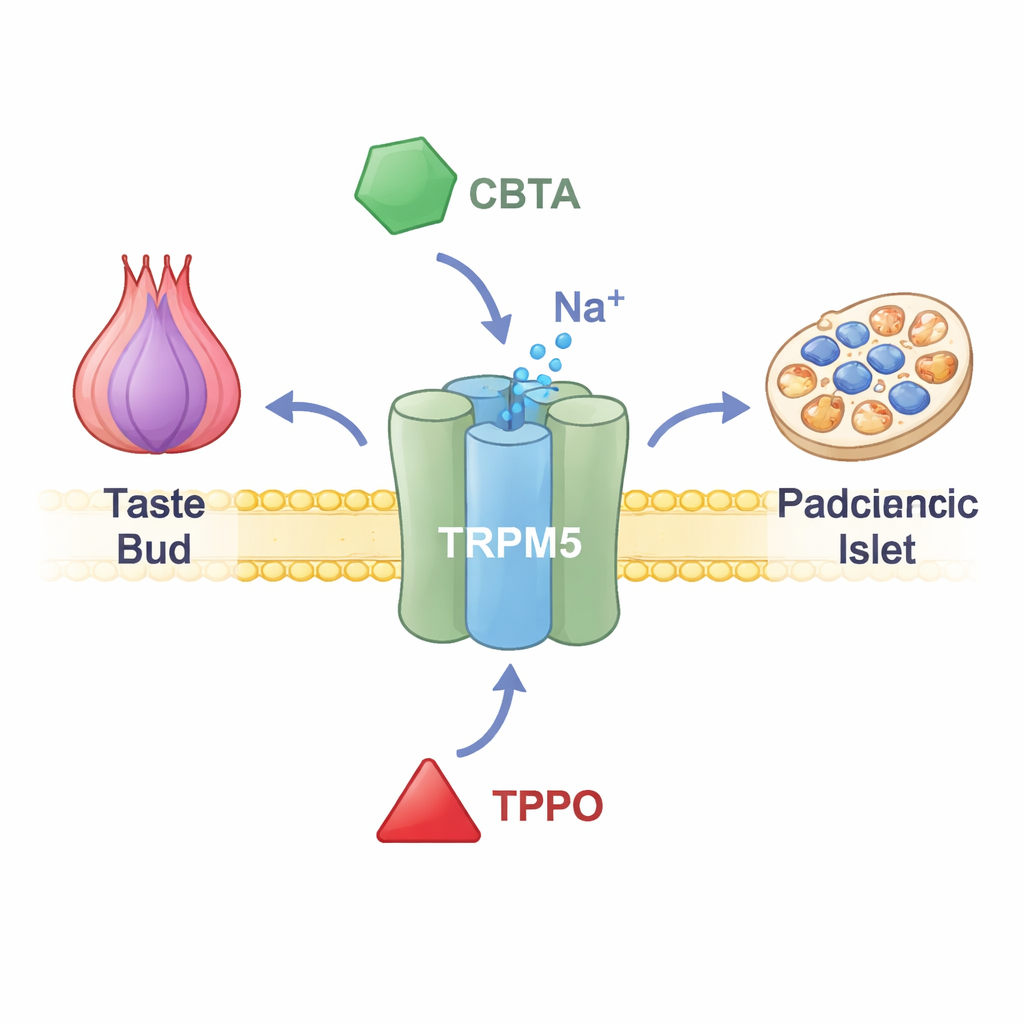
Ein neuer chemischer Schalter, der den Kanal auf Touren bringt
Die Forscher konzentrierten sich auf eine synthetische Verbindung namens CBTA, die bereits zuvor als Stimulator von TRPM5 bekannt war, aber nicht gut verstanden wurde. Mithilfe elektrischer Messungen an Zellen, die TRPM5 exprimieren, zeigten sie, dass CBTA den Kanal selbst dann öffnen kann, wenn Calcium nahezu fehlt — ein Beleg dafür, dass es als wirklicher Aktivator wirkt und nicht nur Calciums Effekte verstärkt. Bei winzigen Calciumkonzentrationen — Werten, bei denen TRPM5 normalerweise still bleibt — wirken CBTA und Calcium zusammen und erzeugen deutlich größere Ströme als jede Substanz allein. Das bedeutet, CBTA macht TRPM5 außerordentlich empfindlich, sodass nahe Ruhe-Calciumspiegel plötzlich ausreichen, um den Kanal weit zu öffnen.
Eine verborgene Kontrolltasche durch Kryo-EM aufgedeckt
Um zu sehen, wie das auf atomarer Ebene funktioniert, nutzte das Team Kryo-Elektronenmikroskopie, um dreidimensionale Schnappschüsse von TRPM5 unter verschiedenen Bedingungen einzufangen. Sie entdeckten, dass CBTA sich in eine zuvor unbemerkte Höhlung im oberen Teil einer spannungs-sensitiven Region des Kanals einfügt, direkt oberhalb der üblichen Calcium-Bindestelle. Diese Höhlung, gebildet von einer Anordnung von Aminosäuren, fungiert als präziser Andockplatz. Wenn die Wissenschaftler entscheidende Bausteine, die diese Tasche auskleiden, mutierten, konnte CBTA TRPM5 nicht mehr aktivieren, obwohl Calcium weiterhin wirkte — ein Beleg dafür, dass diese kleine Nische für die Wirkung der Verbindung essenziell ist. Auffallend ist, dass die Bindung von CBTA benachbarte Proteinabschnitte dezent umordnet und so das Greifen von Calcium an seiner üblichen Stelle erleichtert, was die starke Synergie in den elektrischen Messungen erklärt.
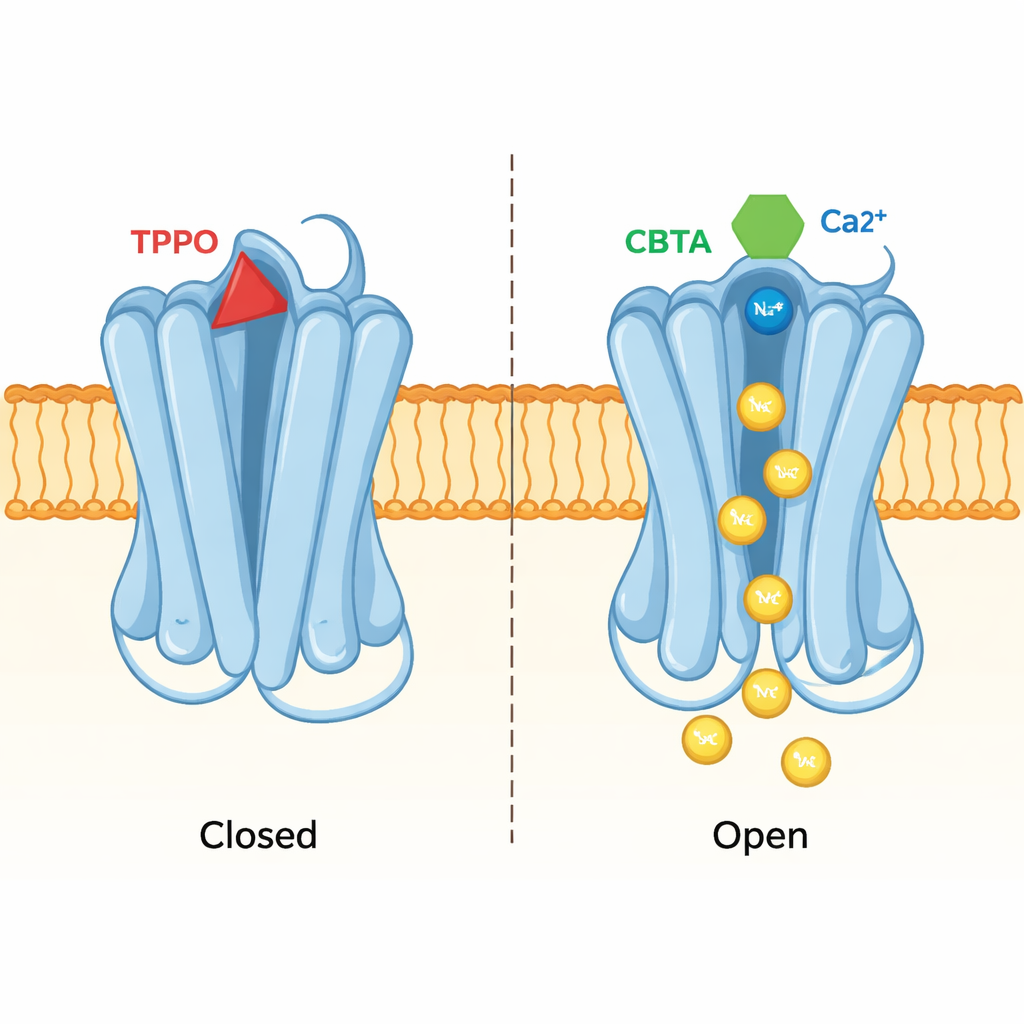
Eine Tasche, zwei gegensätzliche Wirkungen
Der gleiche strukturelle Ansatz zeigte auch, wie ein Inhibitor namens TPPO genau dieselbe Tasche nutzt, um den gegenteiligen Effekt zu erzielen. Wenn TPPO bindet, bleiben beide Calcium-Stellen an TRPM5 gefüllt, doch die zentrale Pore des Kanals bleibt zusammengedrückt und es passieren keine Ionen. Der Vergleich der TPPO- und CBTA-gebundenen Strukturen ergab, dass ihre unterschiedlichen Formen benachbarte Proteinsegmente in entgegengesetzte Richtungen drücken. CBTA fördert Bewegungen, die sich bis zur Pore fortsetzen und sie öffnen; TPPO dagegen stört die Kommunikation zwischen der Tasche und der Pore und hält das Tor geschlossen. Im Kern kann diese eine Tasche also entweder als Beschleuniger oder als Bremse fungieren, je nachdem, welches Molekül sie besetzt.
Die interne Verdrahtung des Kanals umleiten
Die Studie zeigt außerdem, dass diese Kontrolltasche Aufgaben übernehmen kann, die normalerweise von einer separaten Calcium-bindenden Region im Zellinneren ausgeführt werden. In mutierten Kanälen, bei denen die übliche interne Calciumstelle deaktiviert ist, konnte Calcium allein TRPM5 nicht öffnen. CBTA schaltete diese Mutanten jedoch weiterhin ein und veränderte ein wichtiges Strukturelement, das die inneren und äußeren Bereiche des Kanals verbindet. In anderen Mutanten, die die Verbindung zwischen Calciumbindung und Porenöffnung unterbrachen, stellte die Zugabe von CBTA das normale Verhalten wieder her. Diese Ergebnisse zeigen, dass die neu identifizierte Stelle die Kommunikation zwischen verschiedenen Kanaldomänen umleiten oder reparieren kann und als flexibler Knoten für Fernsignale innerhalb des Proteins fungiert.
Warum das für künftige Medikamente wichtig ist
Für Nicht-Spezialisten lautet die zentrale Botschaft: Die Forscher haben eine einzelne, medikamentenempfindliche Tasche auf TRPM5 entdeckt, die Aktivierung, Feinabstimmung und Abschaltung integrieren kann. Ein kleiner Aktivator wie CBTA kann sowohl Calcium nachahmen als auch die Empfindlichkeit des Kanals stark erhöhen, während eine andere Verbindung, TPPO, denselben Kanal durch Andocken an derselben Stelle fest verschließen kann. Dieses einheitliche Bild der TRPM5-Kontrolle eröffnet die Möglichkeit, gezielt Moleküle zu entwerfen, die seine Aktivität in bestimmten Geweben entweder steigern oder dämpfen — mit potenziellen Anwendungen von verbesserten geschmacksbasierten Therapien und Medikamenten zur Darmmotilität bis hin zu neuen Strategien zur Blutzucker- und Stoffwechselregulation.
Zitation: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
Schlüsselwörter: TRPM5-Kanal, Geschmackswahrnehmung, Insulinausschüttung, Ionenkanal-„Gating“, allosterische Modulation