Clear Sky Science · de
CDK4/6‑Hemmung mindert die durch Chemotherapie bedingte Ausbreitung von TP53‑mutiertem klonalem Hämatopoese
Warum es wichtig ist, das Blut vor Krebstherapie zu schützen
Chemotherapie kann Leben retten, trifft aber auch das Knochenmark, in dem neue Blutzellen entstehen. Bei manchen Menschen fördert diese Schädigung unbeabsichtigt das Auftreten seltener, bereits vorhandener mutierter Blutstammzellen, die sich dann ausbreiten und später zu aggressiven Blutkrebserkrankungen führen können. Diese Studie stellt eine hoffnungsvolle Frage: Lässt sich ein kurzzeitiges "Pauseknopf"‑Medikament für Blutstammzellen einsetzen, um sie während der Chemotherapie zu schützen und damit das Wachstum dieser riskanten mutierten Klone zu verlangsamen, ohne die Wirksamkeit der Krebsbehandlung zu beeinträchtigen?
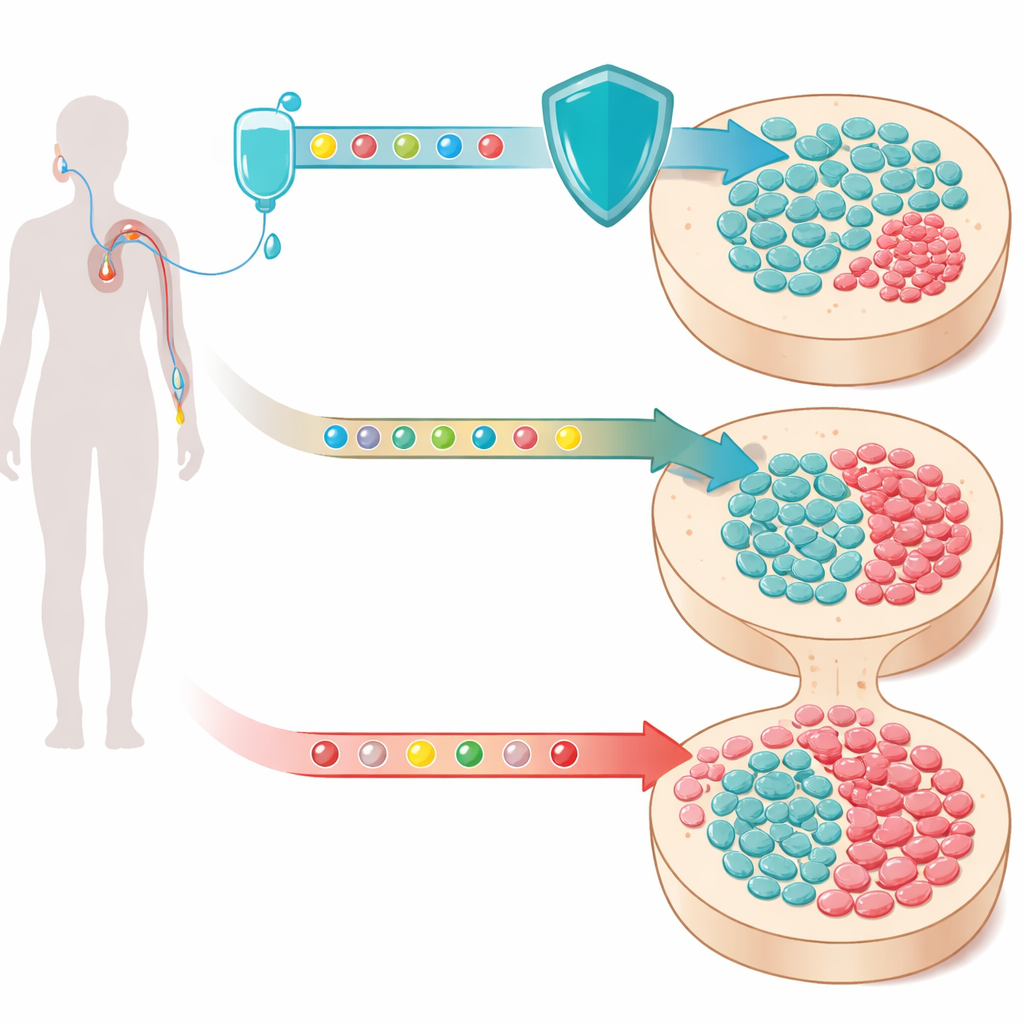
Verborgene Klone im Blut
Mit dem Alter sammeln unsere blutbildenden Stammzellen langsam DNA‑Veränderungen an. Die meisten dieser veränderten Zellen bleiben harmlos, doch einige gewinnen einen Wachstums‑Vorteil und bilden kleine Klone—Ansammlungen genetisch gleicher Zellen—im Blutkreislauf. Dieses Phänomen, klonale Hämatopoese genannt, ist bei älteren Erwachsenen überraschend häufig. Betrifft die Veränderung das TP53‑Gen oder andere Gene der DNA‑Schadensantwort, sind diese Klone besonders bedenklich: Sie überleben Stress, der normale Zellen tötet, und stehen in engem Zusammenhang mit therapiebedingten myeloischen Neoplasien, einer Gruppe oft tödlicher Blutkrebserkrankungen, die Jahre nach einer Chemotherapie auftreten können.
Die Stammzellen während der Chemotherapie auf Pause setzen
Die Forschenden konzentrierten sich auf Wirkstoffe, die CDK4/6 blockieren — Schlüsseltreiber, die die Zellteilung vorantreiben. Ein solcher Wirkstoff, Trilaciclib, ist bereits zugelassen, um niedrige Blutwerte bei bestimmten Lungenkrebspatienten zu verringern. Kurz vor der Chemotherapie verabreicht, bringt er Knochenmark‑Stamm‑ und Vorläuferzellen in einen ruheähnlichen Zustand. Das Team nahm an, dass, wenn sowohl gesunde als auch TP53‑mutierte Stammzellen bei Beginn der Chemotherapie weniger aktiv sind, den Mutanten ein Großteil ihres sonstigen Überlebensvorteils verloren geht, weil weniger Zellen—normal oder mutiert—gerade in Teilung sind, wenn DNA‑schädigende Mittel am toxischsten wirken.
Hinweise aus klinischen Studien und Tiermodellen
Um die Idee bei echten Patientinnen und Patienten zu prüfen, analysierte die Gruppe Blutproben aus vier randomisierten klinischen Studien bei Menschen, die eine Chemotherapie gegen kleinzelligen Lungenkrebs, metastasierten Darmkrebs und triple‑negativen Brustkrebs erhielten. In jeder Studie wurden die Teilnehmenden zufällig zu Standardchemotherapie mit entweder Trilaciclib oder Placebo zugeteilt. Mit ultratiefer DNA‑Sequenzierung von Blutzellen zu Behandlungsbeginn und nach mehreren Zyklen verfolgten die Wissenschaftler, wie sich bekannte mutierte Klone im Verlauf veränderten. In allen Studien expandierten Klone mit Mutationen in DNA‑Schadensantwort‑Genen—insbesondere TP53 und PPM1D—während der Chemotherapie, doch in denjenigen, die Trilaciclib erhalten hatten, wuchsen diese Klone deutlich langsamer. Im Durchschnitt wurde die Wachstumsrate dieser riskanten Klone um etwa ein Drittel reduziert, während häufige altersbedingte Mutationen in anderen Genen weitgehend unbeeinflusst blieben.
Ein Blick darauf, wie der Schutz wirkt
Da die Nachbeobachtung der Patientinnen und Patienten noch relativ kurz ist, griff das Team auf Mausmodelle zurück, um zu untersuchen, wie die CDK4/6‑Blockade das Knochenmark während der Behandlung umgestaltet. Sie erzeugten Mäuse, deren Blut‑System einen kleinen Anteil Trp53‑mutierter Stammzellen enthielt, um die menschliche klonale Hämatopoese zu imitieren. Erhielten diese Mäuse nur platinbasierte Chemotherapie, setzten sich die mutierten Zellen sowohl im Blut als auch im Mark schnell gegen ihre normalen Nachbarn durch. Wurde hingegen kurz vor jeder Chemotherapiedosis Trilaciclib—oder ein anderer CDK4/6‑Hemmer, Palbociclib—verabreicht, wurde diese Übernahme durch die Mutanten nahezu vollständig verhindert. Detaillierte Einzelzell‑RNA‑Sequenzierungen zeigten, dass CDK4/6‑Hemmung Stamm‑ und Vorläuferzellen in einen ruhigeren, weniger proliferativen Zustand drängte, ein "Stemness"‑Genprogramm reduzierte, das langlebige mutierte Zellen begünstigt, die Differenzierung von myeloiden in lymphoide Linien verschob und selektiv programmierte Zellsterbewege in Trp53‑mutierten Stammzellen auslöste, während normale Zellen geschont blieben.
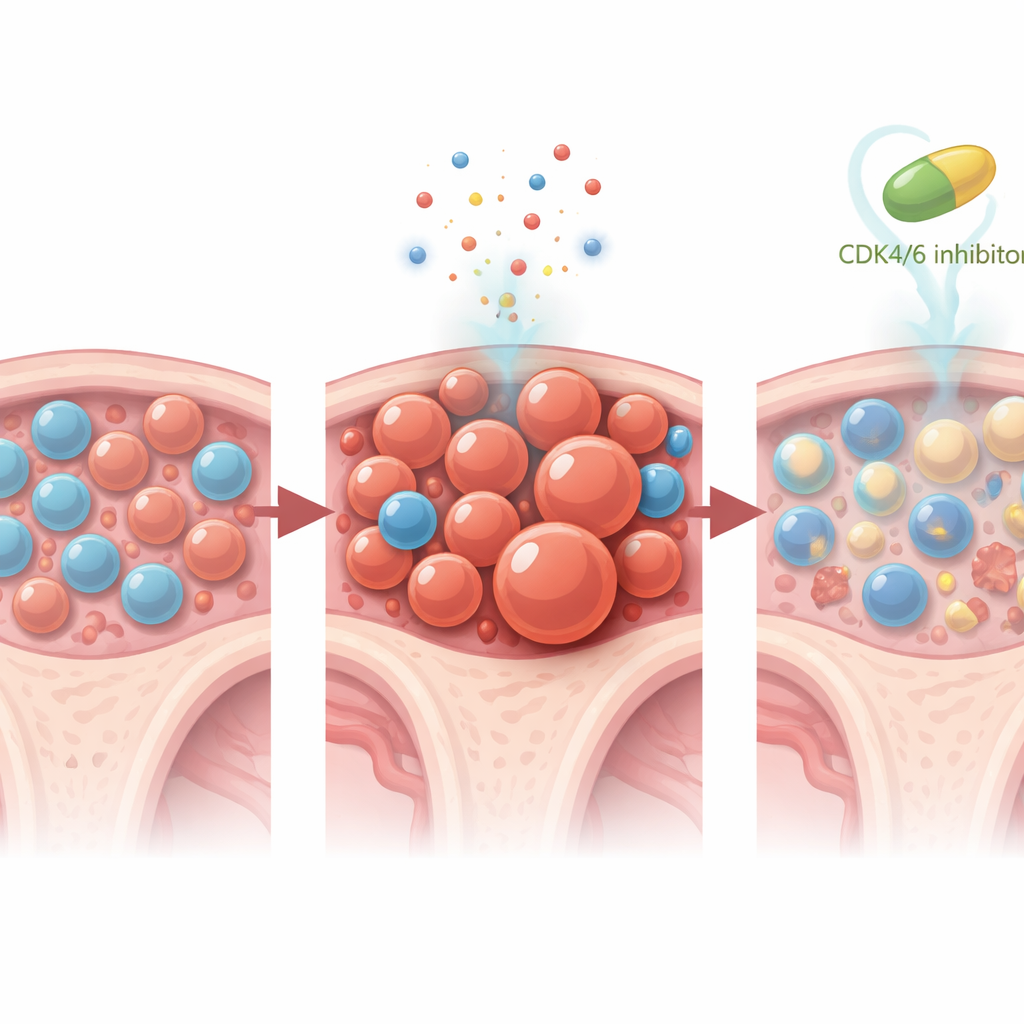
Dauerhafte Wirkung und künftige Richtungen
Ein bemerkenswertes Maus‑Experiment deutete darauf hin, dass schon ein kurzer Kurs mit CDK4/6‑Hemmung dauerhafte Effekte haben kann: Zwei Wochen Trilaciclib, verabreicht rund um die Chemotherapie, verhinderten die Expansion von Trp53‑mutierten Klonen für mindestens sechs Wochen nach Ende aller Behandlungen. Wichtig ist, dass Blutwerte und die allgemeine Gesundheit des Markes akzeptabel blieben, was darauf hinweist, dass diese Schutzstrategie nicht einfach eine Toxizität gegen eine andere eintauscht. Obwohl bei keinem der Studienteilnehmenden während der begrenzten Nachbeobachtungszeit eine Blutkrebserkrankung auftrat, stützt das Vorhandensein und die verlangsamte Ausbreitung sehr kleiner TP53‑mutierter Klone die Idee, dass dies ein früher, modifizierbarer Schritt auf dem Weg zur therapiebedingten Leukämie ist.
Was das für Krebspatientinnen und -patienten bedeuten könnte
Für Patientinnen und Patienten, die bereits hochriskante Blutklone tragen, bestand die Befürchtung, dass die notwendige Chemotherapie zur Kontrolle ihres soliden Tumors auch die Saat für eine zukünftige, oft schwer behandelbare Leukämie legt. Diese Arbeit liefert einen Machbarkeitsnachweis dafür, dass zeitlich präzise eingesetzte CDK4/6‑Hemmer den Wachstums‑Vorteil dieser gefährlichen Klone abschwächen können, indem sie das Knochenmark während der Chemotherapie kurzzeitig schützen. Längere und größere klinische Studien sind erforderlich, um wirklich zu belegen, dass diese Strategie die Häufigkeit therapiebedingter Blutkrebserkrankungen senkt, doch sie weist in eine Zukunft, in der wir den Primärtumor aggressiv behandeln und gleichzeitig das blutbildende System vor langfristigen genetischen Schäden schützen können.
Zitation: Chan, I.C.C., Zhang, P., Pan, X. et al. CDK4/6 inhibition mitigates chemotherapy-induced expansion of TP53-mutant clonal hematopoiesis. Nat Genet 58, 582–592 (2026). https://doi.org/10.1038/s41588-026-02526-w
Schlüsselwörter: klonale Hämatopoese, TP53‑Mutationen, Nebenwirkungen der Chemotherapie, CDK4/6‑Hemmer, therapiebedingte Leukämie