Clear Sky Science · de
Genomweite Assoziationsanalysen der Autoimmunhypothyreose zeigen autoimmune und schilddrüsenspezifische Beiträge und eine inverse Beziehung zum Krebsrisiko
Warum das für die tägliche Gesundheit wichtig ist
Viele Menschen fühlen sich müde, frieren oder sind geistig benebelt, ohne zu bemerken, dass ihre Schilddrüse die Ursache sein könnte. Die Autoimmunhypothyreose, bei der die körpereigenen Abwehrkräfte die Schilddrüse langsam angreifen, betrifft mehr als jeden zwanzigsten Menschen. Diese Studie nutzt genetische Daten von Hunderttausenden Freiwilligen, um zwei große Fragen zu klären: Welche vererbten Veränderungen in unserer DNA erhöhen die Wahrscheinlichkeit für diese Erkrankung, und wie hängen diese Veränderungen mit dem Krebsrisiko zusammen? Die Antworten zeigen einen überraschenden Zielkonflikt: ein Immunsystem, das einerseits der Schilddrüse schadet, andererseits aber zusätzlichen Schutz vor Tumoren bieten kann.
Ein Blick über das gesamte Genom
Die Forschenden kombinierten Gesundheitsdaten und genetische Informationen aus zwei großen Bevölkerungsprojekten, FinnGen in Finnland und dem UK Biobank im Vereinigten Königreich. Sie konzentrierten sich auf Personen, die eine langfristige Schilddrüsenhormon-Ersatztherapie benötigten, und schlossen sorgfältig jene aus, deren Schilddrüsenprobleme durch Operation, Krebs oder andere nicht-autoimmune Ursachen bedingt waren. So entstanden mehr als 81.000 Fälle von Autoimmunhypothyreose und über 700.000 Kontrollen – die bislang größte Studie zu dieser Erkrankung. Beim Durchsuchen von Millionen von DNA-Markern im gesamten Genom identifizierten sie 418 unabhängige genetische Signale außerhalb des großen Immungenlusters, verteilt auf mindestens 280 Regionen des Genoms. Viele dieser Signale betrafen seltene oder niedrigfrequente DNA-Veränderungen, die die Struktur von Proteinen verändern und damit direkte Hinweise auf die zugrundeliegende Biologie liefern.
Allgemeine Immunwirkung von schilddrüsenspezifischen Effekten trennen
Die Autoimmunhypothyreose liegt an der Schnittstelle zwischen allgemeiner Autoimmunität und der spezifischen Biologie der Schilddrüse. Um diese Komponenten zu trennen, verglich das Team seine Ergebnisse mit genetischen Studien anderer Autoimmunerkrankungen und mit Blutwerten des schilddrüsenstimulierenden Hormons (TSH), dem wichtigsten klinischen Marker zur Erkennung einer Unterfunktion der Schilddrüse. Mithilfe einer bayesianischen Klassifikationsmethode gruppierten sie genetische Signale in solche, die mit breiten Autoimmunerkrankungen geteilt werden, und solche, die eher spezifisch die Schilddrüsenhormonregulation betreffen. Sie schätzten, dass etwa 38 % der Signale über allgemeine Immunwege wirken, die viele Autoimmunerkrankungen beeinflussen, während etwa 20 % vorwiegend über die Schilddrüsenfunktion wirken. Die schilddrüsenfokussierten Varianten beeinflussten tendenziell Hormonwerte und Gene, die in Schilddrüsengewebe aktiv sind, während die allgemeinen Immunvarianten stärker in T-Zellen aktiv waren, den weißen Blutkörperchen, die Immunantworten steuern.
Fokussierung auf einen wichtigen Immun-Schalter
Ein besonders auffälliger Befund betraf eine seltene DNA-Veränderung im Gen ZAP70, das ein zentrales Signalisierungsprotein in T-Zellen kodiert. Schwere Defekte dieses Proteins sind bekannt dafür, tiefgreifende Immundefizienz zu verursachen, doch die hier identifizierte Variante führt nur zu einem partiellen Funktionsverlust. Laborversuche in gentechnisch veränderten T-Zellen zeigten, dass dieses veränderte ZAP70 die Signalkaskade nach der Erkennung eines Ziels abschwächt, sie aber nicht vollständig blockiert. Zellen mit der Variante waren weniger in der Lage, Aktivierungsmarker und nachgeschaltete Signalschritte einzuschalten. Diese abgeschwächte Reaktion scheint das empfindliche Gleichgewicht zu stören, das normalerweise selbstreaktive T-Zellen entfernt, wodurch Träger anfälliger für Autoimmunerkrankungen werden, gleichzeitig aber ihr Risiko für bestimmte Immundefizite leicht erhöht ist.
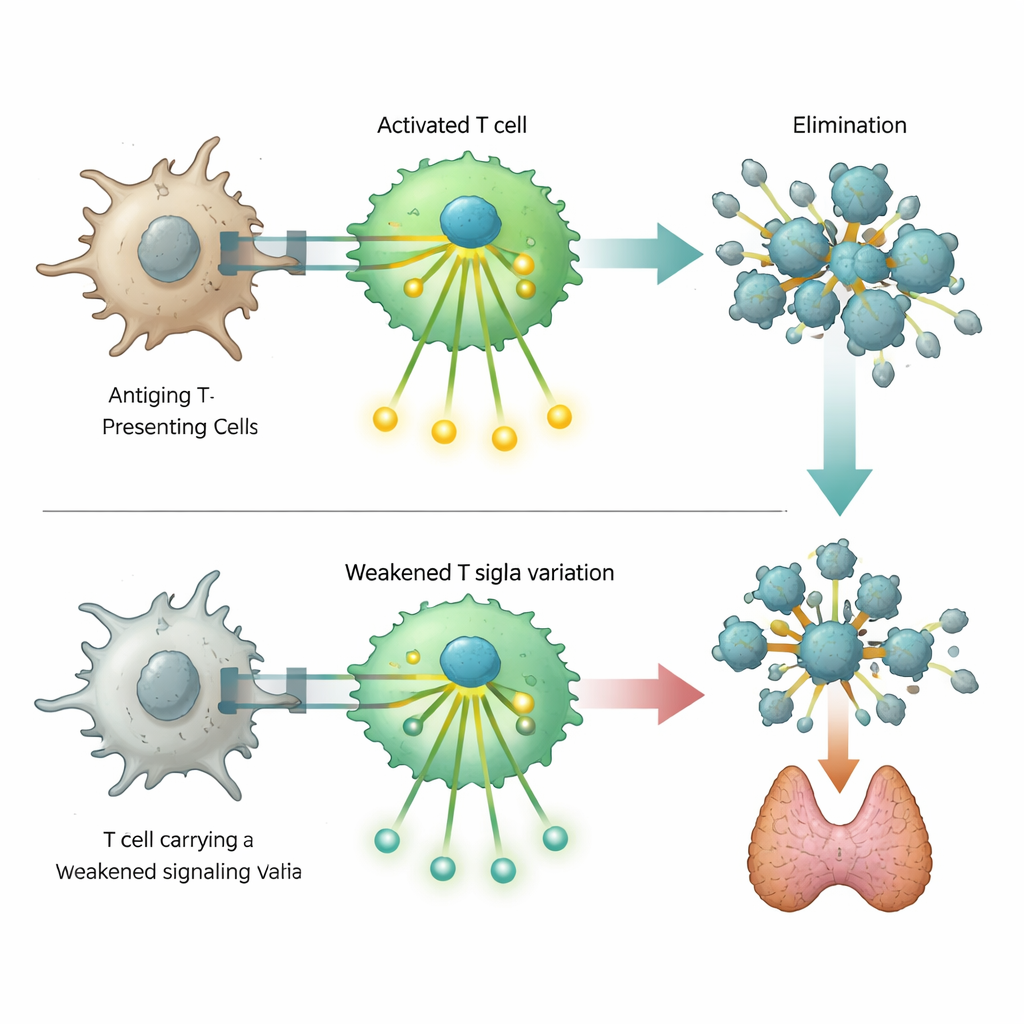
Eine unerwartete Verbindung zum Krebsschutz
Da dieselben Immunwege, die Autoimmunität antreiben, auch Tumore angreifen können, prüften die Autorinnen und Autoren anschließend, wie die Genetik der Autoimmunhypothyreose mit dem Krebsrisiko zusammenhängt. Sie berechneten einen polygenen Risikoscore, der die vererbte Neigung zu Hypothyreose zusammenfasst, und testeten dessen Assoziation mit vielen Krankheiten in den finnischen Daten. Wie erwartet korrelierte ein höherer Score mit einem höheren Risiko für verschiedene Autoimmunerkrankungen. Überraschender war ein konsistentes Muster eines niedrigeren Risikos für mehrere Krebsarten, insbesondere Basalzellkarzinom und andere Hautkrebse, aber auch Brust- und Prostatakrebs sowie eine allgemeine Kategorie „alle Krebserkrankungen“. Beim direkten Vergleich mit genomweiten Krebsstudien beeinflussten etwa 10 % der hypothyreose-assoziierten Stellen auch Hautkrebs, wobei dieselbe genetische Variante in der Regel die Schilddrüsenautoimmunität erhöhte und gleichzeitig das Hautkrebsrisiko senkte. Diese gemeinsamen Varianten konzentrierten sich auf immunbezogene Gene, einschließlich bekannter Arzneimittelziele, die in der Checkpoint-Immuntherapie verwendet werden.
Was das für Patientinnen, Patienten und die Medizin bedeutet
Aus einer allgemein verständlichen Perspektive zeigt diese Arbeit, dass manche Menschen mit einem leicht „heißer eingestellten“ Immunsystem geboren werden: Sie sind anfälliger für langsame, oft stille Schäden an der Schilddrüse, verfügen gleichzeitig aber über eine bessere Fähigkeit, entstehende Krebszellen zu erkennen und zu eliminieren. Die Studie trennt, welche genetischen Veränderungen über allgemeine Immunüberaktivität wirken und welche speziell die Schilddrüsenhormonproduktion beeinflussen, und erklärt so, warum Erkrankungen wie Hashimoto und Morbus Basedow manche Risikogene teilen, aber die Schilddrüsenfunktion in entgegengesetzte Richtungen beeinflussen können. Sie hilft auch zu verstehen, warum Patientinnen und Patienten, die während einer immunsteigernden Krebsbehandlung Schilddrüsenprobleme entwickeln, oft besser auf diese Therapien ansprechen. Insgesamt deuten die Ergebnisse darauf hin, dass verbreitete, natürliche Varianten in Immun-Checkpoint- und Signalisierungsgenen sowohl Autoimmunerkrankungen der Schilddrüse als auch das lebenslange Krebsrisiko mitgestalten und neue Ansätze für Prävention und eine individuellere Nutzung von Immuntherapien bieten.
Zitation: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
Schlüsselwörter: autoimmune Hypothyreose, Schilddrüsenerkrankung, genetisches Risiko, Immunsystem, Krebsschutz