Clear Sky Science · de
Genomeweite Assoziationsanalysen heben die Rolle der molekularen Darmumgebung für die Variation der menschlichen Darmmikrobiota hervor
Warum Ihre DNA und Darmbakterien zur gleichen Geschichte gehören
Billionen von Mikroben leben in unserem Darm und beeinflussen alles von der Verdauung über den Stoffwechsel bis hin zum Immunsystem. Aber warum tragen einige Menschen von Natur aus andere Mischungen von Darmbakterien als andere, selbst wenn sie am gleichen Ort leben und ähnliche Nahrung zu sich nehmen? Diese Studie, basierend auf detaillierten genetischen und mikrobiellen Daten von fast 30.000 Erwachsenen in Schweden und Norwegen, zeigt, dass unsere eigene DNA leise mitschreibt, welche mikrobielle Gemeinschaft in uns lebt.
Ein umfangreicher Blick in nordische Därme
Um aufzudecken, wie menschliche Gene das Mikrobiom formen, kombinierten die Forschenden Daten aus vier großen schwedischen Bevölkerungsstudien mit 16.017 Erwachsenen und prüften ihre Ergebnisse in 12.652 Norwegern. Alle Teilnehmenden stellten Blut für die Analyse der menschlichen DNA sowie Stuhlproben für eine tiefgehende Sequenzierung mikrobieller DNA bereit. Anstatt sich nur auf große Bakteriengruppen zu konzentrieren, nutzte das Team hochauflösende Methoden, die Hunderte einzelner Arten unterscheiden können. Anschließend durchsuchten sie das menschliche Genom, Variante für Variante, um herauszufinden, welche DNA-Abschnitte mit der gesamten mikrobiellen Vielfalt (wie viele verschiedene Arten vorhanden sind) und mit dem Vorkommen oder der Häufigkeit bestimmter bakterieller Arten zusammenhängen.
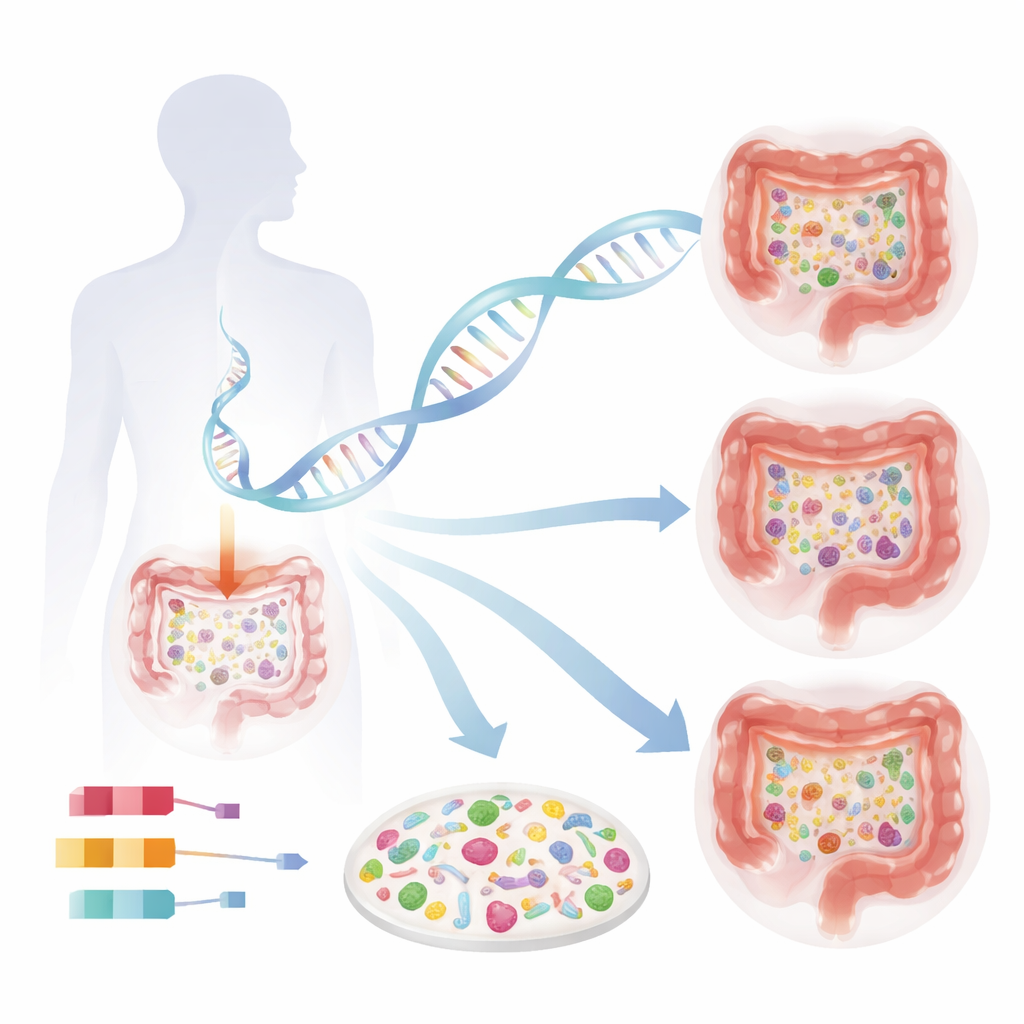
Genetische Schalter, die die mikrobielle Vielfalt steuern
Einer der auffälligsten Befunde war ein Abschnitt des menschlichen Genoms mit zwei Genen, OR51E1 und OR51E2, die zuvor als Geruchsrezeptoren bekannt waren. Diese Rezeptoren sitzen auch auf speziellen hormonproduzierenden Zellen der Darmschleimhaut und nehmen Fettsäuren wahr, die von Mikroben hergestellt werden. Personen, die eine bestimmte Version dieses DNA-Abschnitts tragen, hatten tendenziell weniger Bakterienarten im Darm, und dieses Muster wurde unabhängig in der norwegischen Gruppe bestätigt. Der Befund deutet darauf hin, dass die Art und Weise, wie unsere Darmzellen mikrobenproduzierte Fettsäuren wahrnehmen, rückwirkend die Diversität des Mikrobioms beeinflusst — möglicherweise durch Veränderungen von Darmhormonen, die Motilität, Appetit oder lokale Immunantworten steuern.
Oberflächensugare, Schleim und die mikrobielle Nachbarschaft
Die Studie identifizierte außerdem mehrere genetische Regionen, die die zuckerreiche und schleimige Umgebung an der Darmoberfläche steuern — erstklassiger Lebensraum für Bakterien. Varianten im bekannten Laktasegen (LCT), der bestimmt, ob Erwachsene Milchzucker verdauen können, waren mit Verschiebungen bei mehreren Arten verknüpft, darunter Bifidobacterium, das von Laktose profitiert. Gene, die Blutgruppen und den damit verbundenen „Secretor“-Status definieren — ABO, FUT2 und FUT3–FUT6 — verändern fucosereiche Zucker, die auf dem Darmmukus und in Sekreten präsentiert werden. Unterschiedliche genetische Kombinationen hier wurden mit charakteristischen Bakteriensets assoziiert, die an diese Zucker andocken oder sich davon ernähren können. Eine weitere Schlüsselregion lag in einem Mucin-Gen, MUC12, das zur Gerüststruktur der Schleimschicht beiträgt. Veränderungen in dieser Region korrelierten mit der Häufigkeit der Art Coprobacillus cateniformis und zeigten sogar ein gemeinsames genetisches Signal mit der Häufigkeit der Darmentleerung, was auf verflochtene Effekte von Darmfunktion und mikrobieller Zusammensetzung hinweist.
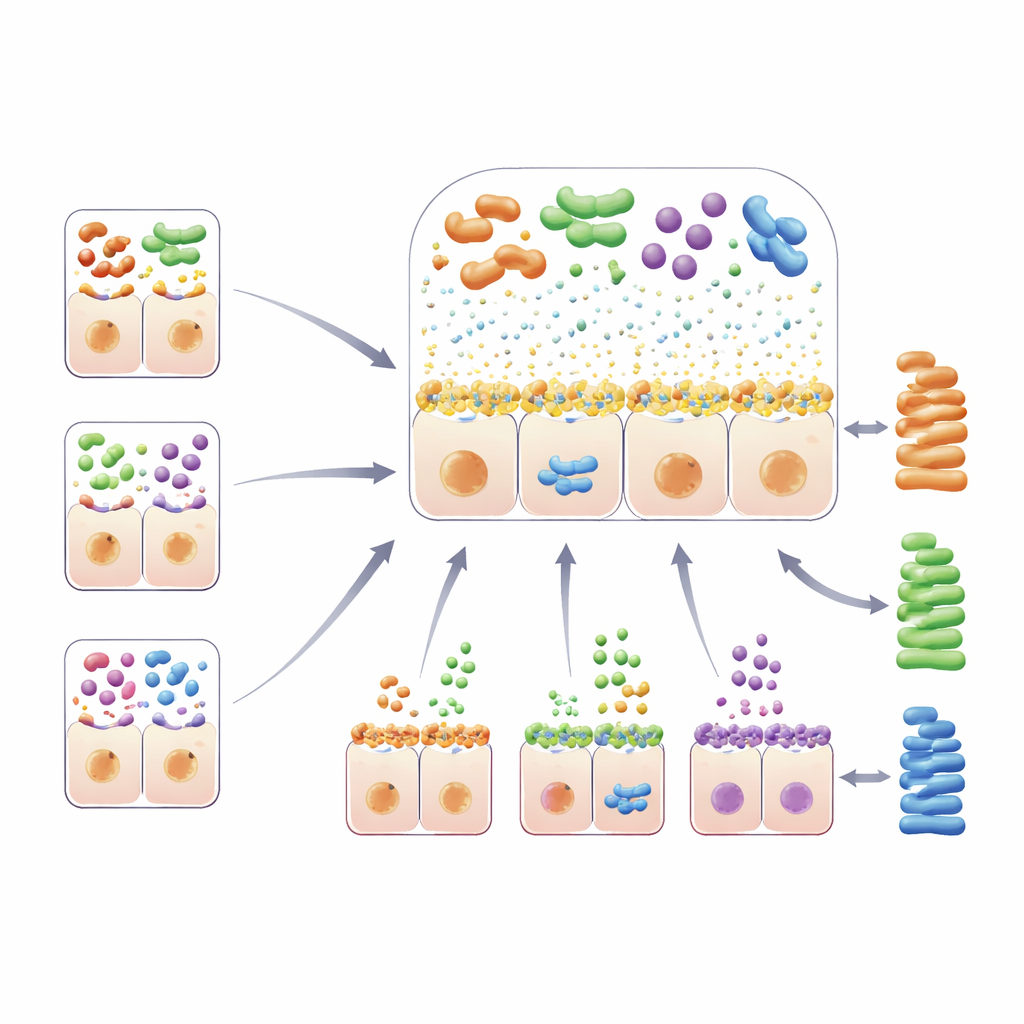
Von Mikroben zu Stoffwechsel und Körperform
Über die Kartierung „wer dort lebt“ hinaus fragten die Forschenden, ob DNA-Regionen, die mit bestimmten Bakterien in Verbindung stehen, auch mit menschlichen Merkmalen wie Blutcholesterin, Gallensäuren und Fettverteilung zusammenfallen. In mehreren Fällen waren dieselben Genomabschnitte beteiligt. Varianten in der Nähe der Gene CORO7–HMOX2 und FOXP1 beeinflussten einen Bakteriencluster, darunter Turicibacter und Clostridium saudiense, und stimmten außerdem mit Unterschieden im Taille-Hüft-Verhältnis, bei Gallensäuren und LDL-Cholesterin überein. Mithilfe genetischer Werkzeuge, die Ursache und Wirkung nahelegen sollen, fanden die Autorinnen und Autoren Hinweise darauf, dass ein Mikroorganismus der Gattung Intestinibacter das LDL-Cholesterin erhöhen könnte und dass Turicibacter die Speicherung von Körperfett beeinflussen könnte. Eine weitere Region, SLC5A11, war mit einem Butyrat-produzierenden Bakterium, Agathobaculum butyriciproducens, verbunden, das in Tiermodellen für Gehirnerkrankungen schützende Effekte gezeigt hat. In diesem Fall schien die menschliche DNA-Variante die Blutspiegel eines kleinen Moleküls namens Myo-Inositol zu senken und gleichzeitig das Wachstum dieses potenziell nützlichen Mikroben zu begünstigen.
Was das für Gesundheit und künftige Therapien bedeutet
Zusammengefasst zeigen diese Ergebnisse, dass menschliche Gene, die an Darmwahrnehmung, Schleimzusammensetzung und Oberflächenzuckern beteiligt sind, mitbestimmen, welche mikrobiellen Arten sich erfolgreich in unserem Darm ansiedeln können. Die Effekte sind für ein einzelnes Gen modest, und das Bild ist bislang am deutlichsten für relativ häufige Bakterien bei Menschen europäischer Abstammung. Dennoch erweitert die Arbeit die Liste der menschlichen DNA-Regionen, die zuverlässig mit spezifischen Darmmikroben verknüpft sind, von nur wenigen auf mindestens acht und verknüpft mehrere davon mit metabolischen Merkmalen wie Cholesterin und Körperfettverteilung. Für eine interessierte Leserschaft lautet die Kernbotschaft: Das Darmmikrobiom wird nicht nur durch Ernährung und Umgebung geformt — unser eigener genetischer Bauplan gestaltet den Lebensraum, dem Mikroben begegnen, und lenkt die Gemeinschaft hin zu bestimmten Bewohnern und weg von anderen. Wenn größere und vielfältigere Studien folgen, könnte das Verständnis dieser Wechselbeziehung zwischen Genen und Mikroben helfen, Ernährungsempfehlungen zu personalisieren, Krankheitsrisiken vorherzusagen und möglicherweise Therapien zu entwickeln, die Medikamente, Ernährung und gezielte Beeinflussung des Mikrobioms kombinieren.
Zitation: Dekkers, K.F., Pertiwi, K., Baldanzi, G. et al. Genome-wide association analyses highlight the role of the intestinal molecular environment in human gut microbiota variation. Nat Genet 58, 540–549 (2026). https://doi.org/10.1038/s41588-026-02512-2
Schlüsselwörter: Darmmikrobiom, menschliche Genetik, Darmmukus, Gallensäuren, Stoffwechsel