Clear Sky Science · de
GGC-Wiederholungsexpansionen in neuen offenen Leseraster werden in toxische Polyglycin-Proteine bei okulopharyngodistaler Myopathie übersetzt
Verborgene Botschaften in unserer DNA
Die meisten von uns lernten in der Schule, dass nur ein kleiner Teil unserer DNA tatsächlich für Proteine kodiert, während der Rest einst als „Junk“ abgetan wurde. Diese Studie kehrt diese Vorstellung um. Sie zeigt, dass kleine, übersehene Abschnitte repetitiver DNA heimlich neue Proteine hervorbringen können, die Muskeln und Gehirn schädigen. Das hilft, eine Gruppe seltener, aber verheerender neurologischer Erkrankungen zu erklären — und weist auf einen möglichen Behandlungsansatz hin.
Repetitive DNA und mysteriöse Muskelerkrankungen
Unser Genom ist voller winziger, wiederholter Sequenzen, ähnlich dreibuchstabigen Silben, die immer wieder vorkommen. Wenn einige dieser Wiederholungen zu lang werden, können sie mehr als 60 bekannte menschliche Krankheiten verursachen. Bei der okulopharyngodistalen Myopathie (OPDM) und einer verwandten Störung mit Hirnveränderungen, OPML, entwickeln Betroffene hängende Augenlider, Schluckstörungen, Schwäche in Händen und Füßen und mitunter weiterreichende Nerven- und Hirnprobleme. Unter dem Mikroskop sehen Ärzte charakteristische Proteinanhäufungen in Muskel- und Nervenzellen, doch bislang war unklar, wie Wiederholungen in vermeintlich „nichtkodierenden“ Bereichen der DNA toxische Proteine erzeugen können.
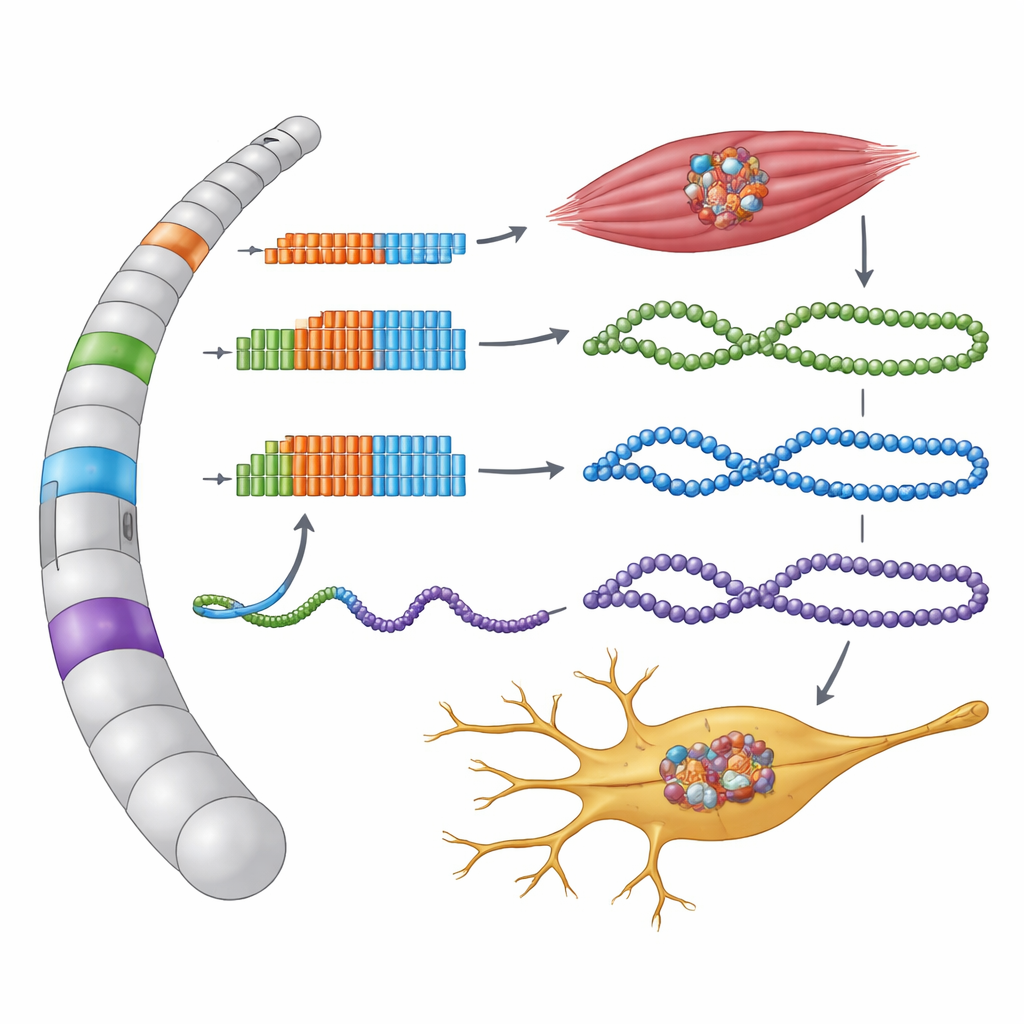
Nichtkodierende Regionen, die heimlich Protein herstellen
Die Forschenden konzentrierten sich auf DNA-Regionen, in denen die dreibuchstabige Sequenz GGC innerhalb mehrerer mit OPDM und OPML verknüpfter Gene viele Male wiederholt vorkommt. Diese Wiederholungen liegen in Bereichen, die als nichtkodierend annotiert sind — unveränderte Enden von Genen oder lange RNAs, denen keine Proteinsynthese zugetraut wurde. Durch das Nachbilden dieser menschlichen Sequenzen in Zellen und das Verfolgen ihrer Ablesung entdeckte das Team, dass jede GGC-Region tatsächlich in einer winzigen, zuvor nicht erkannten proteinkodierenden Einheit liegt, einem kleinen offenen Leserahmen. Wenn Zellen diese versteckten Anweisungen ablesen, wird jede GGC-Wiederholung in die Aminosäure Glycin übersetzt und bildet ungewöhnlich lange „Polyglycin“-Schwänze an neuen Mikroproteinen.
Neue toxische Proteine, die verklumpen und Zellen töten
Mithilfe eigens hergestellter Antikörper zeigten die Wissenschaftler, dass diese Polyglycin-haltigen Mikroproteine in Muskelproben von Patientinnen und Patienten vorhanden sind und genau dort konzentriert auftreten, wo die ungewöhnlichen p62-positiven Proteinansammlungen gefunden werden. Anschließend ließen sie menschliche Muskelzellen, Fruchtfliegen und Mäuse dieselben Polyglycin-Proteine produzieren. In allen drei Systemen kondensierten die Proteine zu runden, dichten Einschlüssen im Zytoplasma und Zellkern, ähnlich den Patientenbefunden. Zellen, die diese Proteine herstellten, hatten eine erhöhte Sterbewahrscheinlichkeit, und bei Mäusen zeigten die betroffenen Muskeln schrumpfende Fasern, zentral gelegene Kerne und Anzeichen von Entzündungen. Reicherte sich die Proteine im Gehirn und Herzen an, entwickelten die Tiere Bewegungsstörungen, Neurodegeneration, Kardiomyopathie und eine verkürzte Lebensspanne — viele der bei Patientinnen und Patienten berichteten Symptome widerspiegelnd.

Ein zentrales toxisches Merkmal, viele lokale Varianten
Obgleich diese Mikroproteine dasselbe zentrale Merkmal teilen — eine lange Kette aus Glycin-Resten — sind sie nicht identisch. Jede entsteht aus einem anderen winzigen Leserahmen in einem anderen Gen und besitzt daher einzigartige Aminosäuresegmente, die die Polyglycin-Strecke flankieren. Das Team fand heraus, dass diese umgebenden Segmente das Verhalten der Proteine stark beeinflussen: wo in der Zelle sie sich anreichern, wie leicht sie Aggregate bilden, mit welchen zellulären Partnern sie interagieren und wie toxisch sie für Muskel- und Nervenzellen sind. Manche Varianten waren besonders schädlich und lösten schnell Einschlussbildung und Zelltod aus, während andere verhältnismäßig milder waren. Das deutet auf einen gemeinsamen toxischen Kernmechanismus hin, der durch den lokalen Sequenzkontext feinabgestimmt wird.
Ein erster Schritt zu einer gemeinsamen Behandlungsstrategie
Ermutigend ist, dass die Forschenden auch ein kleines Molekül identifizierten, das kationische Porphyrin TMPyP4, das sowohl die Anhäufung als auch die Toxizität dieser Polyglycin-Proteine in Zellen und in einem Fruchtfliegenmodell abschwächen kann. TMPyP4 scheint hauptsächlich dadurch zu wirken, dass es die Translation GC-reicher Wiederholungsregionen stört und so die Produktion der schädlichen Proteine verringert, ohne die Gesamtproteinsynthese breit zu unterdrücken. Zwar ist es weit davon entfernt, ein fertiges Medikament zu sein, doch zeigt es prinzipiell, dass ein einziger therapeutischer Ansatz eines Tages Patientinnen und Patienten mit mehreren verwandten Erkrankungen helfen könnte, die durch ähnliche Wiederholungsexpansionen getrieben werden.
Was das für unser Verständnis von Krankheit bedeutet
Für Nicht-Fachleute ist die Kernaussage eindrücklich: DNA-Abschnitte, die lange Zeit als nichtkodierend abgetan wurden, können winzige Rezepturen für Proteine verbergen, die gefährlich werden, wenn bestimmte Wiederholungen sich ausdehnen. Bei OPDM, OPML, neuronaler intranukleärer Einschlusskrankheit und verwandten Störungen werden diese erweiterten GGC-Wiederholungen in klebrige Polyglycin-Proteine übersetzt, die in Zellen verklumpen und nach und nach Muskeln, Nerven und Gehirn beeinträchtigen. Indem die Studie diesen gemeinsamen Mechanismus und einen ersten Kandidatenwirkstoff aufdeckt, erweitert sie unseren Blick darauf, was als Gen gilt, und eröffnet neue Wege zur Behandlung einer wachsenden Familie von durch Wiederholungen verursachten neurologischen Erkrankungen.
Zitation: Boivin, M., Yu, J., Eura, N. et al. GGC repeat expansions within new open reading frames are translated into toxic polyglycine proteins in oculopharyngodistal myopathy. Nat Genet 58, 517–529 (2026). https://doi.org/10.1038/s41588-026-02507-z
Schlüsselwörter: okulopharyngodistale Myopathie, Microsatelliten-Wiederholungsexpansion, Polyglycin-Proteine, Translation nichtkodierender DNA, neurodegenerative Muskelerkrankung