Clear Sky Science · de
GlycoRNA in Komplex mit Heparansulfat reguliert VEGF‑A‑Signalgebung
Wie Zellen die Blutgefäßsignale des Körpers feinabstimmen
Blutgefäße entstehen nicht einfach überall dort, wo Wachstums‑signale auftreten — sie müssen präzise gesteuert werden, damit Gewebe versorgt werden, ohne Tumoren zu nähren oder Blindheit zu verursachen. Diese Arbeit deckt eine unerwartete „Bremse“ für ein zentrales gefäßbildendes Signal namens VEGF‑A auf. Die Autorinnen und Autoren zeigen, dass kleine RNA‑Fragmente, die außen an Zellen zusammen mit Zuckerketten und Proteinen auftreten, die Botschaft von VEGF‑A abschwächen können und damit unsere Vorstellung davon verändern, welche Sprache Zellen an ihrer Oberfläche verwenden.
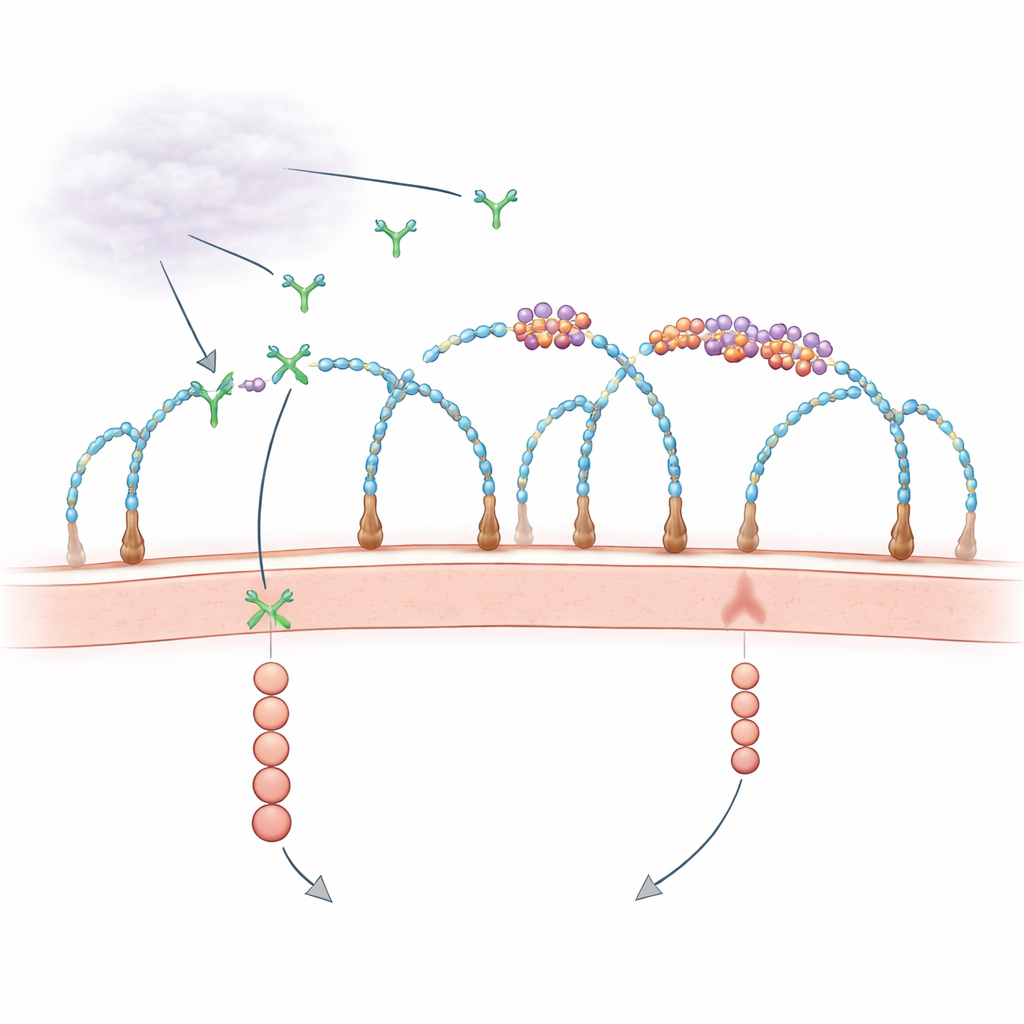
Eine überraschende Rolle für RNA an der Zelloberfläche
Seit Jahrzehnten ist bekannt, dass die äußere Hülle der Zelle, reich an zuckerverzierten Proteinen namens Heparansulfat‑Proteoglykane, Wachstumsfaktoren einfängt und ihren Rezeptoren präsentiert. Zugleich deuteten vereinzelt Beobachtungen darauf hin, dass RNA‑Fragmente außerhalb von Zellen das Gefäßwachstum beeinflussen könnten, doch die Akteure und Mechanismen waren unklar. Jüngere Arbeiten zeigten, dass einige kleine RNAs chemisch an komplexe Zucker gebunden sind und so „GlycoRNAs“ bilden und dass bestimmte RNA‑bindende Proteine ebenfalls an der Zelloberfläche erscheinen und mit diesen RNAs zusammenklumpen. Die neue Studie stellt eine gezielte Frage: Kontrollieren diese winzigen RNA–Protein‑Inseln in der Membran tatsächlich, wie Wachstums‑signale wie VEGF‑A empfangen werden?
Aufbau von clusterbildenden RNA–Protein‑Inseln mit Zuckerketten
Mithilfe genomweiter CRISPR‑Knockout‑Screens und hochauflösender Mikroskopie entdeckten die Forschenden, dass bestimmte Zuckerketten — Heparansulfat mit charakteristischen Sulfatierungen — als essentielle Gerüste für den Aufbau dieser RNA–Protein‑Cluster dienen, die sie als zelloberflächen‑Ribonukleoproteine (csRNPs) bezeichnen. Wenn Schlüsselenzyme, die Heparansulfat synthetisieren oder sulfieren, entfernt wurden, verschwanden die Cluster aus GlycoRNA und ihren Partnerproteinen von der Zelloberfläche, obwohl die RNAs und Proteine weiterhin innerhalb der Zellen vorhanden waren. Enzyme, die Heparansulfatketten von der Oberfläche abschneiden, oder chemische Hemmer der Sulfatierung zeigten denselben Effekt. Diese Ergebnisse belegen, dass intakte, korrekt sulfatiere Heparansulfat‑Ketten csRNPs zu nanoskaligen Inseln in der Membran organisieren.
RNA‑Cluster wirken als Bremse für ein starkes gefäßbildendes Signal
Das Team richtete den Blick dann auf humane Endothelzellen, die Blutgefäße auskleiden und auf VEGF‑A reagieren. Sie fanden, dass auch diese Zellen Heparansulfat‑verankerte csRNP‑Cluster zeigen. Die Behandlung lebender Zellen mit RNasen, Enzymen, die RNA abbauen, entfernte die RNA‑Komponente, ohne die darunterliegenden Zuckerketten zu stören. Unter diesen Bedingungen löste VEGF‑As häufigste heparanbindende Form (VEGF‑A165) eine deutlich stärkere Aktivierung des nachgeschalteten ERK‑Signalwegs aus, während eine kürzere Form ohne heparanbindenden Schwanz (VEGF‑A121) unbeeinflusst blieb. Nach Entfernung der RNA banden sich mehr VEGF‑A165‑Moleküle an die Zelloberfläche, obwohl die Rezeptorzahlen gleich blieben. In 3D‑Mikrofluidik‑Systemen wuchsen Endothelzellen nach RNase‑Behandlung weiter in Kollagengel ein und bildeten robuster röhrenartige Strukturen, was darauf hindeutet, dass die Zerstörung der Oberflächen‑RNA pro‑angiogenes Verhalten freisetzt.
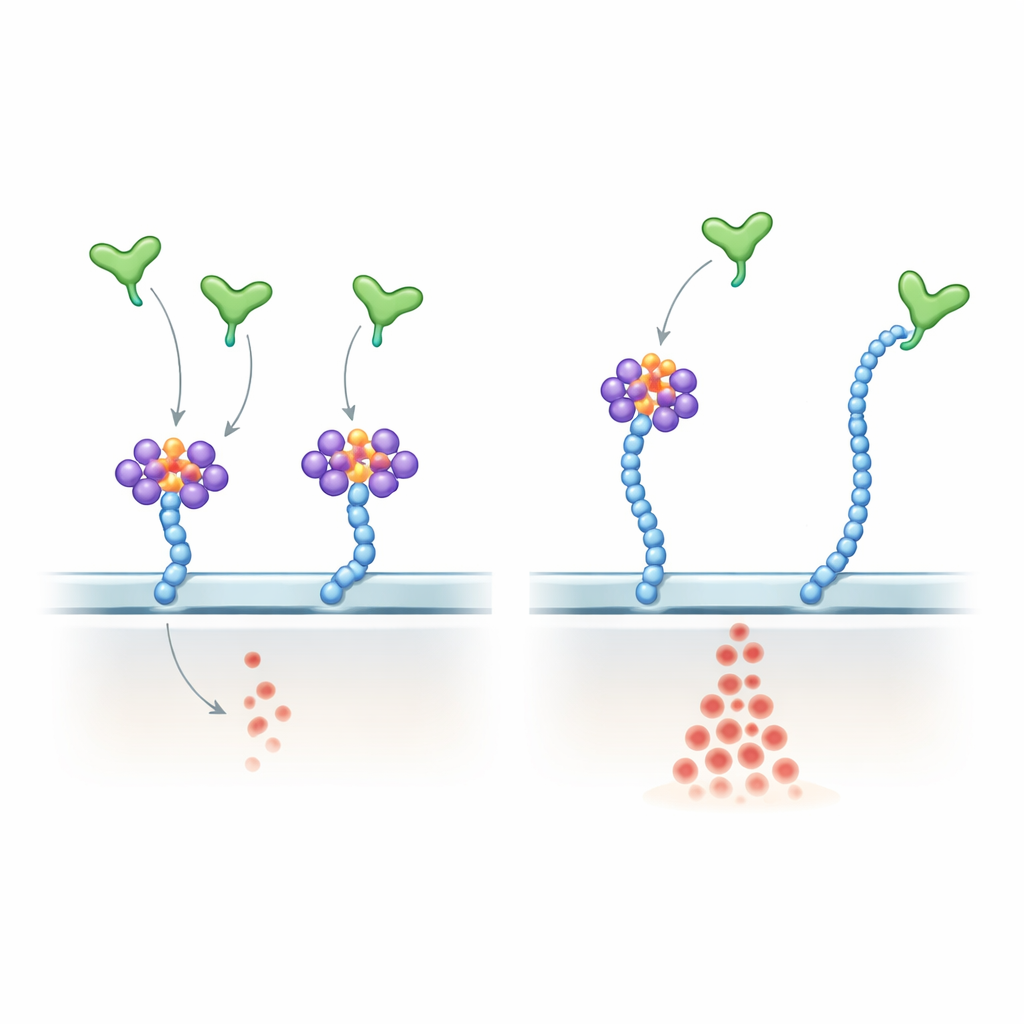
Untersuchung, wie VEGF‑A RNA gegenüber Zucker erkennt
Zur Mechanismusanalyse zeigten die Autorinnen und Autoren, dass VEGF‑A165 ausgewählte kleine RNAs direkt bindet, darunter viele bekannte GlycoRNAs, über seinen positiv geladenen C‑terminalen Bereich — derselbe Bereich, der Heparansulfat bindet. Sie konstruierten eine subtile Variante von VEGF‑A165, bei der Schlüssel‑Argininreste in diesem Schwanz gegen Lysin ausgetauscht wurden. Dieses Mutant behielt seine Gesamtpositivladung und ergriff weiterhin Heparansulfatketten, band GlycoRNA jedoch schlecht und wurde weitgehend unempfindlich gegenüber RNase‑Behandlung. In Endothelzellen erzeugte das Mutant eine stärkere und RNase‑resistentere ERK‑Aktivierung als normales VEGF‑A165 und ahmte damit eng die Wirkung der Entfernung von Oberflächen‑RNA nach. Bei Injektion des Mutants in die Augen lebender Mäuse führte dies zu üppigerem retinalen Gefäßwachstum als das normale Protein. In Zebrafisch‑Embryonen störte die Überexpression der mutierten Vegfa‑Version die normale Gefäßmusterung und erhöhte die Zahl der Endothelzellen.
Vom Basis‑mechanismus zu weiterreichenden Implikationen
Abschließend zeigten die Forschenden, dass das Anfügen des heparanbindenden Schwanzes von VEGF‑A an ein nicht verwandtes Signalmolekül, Wnt3a, dessen Aktivität umlenken konnte: Das Anfügen des normalen Schwanzes dämpfte Wnt‑getriebene Entwicklungsveränderungen, während das Anfügen des RNA‑unempfindlichen Schwanzes sie verstärkte. Zusammengenommen stützen diese Experimente ein Modell, in dem csRNP‑Cluster, verankert durch spezifisch sulfatiertes Heparansulfat, VEGF‑A und verwandte Faktoren binden, um deren Aktivität abzuschwächen. Wird die RNA‑Komponente entfernt oder verlieren Wachstumsfaktoren ihre Fähigkeit, RNA zu erkennen, verschiebt sich das Gleichgewicht hin zu stärkerer Signalgebung und veränderter Gefäßentwicklung in mehreren Spezies.
Warum das für Gesundheit und künftige Therapien wichtig ist
Für Nicht‑Spezialistinnen und Nicht‑Spezialisten lautet die Kernbotschaft: Zellen nutzen nicht nur Proteine und Zucker, sondern auch kleine RNAs an ihrer Oberfläche, um mächtige Wachstumsreize wie VEGF‑A feinzujustieren. Diese zuckerverankerten RNA–Protein‑Cluster wirken als einstellbare Bremsen der Gefäßbildung und helfen sicherzustellen, dass neue Gefäße dort und dann sprießen, wo sie benötigt werden. Das Stören dieses Gleichgewichts — durch Abbau der Oberflächen‑RNA oder Veränderung der RNA‑Bindeeigenschaften von Wachstumsfaktoren — kann Gefäßwachstum übersteigern oder fehlleiten. Das Verständnis dieser neu entdeckten Kontrollschicht könnte den Weg für Therapien öffnen, die die Angiogenese in Krebs, Augenerkrankungen, Wundheilung und regenerativer Medizin gezielter hoch- oder herunterregeln, indem sie Oberflächen‑RNAs, deren Zuckergerüste oder die RNA‑erkennenden Regionen von Wachstumsfaktoren ansprechen.
Zitation: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
Schlüsselwörter: Angiogenese, vaskulärer endothelialer Wachstumsfaktor, Heparansulfat, zelloberflächen‑RNA, GlycoRNA