Clear Sky Science · de
Entwicklungs‑Konvergenz und -Divergenz in menschlichen Stammzellmodellen des Autismus
Warum diese Forschung für Familien und die Gesellschaft wichtig ist
Die Autismus-Spektrum-Störung ist bekannt für ihre Komplexität: Hunderte verschiedener Gene wurden mit erhöhtem Risiko in Verbindung gebracht, dennoch teilen viele autistische Menschen ähnliche Herausforderungen in Kommunikation, sozialer Interaktion und Verhalten. Diese Studie stellt eine auf den ersten Blick einfache, aber folgenreiche Frage: Wenn sehr unterschiedliche genetische Veränderungen das Autismusrisiko erhöhen, stören sie letztlich die Entwicklung des menschlichen Gehirns auf ähnliche Weise? Mithilfe winziger, im Labor aus Patienten-Zellen gezüchteter Modelle des menschlichen Kortex verfolgen die Forschenden, wie frühe Fehlfunktionen in der Genaktivität in gemeinsame Bahnen kanalisiert werden können, die beeinflussen, wie Gehirnzellen geboren werden, reifen und sich vernetzen.
Kleine menschliche Hirngewebe im Labor züchten
Um diese Frage zu untersuchen, sammelte das Team Haut- oder Blutzellen von 55 Personen: Einige trugen gut charakterisierte seltene Mutationen mit starker Verbindung zu Autismus, andere hatten Autismus ohne bekannte große Mutation, und wieder andere dienten als nicht betroffene Kontrollen. Diese Zellen wurden in induzierte pluripotente Stammzellen umprogrammiert, die sich fast in jeden Zelltyp verwandeln können. Die Wissenschaftler leiteten sie anschließend dazu an, dreidimensionale „kortikale Organoide“ zu bilden – winzige Gewebebällchen, die die frühe Entwicklung des menschlichen Gehirnrindens nachbilden. Über 100 Tage entwickelten sich diese Organoide von überwiegend stammzellähnlichen Vorläuferzellen hin zu Netzwerken, die reich an jungen Neuronen sind. Zu vier Zeitpunkten dieses Zeitraums (Tage 25, 50, 75 und 100) maß das Team, welche Gene in Hunderten von Organoiden ein- oder ausgeschaltet waren, und erstellte so einen detaillierten Film molekularer Veränderungen während der frühen Gehirnentwicklung.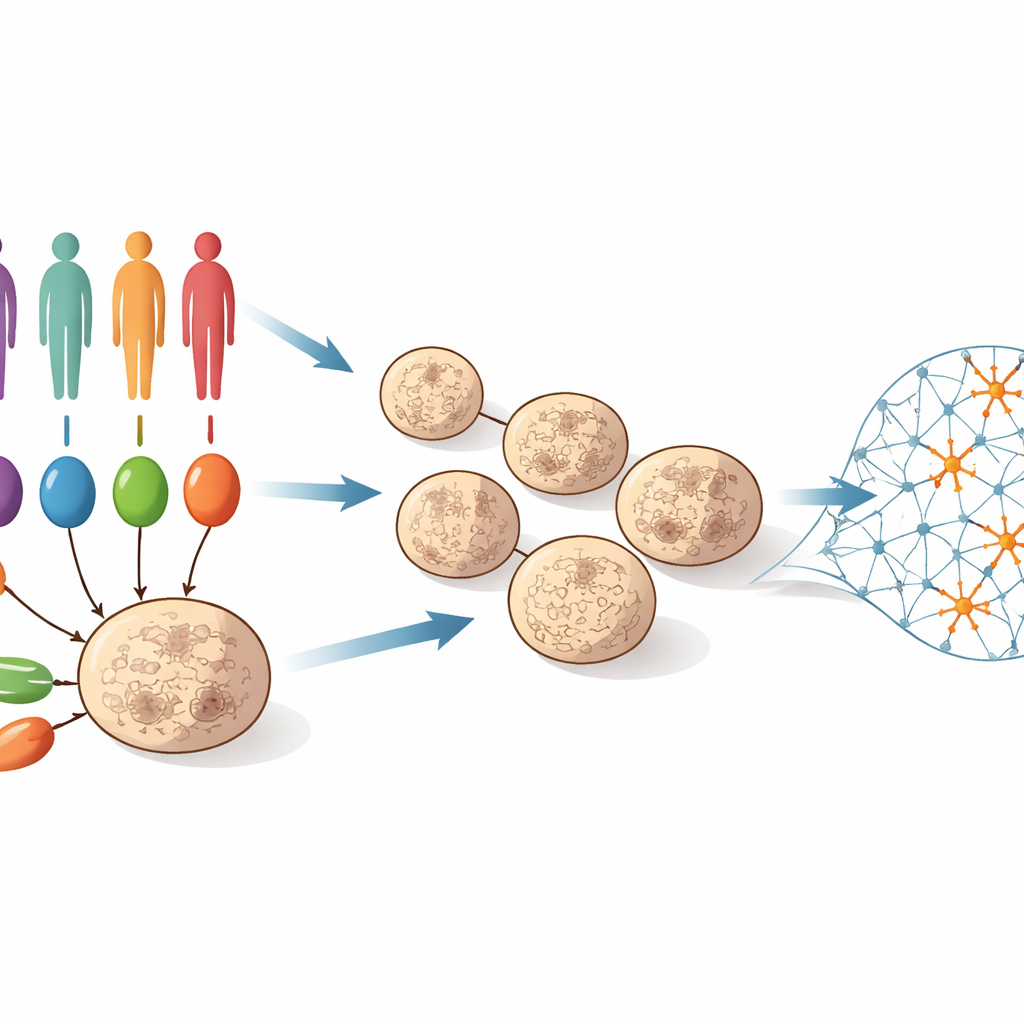
Viele genetische Pfade, gemeinsame frühe Umwege
Obwohl die autismusassoziierten Mutationen sehr unterschiedlich waren – einschließlich großer fehlender oder duplizierter DNA-Abschnitte und spezifischer Genveränderungen – zeigten Organoide mit derselben Mutation hochreproduzierbare Muster der Genaktivität. Früh in der Entwicklung, besonders um Tag 25, erzeugte jede Mutation eine eigene starke Signatur: Hunderte bis mehr als tausend Gene waren im Vergleich zu Kontrollen fehlreguliert. Doch bereits in diesem frühen Stadium veränderten mehrere Mutationen überlappende Genmengen, die an der Art und Weise beteiligt sind, wie DNA in der Zelle verpackt und abgelesen wird. Diese gemeinsamen Veränderungen betrafen bekannte Hochrisiko-Autismusgene und weitere Gene für neuroentwicklungsbedingte Störungen, was darauf hindeutet, dass verschiedene Mutationen sehr früh ähnliche zelluläre Mechanismen stören beginnen.
Konvergenz, während das Gehirnmodell reift
Mit der Reifung der Organoide hin zu ausgereifteren Neuronen (bis Tag 75 und 100) verschob sich das Bild. Die mutationsspezifischen Unterschiede wurden weniger markant, während die Gemeinsamkeiten stärker wurden. In fast allen untersuchten genetischen Formen von Autismus beobachteten die Forschenden eine verringerte Aktivität von Genen, die für elektrische Signalübertragung an Synapsen – den Kommunikationspunkten zwischen Neuronen – wichtig sind, und eine erhöhte Aktivität von Genen, die mit Zellwachstum und Proteinproduktion verknüpft sind. Subtile Verschiebungen in den Anteilen und Reifestadien unterschiedlicher Zelltypen traten zutage, was eher auf Änderungen im Timing der Neuronenbildung und -reifung als auf einen großflächigen Verlust bestimmter Zellen hinweist. Am letzten Zeitpunkt zeigten Tausende von Genen ein gemeinsames Muster der Fehlregulation über die verschiedenen seltenen Mutationen hinweg, obwohl die Mutationen selbst unterschiedliche Ursprungsgene betrafen.
Eine zentrale Steuerungs‑Schaltstelle, die viele Autismusgene verknüpft
Bei tiefergehender Analyse gruppierte das Team Gene, die dazu neigen, gemeinsam ein- und ausgeschaltet zu werden, mithilfe von Netzwerkmethoden in „Module“. Ein Modul stach besonders hervor: M5. Seine Gene sind in der frühen Entwicklung am aktivsten und stark angereichert für Autismus-Risikogene, insbesondere solche, die kontrollieren, wie andere Gene an- oder ausgeschaltet werden und wie DNA verpackt wird. In Organoiden aus mehreren Autismus-Mutationsgruppen war dieses Modul konsistent abgeschwächt. Die Forschenden zeigten, dass viele Proteine in M5 physisch miteinander interagieren und so eine regulatorische Schaltstelle bilden. Mithilfe CRISPR-basierter Werkzeuge, mit denen sie 26 dieser M5-Regulatoren in menschlichen neuronalen Vorläuferzellen selektiv herunterregulierten, bestätigten sie, dass diese Schaltstelle große Mengen nachgeschalteter Gene direkt kontrolliert, einschließlich vieler zusätzlicher Autismus- und neuroentwicklungsrelevanter Risikogene, und dass ihre Störung Pfade beeinflussen kann, die an Neuronenbildung und Synapsenfunktion beteiligt sind.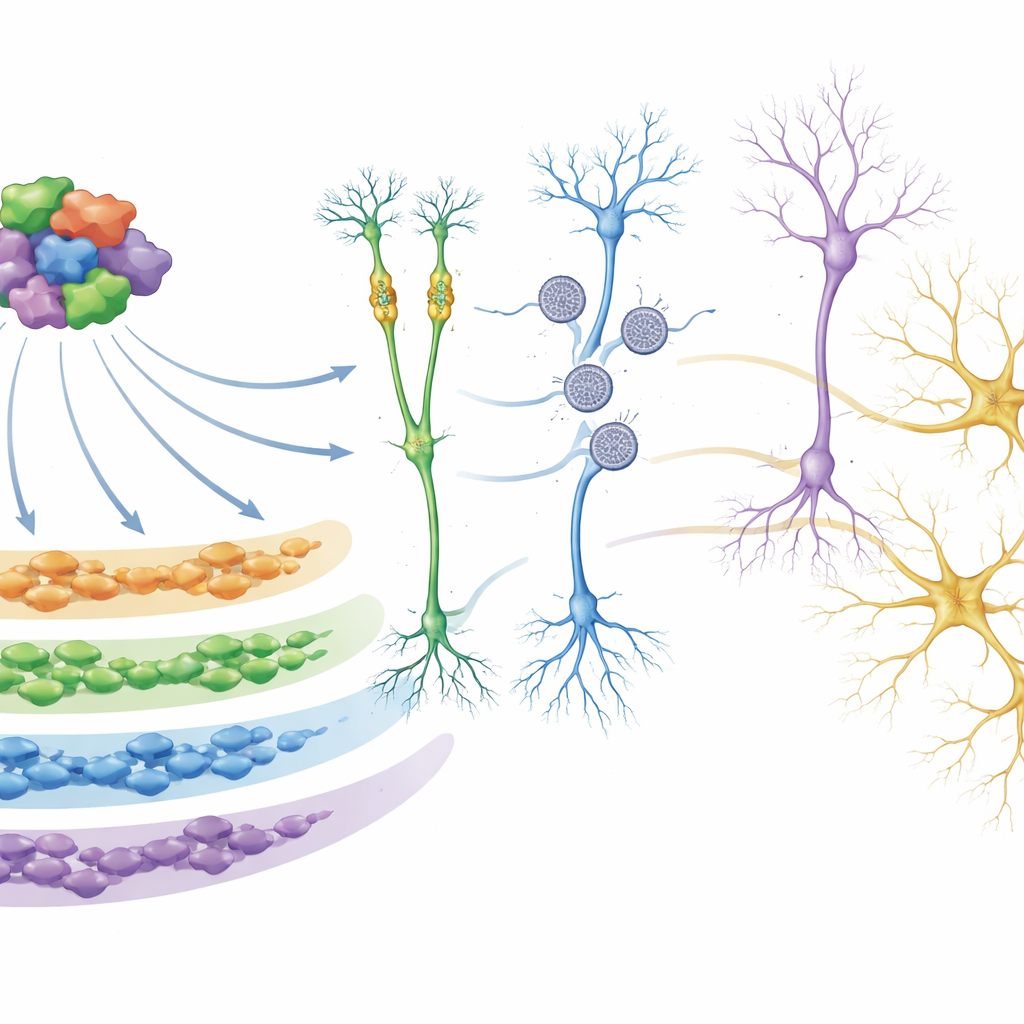
Was das Verständnis von Autismus bedeutet
Diese Arbeit schlägt ein vereinheitlichendes Bild vor: Seltene, stark wirkende autismusassoziierte Mutationen beginnen damit, unterschiedliche Stellen im Genom zu stören, doch ihre Effekte breiten sich vorwärts aus durch ein gemeinsames frühes Kontrollnetzwerk, das steuert, wie kortikale Neurone erzeugt und verschaltet werden. Im Laufe der Zeit konvergieren diese Auswirkungen zu gemeinsamen Ergebnissen – verzögerte oder veränderte Neuronenreifung und gestörte synaptische Programme – obwohl die anfänglichen genetischen Ursachen verschieden sind. Für Familien bedeutet das, dass sehr unterschiedliche DNA‑Diagnosen dennoch überlappende biologische Pfade im sich entwickelnden Gehirn beeinflussen können. Für Forschende und Kliniker bietet das identifizierte regulatorische Netzwerk eine fokussierte Auswahl molekularer Ziele für künftige Therapien, die darauf abzielen, typische Muster der Gehirnentwicklung bei einer breiten Palette autismusbezogener genetischer Zustände wiederherzustellen.
Zitation: Gordon, A., Yoon, SJ., Bicks, L.K. et al. Developmental convergence and divergence in human stem cell models of autism. Nature 651, 707–719 (2026). https://doi.org/10.1038/s41586-025-10047-5
Schlüsselwörter: Autismus-Spektrum-Störung, Gehirn-Organoide, Stammzellmodelle, Genregulation, Neuroentwicklung