Clear Sky Science · de
Systematische Analysen der Lipidmobilisierung durch humane Lipidtransferproteine
Wie Zellen ihre Fette in Ordnung halten
Jede Zelle in Ihrem Körper ist von fettreichen Membranen umgeben, und Tausende unterschiedlicher Lipide helfen diesen Membranen bei Aufgaben vom Signalaustausch bis zur Energieversorgung. Diese Lipide sind jedoch nicht zufällig verteilt: jedes Innenkompartiment einer Zelle hat seine eigene, charakteristische Mischung. Die Studie stellt eine einfache, aber weitreichende Frage: Wie bringen Zellen die richtigen Lipide zur richtigen Zeit an den richtigen Ort, und was passiert, wenn dieses System gestört ist?
Proteine, die Fette shutteln
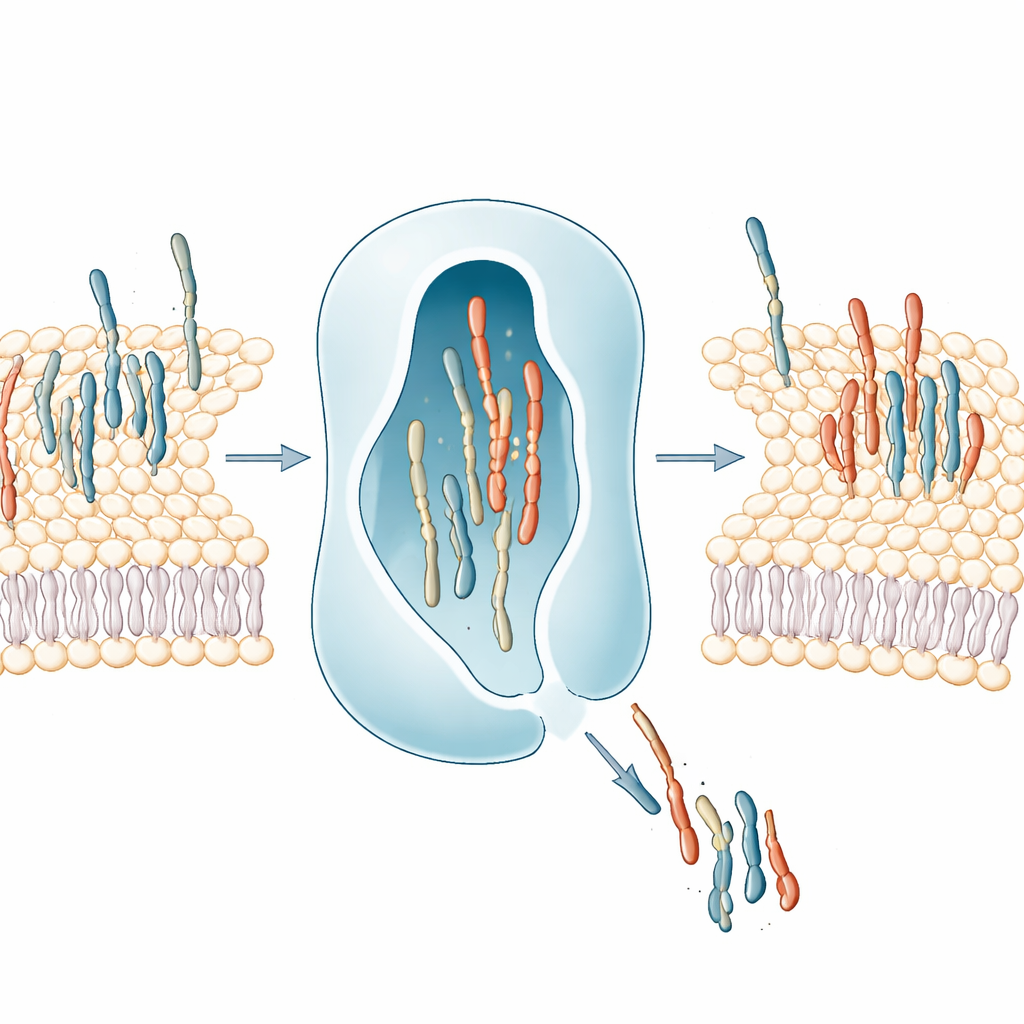
Zellen verlassen sich auf eine große Familie von Molekülen, die Lipidtransferproteine (LTPs) genannt werden: Sie können ein Lipidmolekül aus einer Membran herauslösen, seinen öligen Körper in einer schützenden Tasche verbergen und es an eine andere Membran liefern. Viele humane LTPs werden mit Krankheiten wie Krebs und neurologischen Störungen in Verbindung gebracht, doch für die meisten war bislang unklar, welche Lipide sie tatsächlich transportieren. Die Autoren wollten eine systematische Karte erstellen, welche menschlichen LTPs welche Lipide binden und wie die gesteigerte Aktivität dieser LTPs das gesamte Lipidprofil einer Zelle umgestaltet.
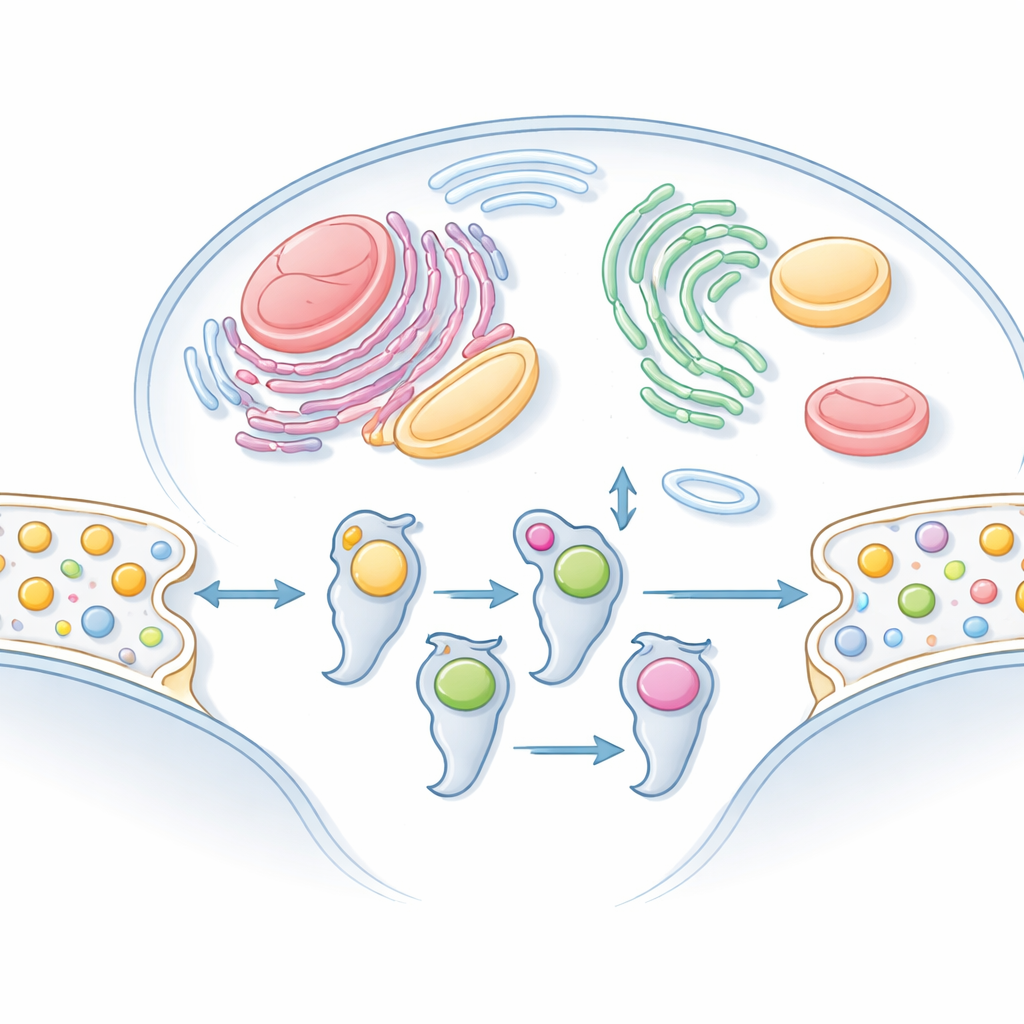
Aufbau einer groß angelegten Karte des Lipidtransports
Dazu klonierte das Team 101 humane LTPs und exprimierte sie in zwei verschiedenen Umgebungen. In zellulären Systemen mit humane Herkunft ließen sie jedes LTP mit den natürlich vorhandenen Lipiden zusammentreffen. In vitro mischten sie gereinigte LTPs mit künstlichen Membranen, die aus Tiergewebeextrakten hergestellt waren. Anschließend reinigten sie mehr als 100 LTP–Lipid-Komplexe und identifizierten die gebundenen Lipide mittels empfindlicher Massenspektrometrie. Durch Abgleich von Protein- und Lipidsignalen über viele Trennschritte filterten sie zufällige Begleiter heraus und behielten nur solche Lipide, die zuverlässig mit jedem LTP mitreisten. Das Ergebnis war ein Katalog von LTP-Partnern, der neun große LTP-Familien abdeckte.
Neue Fracht und neue Regeln
Die Karte bestätigte bekannte Partner — etwa Vitamin A für seine Trägerproteine — deckte aber auch neue und teils überraschende Fracht auf. Ein LTP namens HSDL2, das mit Störungen der Fettspeicherung in Zusammenhang steht, mobilisierte Triacylglycerole, dieselben neutralen Fette, die unsere Fettzellen füllen. Andere LTPs banden Signallipide wie Diacylglycerol oder eine spezielle Gruppe von „Ether“-Lipiden, die über einen eigenen Biosyntheseweg entstehen. Viele LTPs erwiesen sich als polyvalent und gingen mit mehr als einer Lipidklasse um, was darauf hindeutet, dass sie Doppelfunktionen erfüllen: Sie transportieren ihr Hauptfrachtgut, gleichzeitig aber auch Hilfslipide, die den Austausch vorantreiben oder den Stoffwechsel modulieren. Wenn die Forschenden Zellen dazu zwangen, einzelne LTPs zu überproduzieren, änderten sich die Mengen sowohl bekannter als auch neu entdeckter Lipidpartner auf vorhersehbare Weise, was zeigt, dass die neu kartierte Fracht keine Laborartefakte sind, sondern in lebenden Zellen funktionieren.
Warum nur manche Lipide mobil sind
Im gesamten Datensatz fiel den Autoren auf, dass LTPs nicht alle Varianten eines bestimmten Lipids gleich behandelten. Sie zeigten klare Präferenzen für Lipide mit kürzeren Seitenketten und mit ein oder zwei Doppelbindungen in diesen Ketten. Solche Lipide erzeugen winzige Defekte in Membranen, die das Herauspulen erleichtern, während sehr steife oder stark geknickte Ketten schwerer zu extrahieren sind. Einige LTPs gingen noch weiter und bevorzugten extrem spezifische Kettenmuster. Beispielsweise bevorzugte der Ceramidtransporter CERT Ceramide mit bestimmten Kettenlängen, einschließlich seltener sehr langer Spezies, die zur Bildung dicht gepackter Membranregionen beitragen. Eine andere Gruppe, die Phosphatidylinositol-Transferproteine, favorisierte eine Spezies, die eine Arachidonsäure-Seitenkette trägt — ein Baustein vieler hormonähnlicher Signalstoffe. Computersimulationen von LTP-Strukturen zeigten, wie Cluster bestimmter Aminosäuren in den Bindungstaschen eine enge Passform für diese ausgewählten Ketten erzeugen.
Verbundene Lipide und koordinierte Zellvorgänge
Die Studie untersuchte auch, ob verschiedene Lipide, die vom selben LTP transportiert werden, im Leben einer Zelle zusammenhängen. Durch den Vergleich ihrer Karte mit umfangreichen bestehenden Datensätzen fanden die Autoren, dass Lipide, die vom selben LTP gehandhabt werden, dazu neigen, bei Stoffwechselstörungen gemeinsam zuzunehmen oder abzunehmen und an denselben Orten in Zellen und Geweben aufzutreten. Das deutet darauf hin, dass LTPs Gruppen von Lipiden koordinieren, die zusammenarbeiten, statt einzelne Moleküle isoliert zu bewegen. Anders formuliert: Jedes LTP könnte ein kleines „Netzwerk“ von Lipiden definieren, das zusammenreist und als Einheit wirkt.
Warum das für Gesundheit und Krankheit wichtig ist
Für Nichtfachleute lautet die Kernbotschaft: Zellen produzieren nicht nur die richtigen Lipide; sie müssen auch sorgfältig ausgewählte Lipidarten an die richtigen Membranen bringen — und sie tun dies mit einem überraschend vielseitigen Satz von Transferproteinen. Diese Arbeit liefert die erste breite, experimentell fundierte Karte darüber, welche menschlichen LTPs welche Lipide transportieren, und offenbart einfache Regeln — etwa eine Neigung zu bestimmten Kettenlängen und zu bestimmten Graden der Untersättigung — die darüber entscheiden, welche Mitglieder des großen Lipidpools tatsächlich mobil sind. Da viele LTPs und ihre Lipidpartner mit Krebs, Immunreaktionen und Gehirnfunktionen verknüpft sind, bietet diese Ressource einen Ausgangspunkt, um zu verstehen, wie subtile Veränderungen im Lipidverkehr sich auf Krankheiten auswirken können, und um künftige Therapien zu entwerfen, die diese mikroskopischen Shuttles auf gesündere Routen lenken.
Zitation: Titeca, K., Chiapparino, A., Hennrich, M.L. et al. Systematic analyses of lipid mobilization by human lipid transfer proteins. Nature 651, 511–520 (2026). https://doi.org/10.1038/s41586-025-10040-y
Schlüsselwörter: Lipidtransferproteine, Celluläre Membranen, Lipidomik, Membranstoffwechsel, Ceramidtransport