Clear Sky Science · de
Tumor–Gehirn‑Kommunikation bremst die Krebsimmunität über eine sensorisch‑sympathische Achse
Wie Nerven Tumoren beim Verstecken helfen können
Krebs wird meist als Kampf zwischen entarteten Zellen und dem Immunsystem dargestellt, doch diese Studie enthüllt einen überraschenden dritten Akteur: das Nervensystem. Die Forschenden zeigen, dass Lungen‑Tumoren auf einen sensorisch‑sympathischen Nervenkreiszug zwischen Lunge und Gehirn zugreifen können und diesen nutzen, um die körpereigenen Anti‑Krebs‑Abwehrkräfte zu schwächen. Das Verständnis dieses verborgenen „Kabels“ zwischen Tumor und Gehirn könnte neue Wege eröffnen, Lungenkrebs zu behandeln, indem man Nerven und ihre Signale anvisiert und nicht nur die Krebszellen selbst. 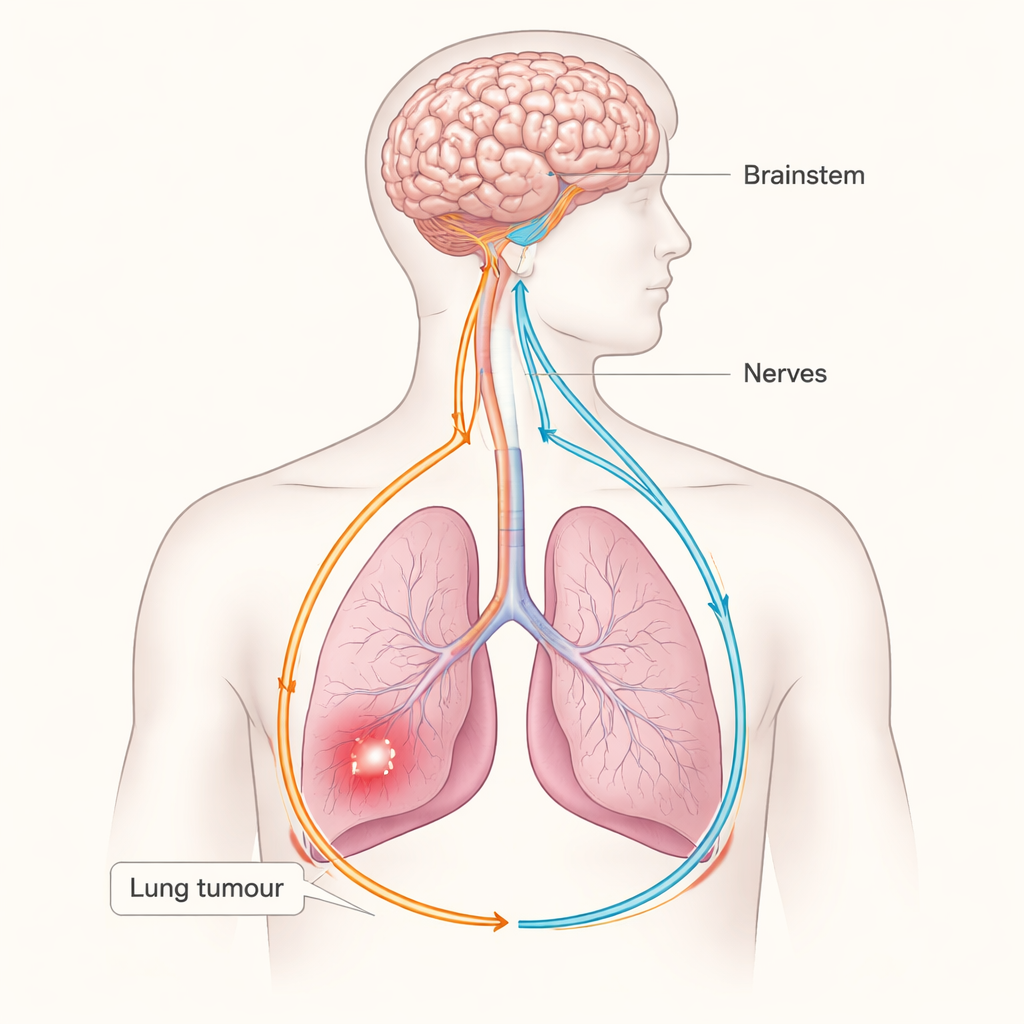
Nerven, die in den Tumor hineinwachsen
Das Team untersuchte Lungenadenokarzinome, eine häufige Form von Lungenkrebs, in ausgefeilten Mausmodellen, die die menschliche Erkrankung gut nachbilden. Mittels ganzer Organ‑3D‑Bildgebung und genetischer Markierung fanden sie, dass Tumoren in der Lunge dicht mit Nervenfasern durchzogen sind. Diese Nerven sind nicht zufällig: Viele stammen von einer spezifischen Gruppe sensorischer Zellen im Vagusnerv, der normalerweise Informationen über den Zustand der Organe ans Gehirn übermittelt. Tumorzellen wurden dabei beobachtet, wie sie wachstumsfördernde Proteine wie den Nervenwachstumsfaktor ausschütten, die diese vagalen sensorischen Fasern zum Auskeimen und zur Invasion des Tumors anregen. Gleichzeitig veränderten die sensorischen Neurone selbst ihre Genaktivität, was darauf hindeutet, dass der Tumor sie umprogrammiert, sodass sie anders reagieren als in gesundem Lungengewebe.
Eine einseitige Verstärkung tumorfördernder Signale
Nicht alle vagus‑assoziierten sensorischen Neurone waren beteiligt. Die Forschenden identifizierten einen Subtyp, der durch zwei Moleküle, NPY2R und TRPV1, gekennzeichnet ist, als die Hauptakteure. Diese Neurone waren in Tumorregionen zahlreich, aber in der umliegenden normalen Lunge weitgehend fehlend. Als die Wissenschaftler diese NPY2R/TRPV1‑Gruppe gezielt entfernten oder stilllegten — mithilfe genetischer Tricks, zielgerichteter Toxine oder Designer‑Rezeptoren, die sich mit einem Medikament ausschalten ließen — schrumpften Lungentumoren dramatisch und die Mäuse lebten länger, mit besserem Gewicht und Verhalten. Im Gegensatz dazu verlangsamte das Entfernen einer anderen sensorischen Untergruppe, die andere Lungenstrukturen innerviert, das Tumorwachstum nicht, was unterstreicht, dass nur ein spezifischer sensorischer „Kanal“ in die Krebskontrolle eingebunden ist. 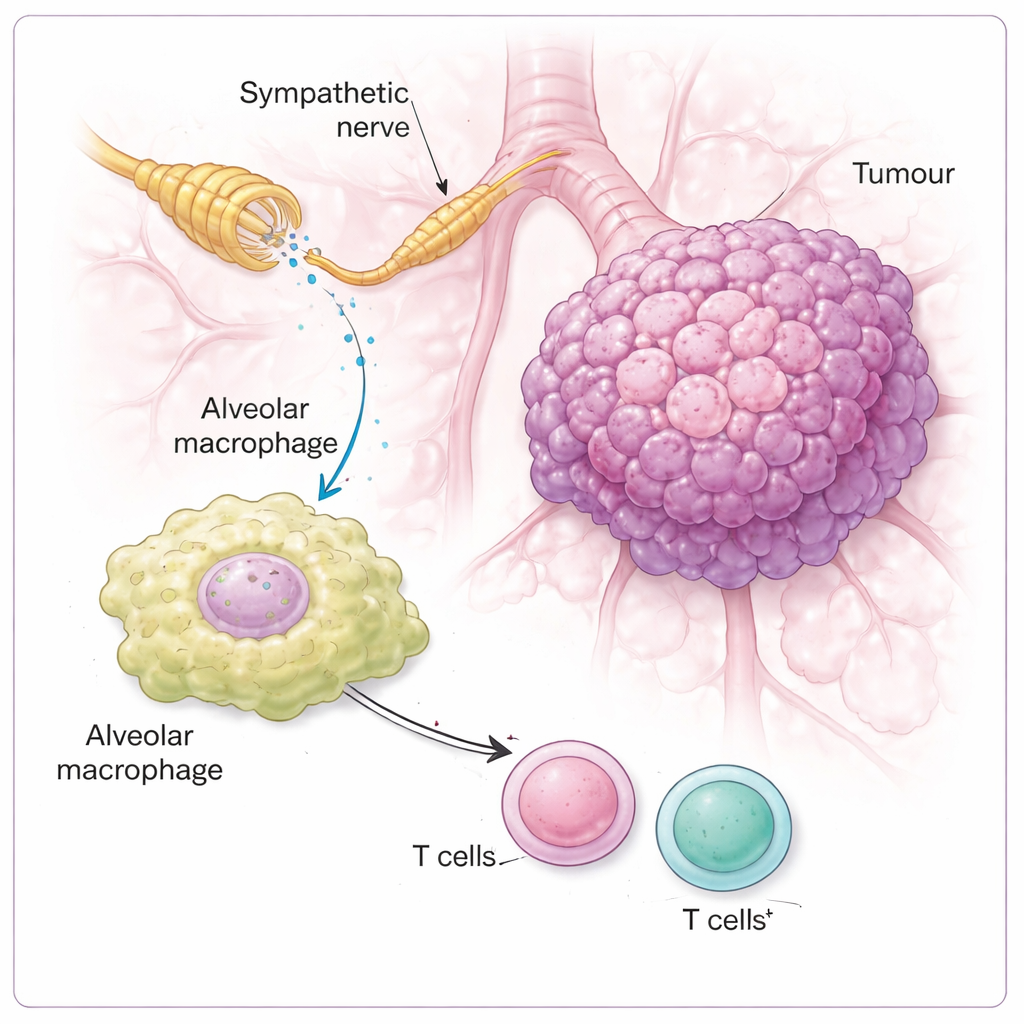
Vom Hirnstamm zu stressähnlichen Signalen in der Lunge
Um zu sehen, wie diese sensorischen Signale vom Gehirn verarbeitet werden, verfolgte das Team die Schaltung stromaufwärts. Aktivitätsmarker zeigten, dass bei Vorhandensein von Lungentumoren Hirnstammregionen, die vagale Eingänge erhalten, aufleuchteten — insbesondere ein Bereich, der als rostrales ventrolaterales Medulla (RVLM) bezeichnet wird, ein zentraler Knoten, der die sympathische „Kampf‑oder‑Flucht“‑Antwort verstärkt. Das Ausschalten der NPY2R/TRPV1‑Sensorneurone beruhigte diese Hirnstammaktivität und verringerte die Anzahl sympathischer Nervenfasern sowie die Konzentration des Stressbotenstoffs Noradrenalin im Tumorbereich. Auch die Stummschaltung des Hirnstamm‑Knotens selbst verlangsamte das Tumorwachstum. Zusammen zeichnen diese Ergebnisse eine geschlossene Schleife: Der Tumor stimuliert vagale Sensoren, der Hirnstamm reagiert mit erhöhter sympathischer Aktivität, und sympathische Nerven wirken auf die Lungenumgebung zurück auf eine Weise, die den Krebs begünstigt.
Immunsystem‑Zellen über lokale Vermittler ausschalten
Die Studie fragte dann, welche Zellen in der Tumornahe die sympathischen Signale tatsächlich „hören“. Überraschenderweise hatte Noradrenalin wenig direkten Einfluss auf das Tumorwachstum in Kulturen. Stattdessen waren die Schlüsselantworter Immunzellen, insbesondere alveoläre Makrophagen — Wächterzellen, die in den Lungenbläschen sitzen. Diese Makrophagen trugen hohe Mengen eines Rezeptors namens β2‑Adrenerger Rezeptor, der Noradrenalin erkennt. Wenn dieser Rezeptor fehlte oder die Noradrenalin‑Signalgebung blockiert wurde, wuchsen Tumoren weniger und die T‑Zell‑vermittelte Immunantwort wurde stärker. In Mäusen mit intaktem Nervenkreis drängte Noradrenalin die Makrophagen in einen unterdrückenderen Zustand, gekennzeichnet durch höhere Spiegel des Enzyms ARG1, das dafür bekannt ist, T‑Zellen abzudämpfen. Wurden Makrophagen auf diese Weise umprogrammiert, konnten benachbarte CD4‑ und CD8‑T‑Zellen — normalerweise die ersten Kämpfer gegen Krebs — keine robuste Reaktion entfalten.
Warum das für die Krebsbehandlung wichtig ist
Kurz gesagt zeigen die Autorinnen und Autoren, dass Lungentumoren über den Vagusnerv mit dem Gehirn „sprechen“ und eine schädliche Gegenreaktion über sympathische Nerven erhalten, die lokale Makrophagen anweisen, T‑Zellen zu beruhigen. Das Unterbrechen eines beliebigen Hauptglieds dieser Schleife — sensorischer Input, Hirnstamm‑Relay, sympathischer Output oder β2‑adrenerge Signalgebung in Makrophagen — reichte aus, um eine stärkere Anti‑Tumor‑Immunität wiederherzustellen und das Krebswachstum bei Mäusen zu bremsen. Daten aus dem Menschen deuteten ebenfalls darauf hin, dass Patientinnen und Patienten, deren Tumoren höhere Signaturen dieser Nervenwege zeigen, tendenziell schlechtere Verläufe und weniger Killer‑T‑Zellen im Tumor aufweisen. Die Arbeit legt nahe, dass bereits für Herzkrankheiten und Angststörungen eingesetzte Medikamente wie Betablocker oder künftig gezielt auf Nervenschaltungen abzielende Therapien umfunktioniert bzw. verfeinert werden könnten, um die „Kabel“ zu durchtrennen, die Tumoren zur Immunflucht nutzen.
Zitation: Wei, H.K., Yu, C.D., Hu, B. et al. Tumour–brain crosstalk restrains cancer immunity via a sensory–sympathetic axis. Nature 650, 1007–1016 (2026). https://doi.org/10.1038/s41586-025-10028-8
Schlüsselwörter: Krebs‑Neurobiologie, Immunität bei Lungenkrebs, Vagusnerv, sympathisches Nervensystem, Tumormikroumgebung