Clear Sky Science · de
Population-scale sequencing resolves determinants of persistent EBV DNA
Warum ein verbreitetes Virus weiterhin relevant ist
Die meisten Erwachsenen tragen das Epstein‑Barr‑Virus (EBV) in sich, oft ohne es je zu bemerken. Für einige ist dieser stille Begleiter jedoch mit Erkrankungen von Pfeifferschem Drüsenfieber bis zu bestimmten Krebsarten und Autoimmunerkrankungen verbunden. Die Studie stellt eine einfache, aber weitreichende Frage: Lassen sich die gewaltigen DNA‑Datenbestände, die bereits aus Bevölkerungsstudien vorliegen, nutzen, um herauszufinden, wer mehr EBV im Blut trägt und ob die Gene dieser Personen mitbestimmen, wer das Virus in Schach hält und wer nicht?
Eine versteckte virale Spur in unserer DNA lesen
Moderne Biobanken wie die UK Biobank und das US‑Programm All of Us haben das komplette Erbgut von Hunderttausenden Freiwilligen sequenziert. Diese Projekte konzentrierten sich auf menschliche Gene, doch die Rohdaten enthalten auch vereinzelte DNA‑Fragmente von Viren. Die Forscher bemerkten, dass das für die Ausrichtung verwendete Referenzgenom der Menschheit eine zusätzliche „Chromosom“-Sequenz für EBV enthält. Indem sie die Reads erneut untersuchten, die auf dieses EBV‑Segment gemappt worden waren, konnten sie abschätzen, wie viele Kopien des EBV‑Genoms zum Zeitpunkt der Probennahme im Blut jeder Person vorhanden waren. Nach sorgfältigem Maskieren einiger irreführender, repetitiver Regionen definierten sie Personen mit klar nachweisbaren Werten als Träger von „EBV‑DNAämie“ — einer messbaren Menge EBV‑DNA im Blut.
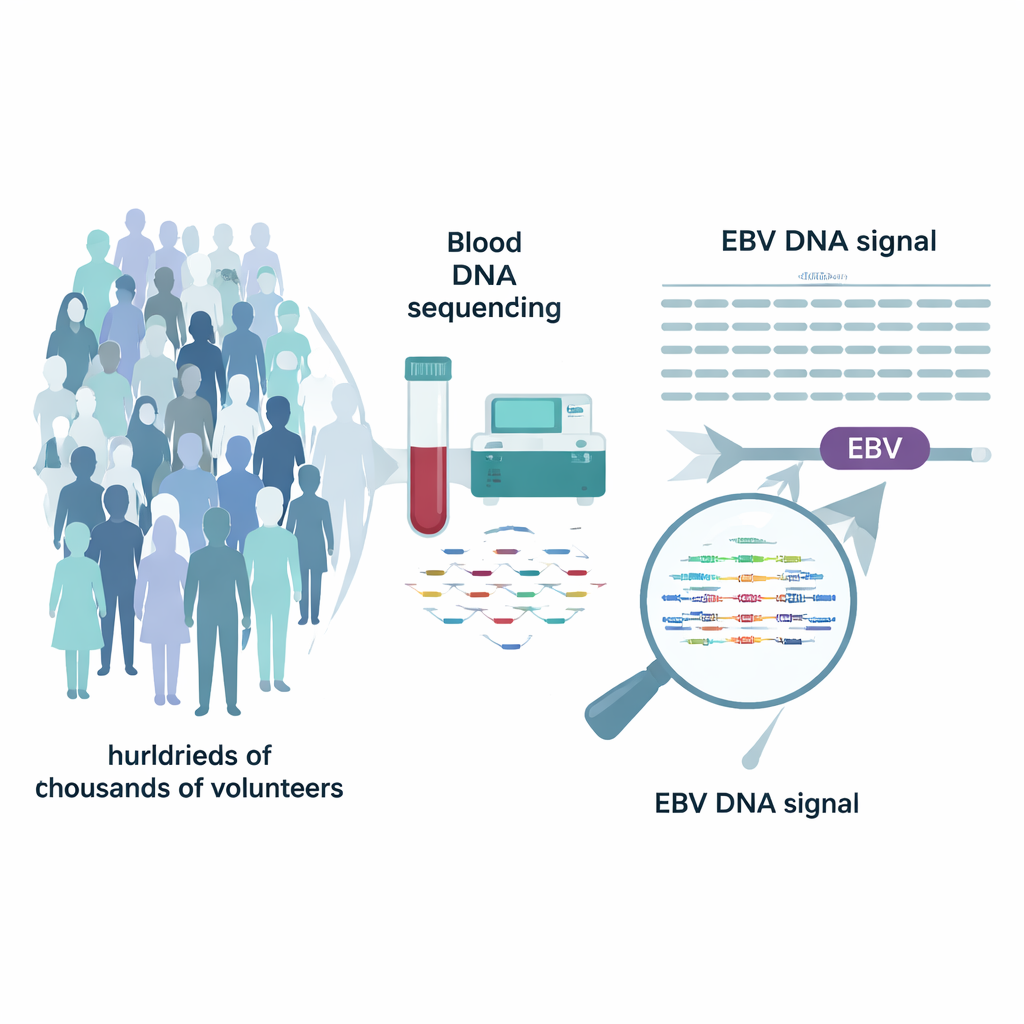
Eine kleine Minderheit trägt eine hohe Viruslast
Bei der Analyse von fast einer halben Million Menschen in der UK Biobank und einer viertel Million in All of Us fand das Team, dass die meisten Erwachsenen keine nachweisbare EBV‑DNA im Blut hatten, obwohl über 90 % durch Antikörpertests Hinweise auf eine frühere Infektion zeigten. Ungefähr 10 % der Teilnehmenden hingegen lagen in einem Schwanz der Verteilung mit deutlich erhöhten EBV‑DNA‑Werten. Diese Personen waren tendenziell älter, häufiger männlich und etwas öfter in Einnahme immunsuppressiver Medikamente. Ähnliche Muster zeigten sich in beiden Kohorten; in einer separaten Gruppe von Speichelproben war das Virus weitaus häufiger nachweisbar, was hervorhebt, dass EBV in verschiedenen Reservoiren des Körpers sitzt und Blutmessungen nur eines davon erfassen.
Zusammenhänge zwischen viraler Persistenz und Krankheit
Mit diesem neuen Biomarker fragten die Autorinnen und Autoren, wie persistente EBV‑DNA im Blut mit dem Gesundheitszustand zusammenhängt. Sie durchsuchten Tausende von Diagnoseschlüsseln und Laborwerten, um zu ermitteln, welche häufiger bei Personen mit EBV‑DNAämie vorkamen. Starke Assoziationen ergaben sich mit Zuständen, die bereits im Verdacht standen, mit EBV verknüpft zu sein, darunter Hodgkin‑Lymphom, rheumatoide Arthritis, Lupus, chronisch obstruktive Lungenerkrankung und bestimmte Lungenkrebsarten. Es gab zudem Signale für Herz‑Kreislauf‑Probleme, Nierenversagen, Depression und Fatigue sowie Hinweise auf seltene neurologische Erkrankungen wie Neuromyelitis optica. Viele dieser Muster wurden in der unabhängigen All of Us‑Kohorte reproduziert. Die Studie kann nicht beweisen, dass EBV diese Probleme verursacht, aber sie zeigt, dass hohe EBV‑DNA‑Werte im Blut ein Marker für weitergehende Gesundheitsrisiken und Störungen des Immunsystems sind.
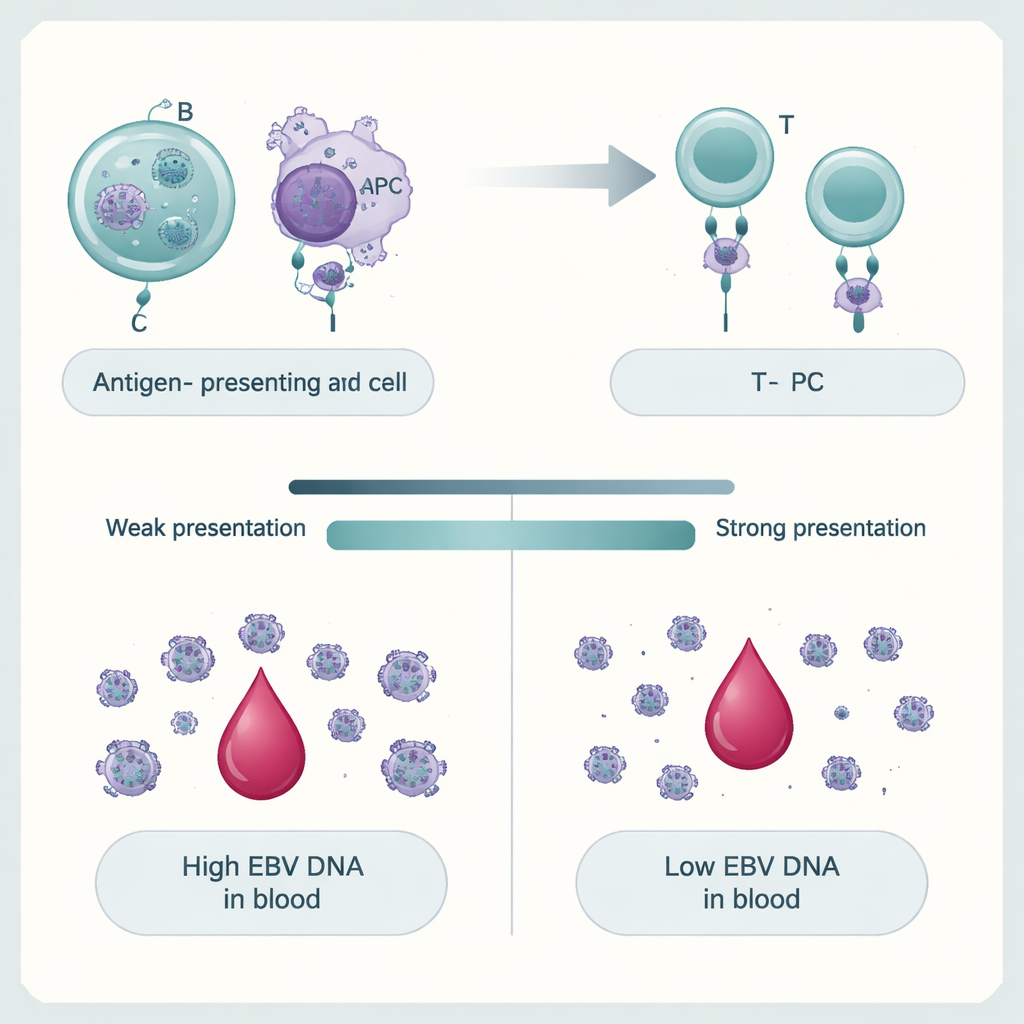
Wie unsere Gene die Kontrolle über das Virus formen
Die Forscher wollten dann wissen, warum nur einige Personen hohe EBV‑DNA‑Werte haben. Durch das Scannen von Millionen genetischer Varianten im gesamten Genom zeigten sie, dass EBV‑DNAämie ein polygenes Merkmal ist: Viele kleine DNA‑Unterschiede zusammen verschieben die Virusmengen nach oben oder unten. Die stärksten Signale häuften sich in und um Gene des Haupthistokompatibilitätskomplexes (MHC), die Immunzellen helfen, virale Fragmente T‑Zellen zu präsentieren. Varianten, die diese Proteine verändern, insbesondere MHC‑Klasse‑II‑Moleküle, waren eng verknüpft damit, ob EBV‑DNA persistierte. Gene, die in B‑Zellen aktiv sind — dem wichtigsten langfristigen Aufenthaltsort von EBV — und in anderen antigenpräsentierenden Zellen, waren besonders angereichert. Mittels Computermodellen, die vorhersagen, wie verschiedene menschliche MHC‑Varianten Stücke des EBV‑Proteoms binden, fanden die Autorinnen und Autoren, dass Varianten, die EBV‑Fragmente stärker präsentieren sollen, tendenziell vor hoher EBV‑DNA schützen, während schwächere Präsentatoren mit Persistenz assoziiert waren.
Was das Verständnis von Infektionen bedeutet
Für Nicht‑Fachleute lautet die Kernbotschaft, dass unser langfristiges Gleichgewicht mit EBV nicht zufällig ist. Durch das Auswerten vorhandener bevölkerungsweiter DNA‑Daten zeigt die Studie, dass die genetische Ausstattung einer Person — insbesondere in Immungenen, die virale Bruchstücke T‑Zellen zeigen — mitbestimmt, wie viel EBV im Blut verbleibt. Hohe Werte kennzeichnen eine Untergruppe von Menschen mit erhöhtem Risiko für eine Reihe von immunologischen, respiratorischen und möglicherweise neurologischen Erkrankungen. Die Arbeit liefert ein Konzept, wie alte Sequenzierungsdaten in neue Einsichten über viele mit uns geteilte Viren verwandelt werden können, und legt nahe, dass gezielte Strategien zur Stärkung oder Nachahmung effektiver Antigenpräsentation eines Tages helfen könnten, lebenslange Infektionen wie EBV besser unter Kontrolle zu halten.
Zitation: Nyeo, S.S., Cumming, E.M., Burren, O.S. et al. Population-scale sequencing resolves determinants of persistent EBV DNA. Nature 650, 664–672 (2026). https://doi.org/10.1038/s41586-025-10020-2
Schlüsselwörter: Epstein–Barr-Virus, viruspersistenz, menschliche Genetik, Autoimmunerkrankung, Biobank-Sequenzierung