Clear Sky Science · de
Individualisierte mRNA‑Impfstoffe rufen langlebige T‑Zell‑Immunität bei adjuvanter TNBC hervor
Neue Hoffnung nach Brustkrebsbehandlung
Für viele Frauen mit einer aggressiven Form von Brustkrebs, dem sogenannten triple‑negativen Brustkrebs, endet die Angst nicht mit dem Abschluss von Chemotherapie und Operation. Diese Krebsart hat ein hohes Risiko für Rückfälle und Metastasen, oft schon innerhalb weniger Jahre. Die hier beschriebene Studie prüft einen stark personalisierten Impfstoff, der aus den Mutationen des Tumors jeder Patientin hergestellt wird, um zu untersuchen, ob er das Immunsystem über Jahre wachsam halten und die Wahrscheinlichkeit eines Rückfalls nach Abschluss der Standardbehandlung reduzieren kann.
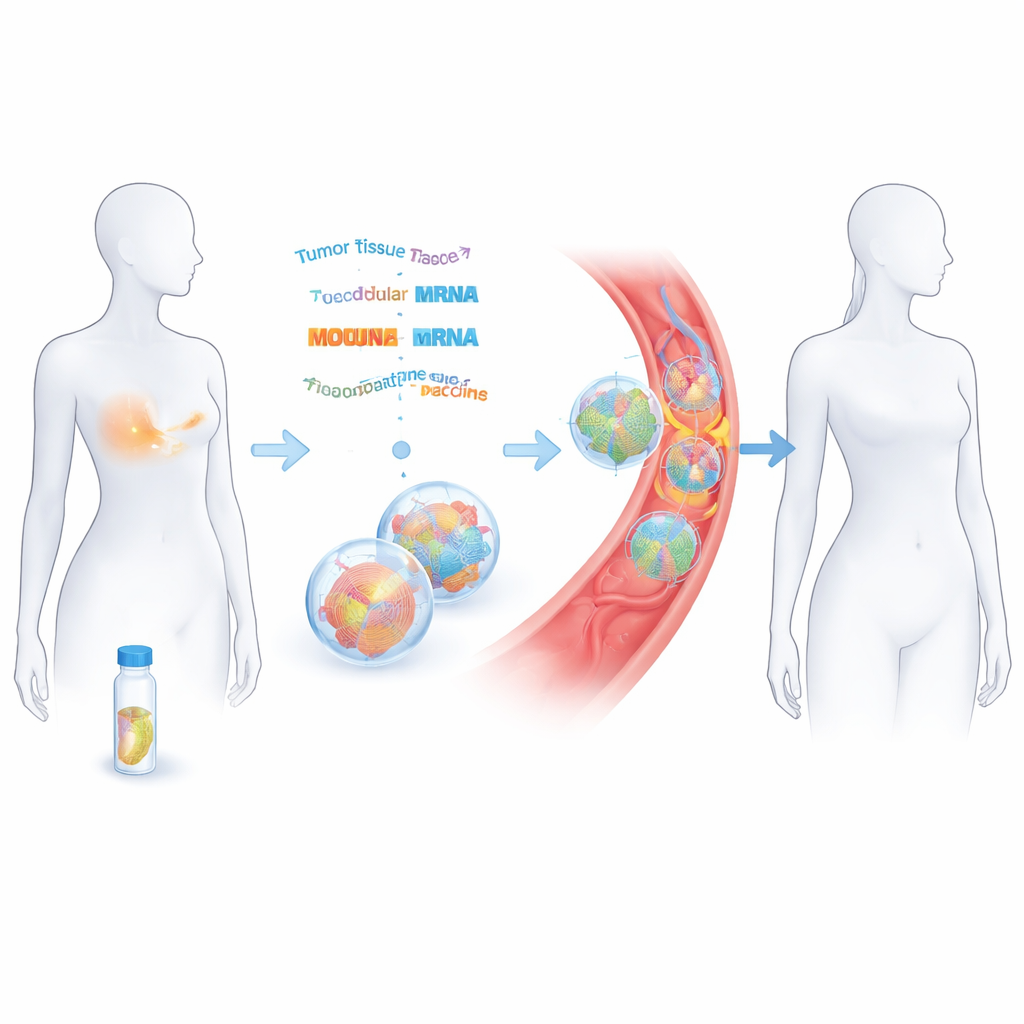
Aus einem entfernten Tumor einen maßgeschneiderten Impfstoff herstellen
Die Forschenden arbeiteten mit 14 Frauen, die einen frühen triple‑negativen Brustkrebs hatten und bereits mit kurativer Absicht operiert und chemotherapeutisch behandelt worden waren. Aus dem entfernten Tumorgewebe bestimmten sie DNA und RNA, um die einzigartigen Mutationen des Krebses zu katalogisieren. Mithilfe von Computerwerkzeugen sagten sie voraus, welche dieser Veränderungen von Immunzellen als fremd erkannt werden könnten. Bis zu 20 dieser „Neoantigene“ wurden dann aneinandergereiht und in zwei Stränge Messenger‑RNA (mRNA) codiert, ähnlich dem Prinzip der COVID‑19‑Impfstoffe, aber auf jede Patientin zugeschnitten. Diese mRNA‑Stränge wurden in winzige Fett‑Bläschen verpackt und in acht Dosen über etwa zwei Monate intravenös verabreicht.
Wie der Impfstoff die Immunverteidiger weckt
Einmal im Körper, weist die mRNA dendritische Zellen, die Wächter des Immunsystems, an, kurzzeitig die Neoantigen‑Proteine herzustellen und Bruchstücke davon auf ihrer Oberfläche zu präsentieren. Das wirkt wie ein Steckbrief für T‑Zellen, die wichtigste krebsbekämpfende Kraft des Immunsystems. Das Team entnahm Blut vor der Impfung und zu mehreren Zeitpunkten danach, um zu prüfen, ob neoantigen‑spezifische T‑Zellen auftauchten und wie stark die Antworten waren. Mit empfindlichen Labortests stellten sie fest, dass jede Patientin neue oder verstärkte T‑Zell‑Antworten gegen mindestens eine der ausgewählten Mutationen entwickelte, und die meisten reagierten gegen mehrere. In vielen Fällen waren nun große Anteile zirkulierender T‑Zellen — Werte, wie man sie sonst nur bei starken Zelltherapien sieht — auf tumor‑spezifische Ziele eingestellt.
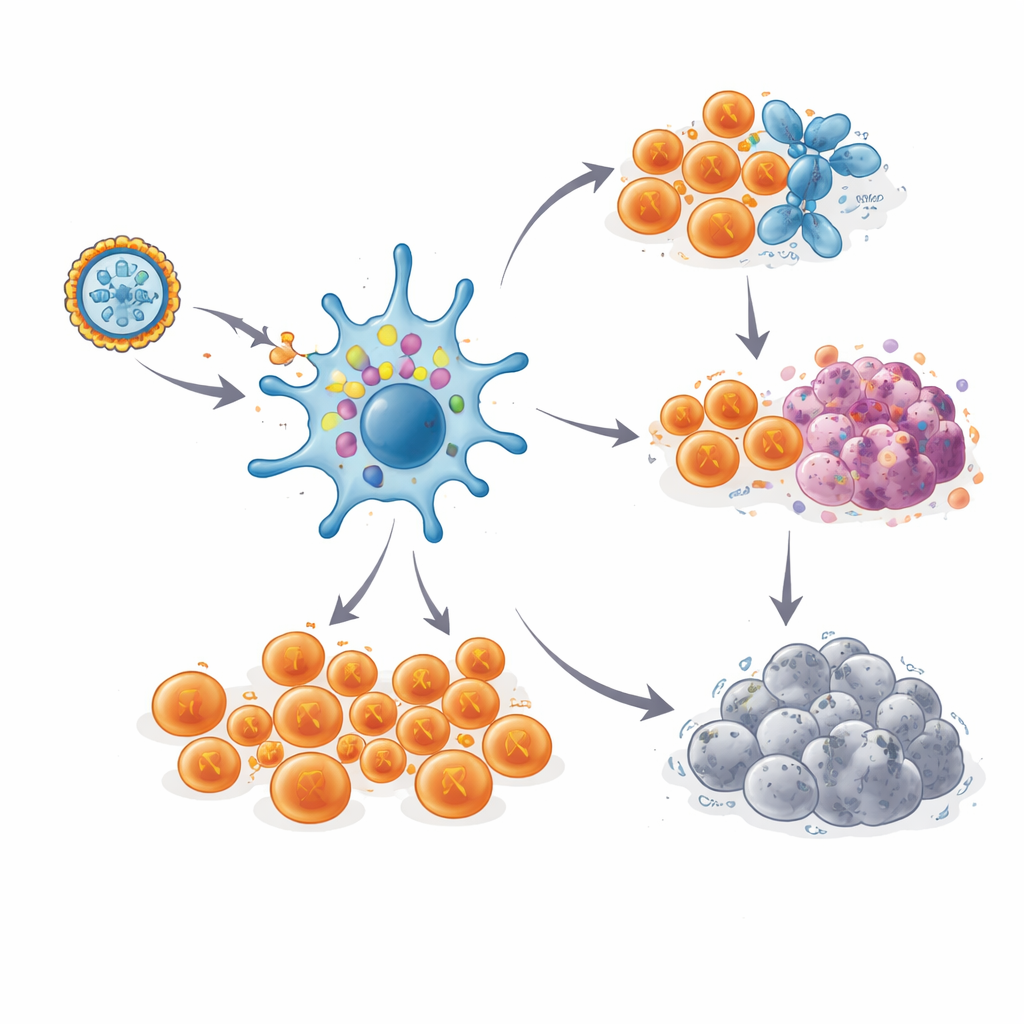
Langanhaltendes immunologisches Gedächtnis
Wichtig ist, dass diese T‑Zell‑Antworten nicht schnell nachließen. Bei den meisten Patientinnen erreichten die starken Antworten ihren Höhepunkt während der Impfserie, gingen leicht zurück und blieben dann über ein bis dreieinhalb Jahre auf hohem Niveau, selbst ohne Auffrischungsimpfungen. Durch das Verfolgen der einzigartigen Rezeptor‑„Barcode“ einzelner T‑Zell‑Klone konnten die Forschenden spezifische neoantigen‑reaktive Zellen bei einer Patientin, die krebsfrei blieb, bis zu sechs Jahre verfolgen. Detaillierte Einzelzellanalysen zeigten zwei Hauptschicksale dieser Zellen: Viele wurden zu stark bewaffneten Killer‑T‑Zellen, bereit, jede Zelle mit dem passenden Neoantigen zu zerstören. Andere entwickelten sich zu einem selteneren, stammlinienähnlichen Gedächtnispool mit Merkmalen der Selbsterneuerung, was auf ein Reservoir hindeutet, das im Falle eines Wiederauftretens des Krebses neue Wellen von Effektorzellen regenerieren könnte.
Was mit den Patientinnen geschah
Nach einer Nachbeobachtungszeit von median etwas über fünf Jahren nach der ersten Impfdosis hatten elf der vierzehn Frauen kein Wiederauftreten ihres Krebses erlebt; eine von ihnen starb während der Remission aus nicht mit dem Krebs zusammenhängenden Gründen. Drei Frauen erlitten einen Rückfall, und ihre Fälle geben Hinweise darauf, warum ein personalisierter Impfstoff manchmal versagen kann. Eine Patientin zeigte nur eine schwache T‑Zell‑Antwort und profitierte später von einer anderen Immuntherapie, einem Anti‑PD‑1‑Antikörper, bevor sie schließlich an weit verbreiteter Erkrankung verstarb. Eine zweite Patientin hatte eine erbliche Veranlagung und Tumoren in beiden Brüsten; nur ein Tumor wurde für die Impfstoffgestaltung verwendet, und später zeigte sich, dass der Rückfall vom genetisch unterschiedlichen, nicht durch den Impfstoff abgedeckten Tumor stammte. Die dritte Patientin hatte starke, durch den Impfstoff induzierte T‑Zellen, die den rezidivierenden Tumor infiltrierten, aber die Krebszellen hatten größtenteils wichtige Moleküle verloren, die nötig sind, um Neoantigene an ihrer Oberfläche zu präsentieren, wodurch sie sich effektiv vor dem Immunangriff versteckten.
Warum diese Arbeit für die Zukunft wichtig ist
Diese Studie in einer frühen Phase war klein und hatte keine Kontrollgruppe, sodass sie nicht beweisen kann, dass der Impfstoff allein Rückfälle verhindert hat. Trotzdem zeigt sie, dass die Herstellung eines komplexen, individuellen mRNA‑Impfstoffs aus dem eigenen Tumor einer Patientin in routinemäßigen Krankenhausumgebungen machbar ist, im Allgemeinen gut vertragen wurde und potente, langlebige T‑Zell‑Armeen gegen mehrere krebspezifische Ziele auslösen kann. Die Ergebnisse heben auch Fluchtwege hervor, die Tumoren nutzen können, etwa den Verlust ihrer Antigenpräsentations‑Maschinerie oder das Entstehen aus nicht erfassten Läsionen, und weisen auf Kombinationen mit anderen Immuntherapien sowie umfangreichere Tumorsequenzierung hin. Für Patientinnen mit triple‑negativem Brustkrebs deutet diese Arbeit darauf hin, dass ein maßgeschneiderter Impfstoff, der nach der Standardbehandlung gegeben wird, eines Tages helfen könnte, ein Wiederauftreten der Erkrankung zu verhindern, indem er ihr eigenes Immunsystem in eine dauerhafte, hochspezifische Verteidigungslinie verwandelt.
Zitation: Sahin, U., Schmidt, M., Derhovanessian, E. et al. Individualized mRNA vaccines evoke durable T cell immunity in adjuvant TNBC. Nature 651, 1088–1096 (2026). https://doi.org/10.1038/s41586-025-10004-2
Schlüsselwörter: triple-negativer Brustkrebs, mRNA-Krebsimpfstoffe, Neoantigen-Immuntherapie, T‑Zell‑Immunität, Tumorrezidiv