Clear Sky Science · de
Polyaminabhängige metabolische Abschirmung reguliert alternatives Spleißen
Wie winzige Moleküle Zellen beim Lesen ihrer Gene helfen
In jeder Zelle kann das gleiche DNA-Skript auf viele Arten gelesen werden, sodass eine begrenzte Zahl von Genen eine enorme Vielfalt an Proteinen erzeugen kann. Diese Flexibilität beruht auf einem Prozess namens alternatives Spleißen, der RNA-Botschaften bearbeitet, bevor sie in Proteine übersetzt werden. Diese Arbeit zeigt, dass kleine, positiv geladene Moleküle, sogenannte Polyamine, stillschweigend dieses Bearbeitungsschritt lenken und als eine Art Schutzschild wirken, das Zellen hilft zu entscheiden, welche RNA-Versionen entstehen sollen. Da alternatives Spleißen eine zentrale Rolle bei Krebs, Hirnfunktionen und Stammzellen spielt, hat die Entdeckung dieser verborgenen Kontrollschicht weitreichende Folgen für Gesundheit und Krankheit.
Kleine geladene Helfer in jeder Zelle
Polyamine sind winzige, flexible Moleküle mit mehreren positiven Ladungen. Zellen stellen sie aus einfachen Nährstoffen her, und seit langem sind sie als Unterstützer von Wachstum und Überleben bekannt, besonders in schnell teilenden Zellen wie Tumoren. Die Autor:innen fragten, ob Polyamine nicht nur als Bausteine dienen, sondern auch als Signale. Durch teilweise Blockade der Polyaminproduktion in Prostatakrebszellen und in Mäusen verfolgten sie, wie sich Proteine und RNA im Zeitverlauf veränderten. Sie fanden, dass lange bevor die Gesamtmenge an Polyaminen stark sank, eine ausgeprägte Welle von Veränderungen in der Proteinkinase-Phosphorylierung auftrat—chemische Markierungen, die Proteinschalter an- oder ausschalten—insbesondere an Komponenten der zellulären RNA-Bearbeitungsmaschinerie, dem Spleißosom.
Umbau des RNA-Editors der Zelle
Mit Blick auf die RNA nutzte das Team tiefgehende Sequenzierung, um alternatives Spleißen zu verfolgen, wenn die Polyaminsynthese gehemmt wurde. Hunderte von RNA-Segmenten wurden unterschiedlich übersprungen oder eingebaut, sowohl in Krebszelllinien, normalen Zelltypen als auch in Geweben von Mäusen. Diese Veränderungen waren nicht einfach eine Begleiterscheinung verlangsamter Zellteilung oder eines anderen bekannten polyaminabhängigen Prozesses, der Hypusinierung heißt. Stattdessen kehrten viele Spleißveränderungen zurück, wenn die Forschenden den Zellen von außen Polyamine zuführten. Sowohl Medikamente als auch genetische Werkzeuge, die Polyamine senkten, erzeugten ähnliche Spleißmuster, und eine zusätzliche Erniedrigung der Polyamine durch eine Wirkstoffkombination verstärkte die Effekte, was bestätigt, dass der Effekt eng mit der Verfügbarkeit von Polyaminen verknüpft ist.
Ein verstecktes Ziel: das SF3-Spleißmodul
Um zu bestimmen, wo im Spleißapparat Polyamine wirken, verglichen die Autor:innen die durch Polyaminabnahme verursachte Spleißsignatur mit einer großen Referenzkarte, die durch individuelles Stilllegen von mehr als 300 bekannten Spleißfaktoren erstellt worden war. Die engste Übereinstimmung wies auf einen bestimmten Teil des Spleißosoms, das SF3-Subkomplex, hin, der dabei hilft, wichtige Signale in der RNA zu erkennen. Computergestützte Analysen öffentlicher Protein–RNA-Bindungsdaten unterstützten diesen Zusammenhang: RNAs, deren Spleißen durch Polyaminverlust verändert wurde, wurden besonders häufig von SF3-Proteinen gebunden. Wenn das Team SF3-Komponenten partiell genetisch oder pharmakologisch abschwächte, wurden die Spleißeffekte der Polyaminminderung weitgehend aufgehoben, was zeigt, dass eine intakte SF3-Aktivität für diesen neuen Regulationsweg erforderlich ist. 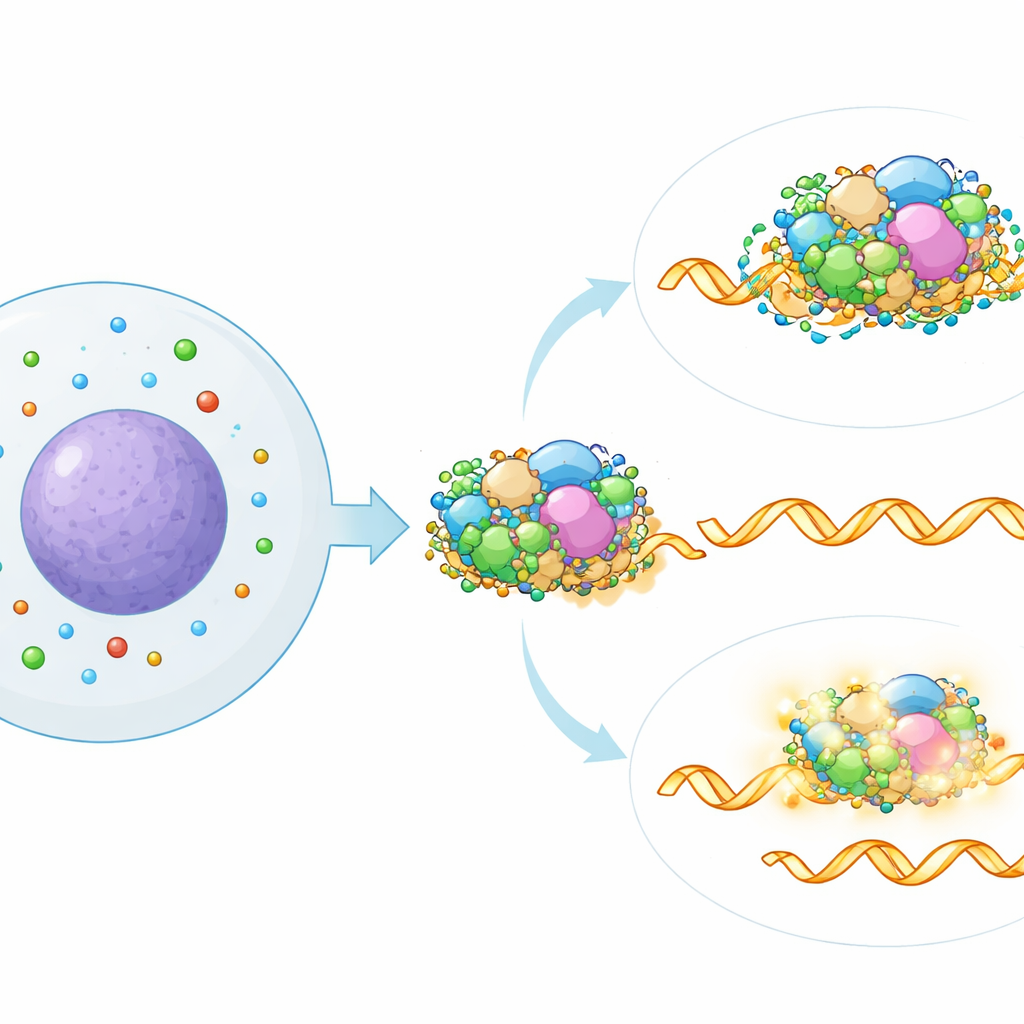
Metabolische Abschirmung: wie Polyamine Proteinmarkierung blockieren
Bei genauerer Betrachtung stellten die Forschenden fest, dass die am stärksten betroffenen Phosphorylierungsstellen auf SF3-Proteinen innerhalb kurzer Abschnitte mit vielen negativ geladenen Aminosäuren gehäuft lagen. Molekulare Modellierung und Kernspinresonanzexperimente zeigten, dass Polyamine sich in diese sauren Taschen einlagern, mehrere elektrostatische Kontakte bilden und benachbarte Serinreste, an denen typischerweise Phosphatgruppen angebracht werden, teilweise überdecken. Diese physikalische „Umarmung“ verringert die Zugänglichkeit dieser Stellen für Proteinkinasen—die Enzyme, die Phosphate anbringen. In Reagenzglasversuchen blockierten zugefügte Polyamine direkt eine Kinase namens CK1 daran, SF3-Proteine zu phosphorylieren. In Zellen dämpften die Hemmung von CK1 und seinem nahen Verwandten CK2 die durch Polyaminverlust ausgelösten Spleißeffekte, und speziell konstruierte Mäuse, deren SF3A3-Protein drei zentrale Phosphorylierungsstellen nicht mehr besaß, zeigten weitgehend Unempfindlichkeit gegenüber polyaminabhängigen Spleißverschiebungen. 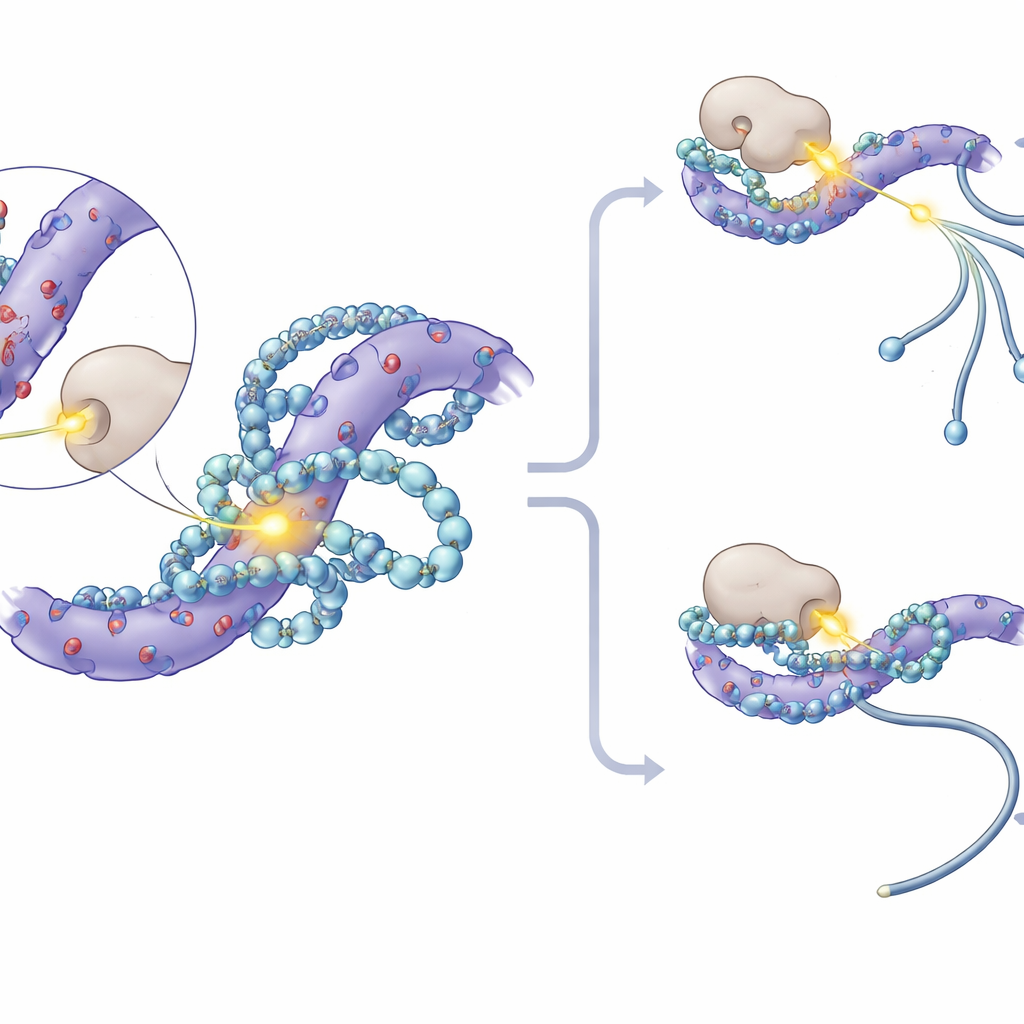
Ein Designer-Molekül, das Funktionen trennt
Die Studie stellt außerdem ein polyaminähnliches Medikament vor, BENSpm, das stärker positiv geladen ist, gleichzeitig aber die körpereigene Polyaminproduktion herunterfährt. BENSpm band fest an die sauren SF3-Patches und blockierte die Kinasewirkung, ähnlich wie natürliche Polyamine, konnte jedoch das Zellwachstum nicht retten, wenn echte Polyamine knapp waren. Dadurch konnten die Autor:innen klassische Polyaminfunktionen (Unterstützung von Wachstum und Stoffwechsel) von der neu definierten Abschirmungsrolle trennen. In embryonalen Stammzellen von Mäusen trieb Polyaminmangel die Zellen dazu, ihr Stammzellmerkmal Nanog zu verlieren, und veränderte ihr Spleißprofil. BENSpm stellte sowohl das Spleißmuster als auch die Nanog-Expression wieder her, obwohl die normale Polyaminsynthese weiterhin unterdrückt war, was darauf hinweist, dass metabolische Abschirmung eine Schlüsselanforderung für die Erhaltung der Stammzellidentität ist.
Warum diese Entdeckung wichtig ist
Alltäglich gesprochen zeigt diese Arbeit, dass Polyamine wie winzige Schutzhandschuhe um empfindliche Bereiche wichtiger Spleißproteine wirken. Sind die Handschuhe an, können Kinasen diese Stellen nicht leicht greifen und markieren, und die RNA-Bearbeitung verläuft wie vorgesehen. Sind Polyamine knapp, fallen die Handschuhe ab, die Phosphorylierung steigt an und Spleißmuster verändern sich, mit Folgen sowohl für Krebs- als auch für Stammzellen. Indem die Studie diesen Mechanismus der „metabolischen Abschirmung“ definiert und ein Werkzeugmolekül bereitstellt, das ihn selektiv nachahmt, öffnet sie Wege, das Genablesen zu modulieren, ohne die DNA zu verändern, und könnte künftige Therapien inspirieren, die auf das Spleißen bei Krebs und in der regenerativen Medizin abzielen.
Zitation: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
Schlüsselwörter: Polyamine, alternatives Spleißen, RNA-Verarbeitung, metabolische Signalgebung, Stammzellregulation