Clear Sky Science · de
Ligand-spezifische Aktivierungspfade bestimmen GPCR-Signale in Zellen
Wie ein einzelner Rezeptor wie viele Schalter wirken kann
Viele der heutigen Medikamente wirken auf eine große Familie von Zelloberflächenproteinen, die G-Protein-gekoppelte Rezeptoren oder GPCRs genannt werden. Diese Rezeptoren beeinflussen Herzfrequenz, Stimmung, Atmung und unzählige andere Körperfunktionen. Jahrzehntelang wurden sie als einfache Ein-/Aus-Schalter behandelt: Ein Wirkstoff bindet, der Schalter klappt um und ein Signal fließt in die Zelle. Diese Arbeit zeigt, dass die Wirklichkeit weit komplexer ist. Mit einer neuen Art von fluoreszierendem „Spion“, der direkt in einen Rezeptor eingebaut ist, beobachten die Autoren in lebenden Zellen, wie verschiedene Wirkstoffe denselben Rezeptor auf unterschiedlichen Aktivierungspfaden — wie verschiedene Routen durch eine Stadt — entlangschicken, um unterschiedliche Muster der Signalgebung hervorzurufen. Das Verständnis dieser verborgenen Routen könnte helfen, Medikamente zu entwickeln, die den gewünschten Nutzen bringen und Nebenwirkungen vermeiden.
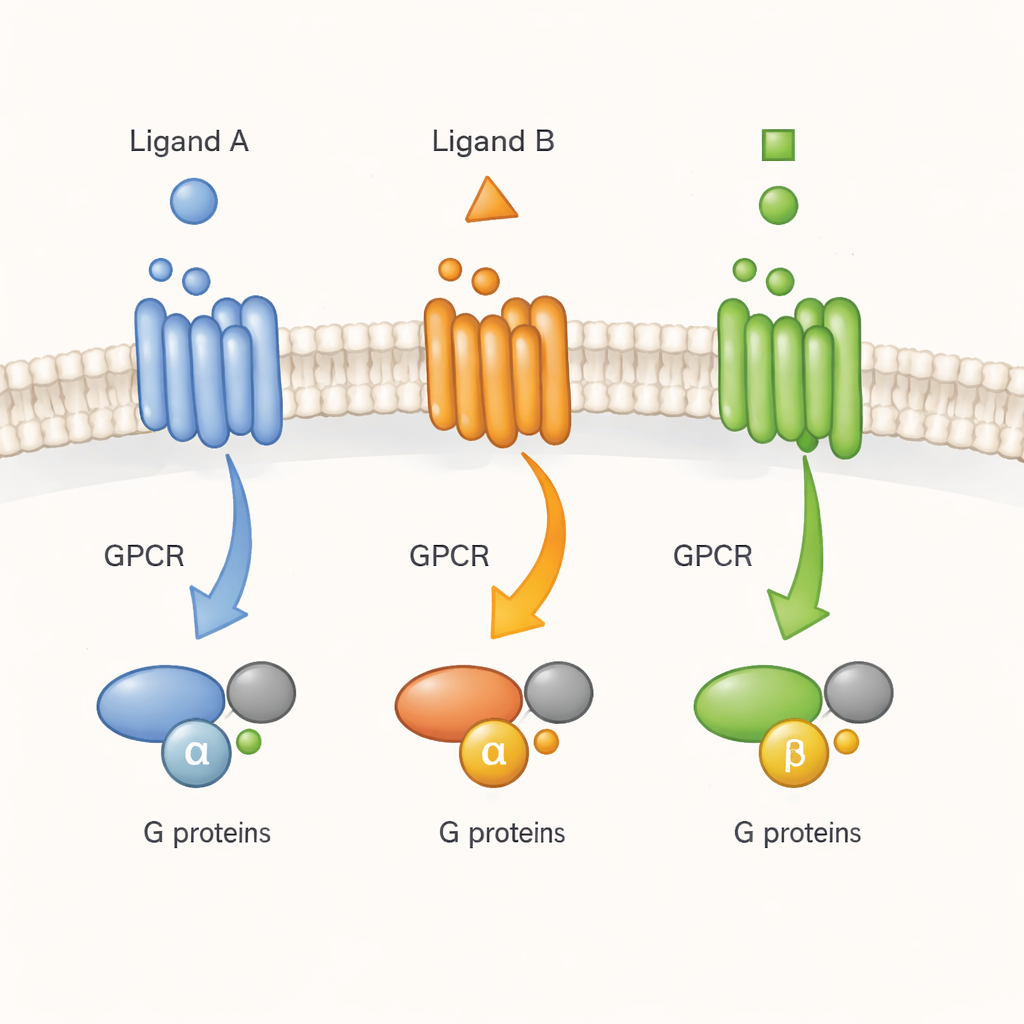
Die Türklingel einer Zelle in Echtzeit beobachten
GPCRs werden oft als molekulare Türklingeln beschrieben: Ein Signalmolekül (ein Ligand) läutet von außen, und der Rezeptor gibt die Nachricht an G-Proteine auf der Innenseite weiter. Frühere Arbeiten mit gereinigten Rezeptoren in Detergenzien hatten angedeutet, dass GPCRs nicht einfach zwischen einer inaktiven und einer aktiven Form umschalten. Stattdessen nehmen sie viele Formen ein, die Wirkstoffe in unterschiedlichem Maße stabilisieren können. Es war jedoch unklar, ob dieselbe Komplexität auch in der überfüllten, dynamischen Umgebung einer lebenden Zelle besteht. Hier konzentrieren sich die Autoren auf einen repräsentativen Rezeptor, den M2-muskarinischen Acetylcholinrezeptor, einen wichtigen Regulator von Herz- und Nervenaktivität, und fragen, ob unterschiedliche Liganden ihn in verschiedene aktive Formen treiben, die für die tatsächliche zelluläre Signalgebung relevant sind.
Kleine Lichtmelder an der Rezeptoroberfläche bauen
Um die Bewegungen des Rezeptors zu verfolgen, ohne seine normale Funktion zu stören, verwendete das Team die Erweiterung des genetischen Codes, eine Technik, die es erlaubt, eine spezielle designer-Aminosäure an ausgewählten Positionen auf der Außenfläche des Rezeptors einzufügen. Dieser chemische „Anker“ kann in lebenden Zellen an ein kleines fluoreszierendes Farbstoffmolekül gekoppelt werden. Durch das Abtasten von 72 Positionen und das Beibehalten nur jener, die sich wie normale Rezeptoren verhielten, bauten sie eine Reihe von sieben M2-Rezeptorvarianten, von denen jede einen einzelnen Farbstoff an einer anderen Außenschleifenstelle trug. Bei Zugabe des natürlichen Botenstoffs Acetylcholin stieg oder fiel an diesen Stellen die Farbstoffhelligkeit auf charakteristische Weise und zeigte, wie sich jeder Teil der äußeren Rezeptoroberfläche beim Einsetzen der Signalgebung verschob. Entscheidend ist, dass diese markierten Rezeptoren weiterhin G-Proteine aktivieren und normale Internalisierung durchlaufen konnten, was belegt, dass die Reporter treu und nicht störend waren.
Wirkstoffe hinterlassen unterschiedliche „konformationelle Fingerabdrücke“
Die Forscher verglichen dann mehrere Wirkstoffe, die alle den M2-Rezeptor aktivieren, jedoch mit unterschiedlicher Stärke: das körpereigene Acetylcholin, ein sehr starker synthetischer Agonist namens Iperoxo und zwei schwächere partielle Agonisten, Arecolin und Pilocarpin. Jeder Wirkstoff erzeugte ein einzigartiges Muster von Fluoreszenzänderungen über die sieben Reporterstellen hinweg — einen konformationellen Fingerabdruck. An den meisten Positionen korrelierte die Größe der Bewegung mit der Stärke der Rezeptoraktivierung. An zwei Stellen war die Beziehung jedoch invertiert: Die schwächeren Wirkstoffe bewirkten die größten Veränderungen, während der stärkste Wirkstoff nahezu keine Veränderung hervorrief. Ein solches Verhalten lässt sich nicht durch einen einzigen aktiven Zustand erklären. Stattdessen deutet es darauf hin, dass derselbe Rezeptor in lebenden Zellen mehrere unterschiedliche aktive Formen annehmen kann, von denen einige von starken Wirkstoffen bevorzugt werden und andere von schwachen.
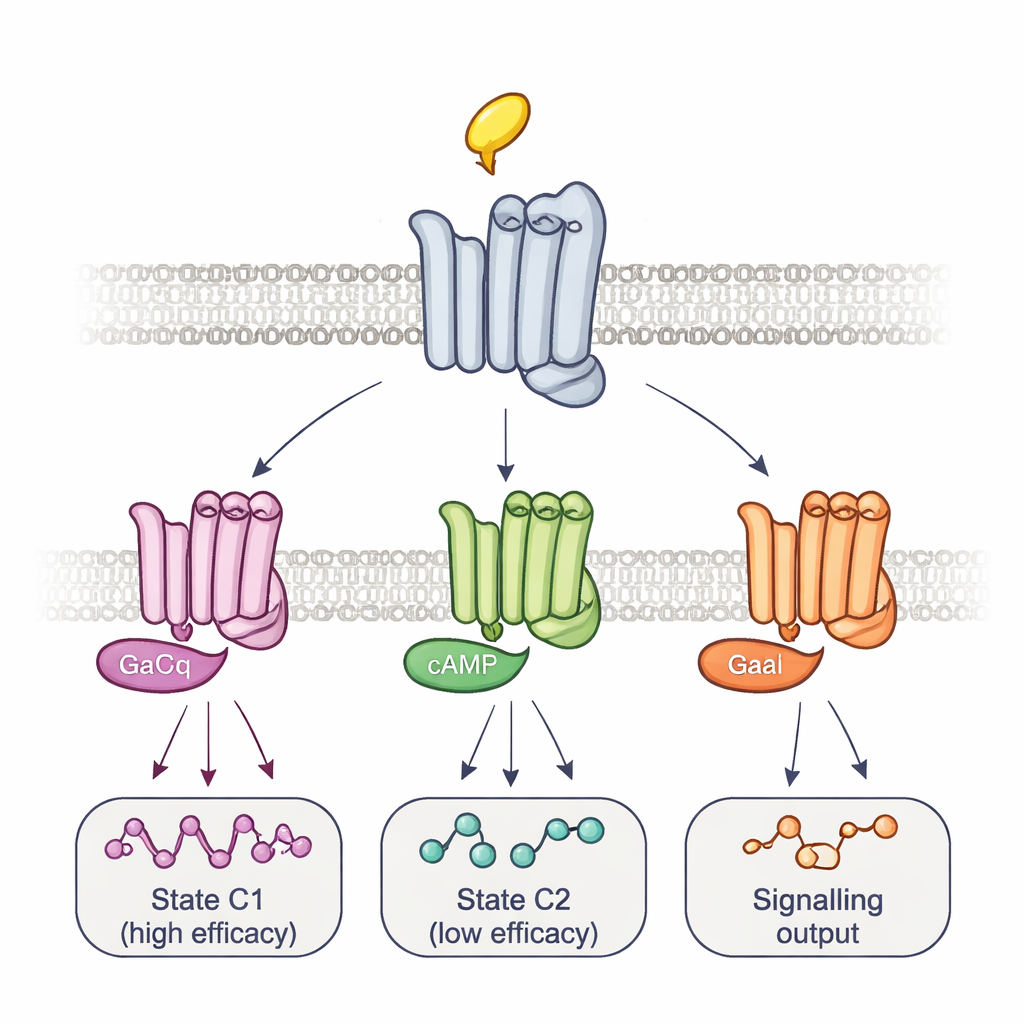
Mehrere Komplexe und zeitlich abgestimmte Wege zur Signalgebung
Um diese Formen mit der tatsächlichen Signalweiterleitung zu verknüpfen, veränderte das Team die G-Proteine selbst. Die Überexpression eines mutierten G-Proteins, das sehr enge, langlebige Komplexe mit Rezeptoren bildet, löschte selektiv das Signal an einigen Reporterstellen und verstärkte es an anderen. Dieses Muster zusammen mit dem zeitlichen Verlauf der Fluoreszenzänderungen enthüllte mindestens zwei Haupt-Rezeptor–G-Protein-Komplexe: einen schnell bildenden, hochwirksamen Komplex und einen langsameren, weniger wirksamen. Verschiedene Wirkstoffe verschoben das Gleichgewicht zwischen diesen Komplexen und nutzten sogar unterschiedliche Zwischenstufen, um dorthin zu gelangen, sodass ligandenspezifische Aktivierungstrajektorien verfolgt werden konnten. Mit einem separaten Biolumineszenz-Assay, der ein Panel von 14 G-Protein-Subtypen überwacht, zeigten die Autoren, dass diese Gleichgewichte nicht nur bestimmen, wie stark ein Wirkstoff die Signalgebung insgesamt aktiviert, sondern auch, welche konkreten G-Proteine eingeschaltet werden. Beispielsweise aktivierte Arecolin bevorzugt bestimmte Go-Proteine, während Pilocarpin stark den niedrigwirksamen Komplex begünstigte.
Warum das für bessere Medikamente wichtig ist
Für Nichtfachleute lautet die Kernbotschaft: Ein einzelner Rezeptor ist nicht einfach nur ein Schalter, sondern ein Cluster verwandter Schalter, die über unterschiedliche Wege erreichbar sind und jeweils leicht unterschiedliche nachgeschaltete Effekte auslösen. Diese Studie liefert eine direkte Sicht auf jene Wege und Zustände in intakten Zellen statt in vereinfachten Reagenzglas-Systemen. Durch die Kartierung, wie bestimmte Wirkstoffe den Rezeptor zugunsten spezifischer Komplexe und G-Protein-Partner beeinflussen, erhalten Forschende eine Blaupause für die Entwicklung „intelligenterer“ Medikamente — Verbindungen, die Rezeptoren in Zustände lenken, die hilfreiche Signale fördern und solche vermeiden, die mit Nebenwirkungen verbunden sind. Die hier entwickelte Strategie fluoreszenzbasierter Biosensoren sollte sich auf viele andere Rezeptoren übertragen lassen und ein Fenster in die Echtzeit-Choreographie der Wirkstoffwirkung in lebenden Zellen öffnen.
Zitation: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
Schlüsselwörter: GPCR-Signalübertragung, Ligandenwirksamkeit, G-Proteine, konformationelle Biosensoren, Arzneimittelentwicklung