Clear Sky Science · de
CFAP20 rettet angehaltene RNAPII aus dem Weg ko‑gerichteter Replisomen
Den Fluss unseres genetischen Verkehrs aufrechterhalten
Jedes Mal, wenn sich eine Zelle teilt, muss sie ihre gesamte DNA kopieren und gleichzeitig dieselben DNA‑Anweisungen weiterhin verwenden, um RNA herzustellen. Das ist, als würde man eine stark befahrene Autobahn neu asphaltieren, während der Verkehr noch rollt. Stoßen die Kopiermaschinerie und die Ablesemaschinerie zusammen, kann die DNA beschädigt werden — auf lange Sicht ein Beitrag zu Alterung und Erkrankungen, einschließlich Krebs. Diese Studie deckt ein kleines, aber entscheidendes Protein auf, CFAP20, das hilft, solche Staus zu verhindern und den Fluss genetischer Informationen glatt und sicher zu halten.
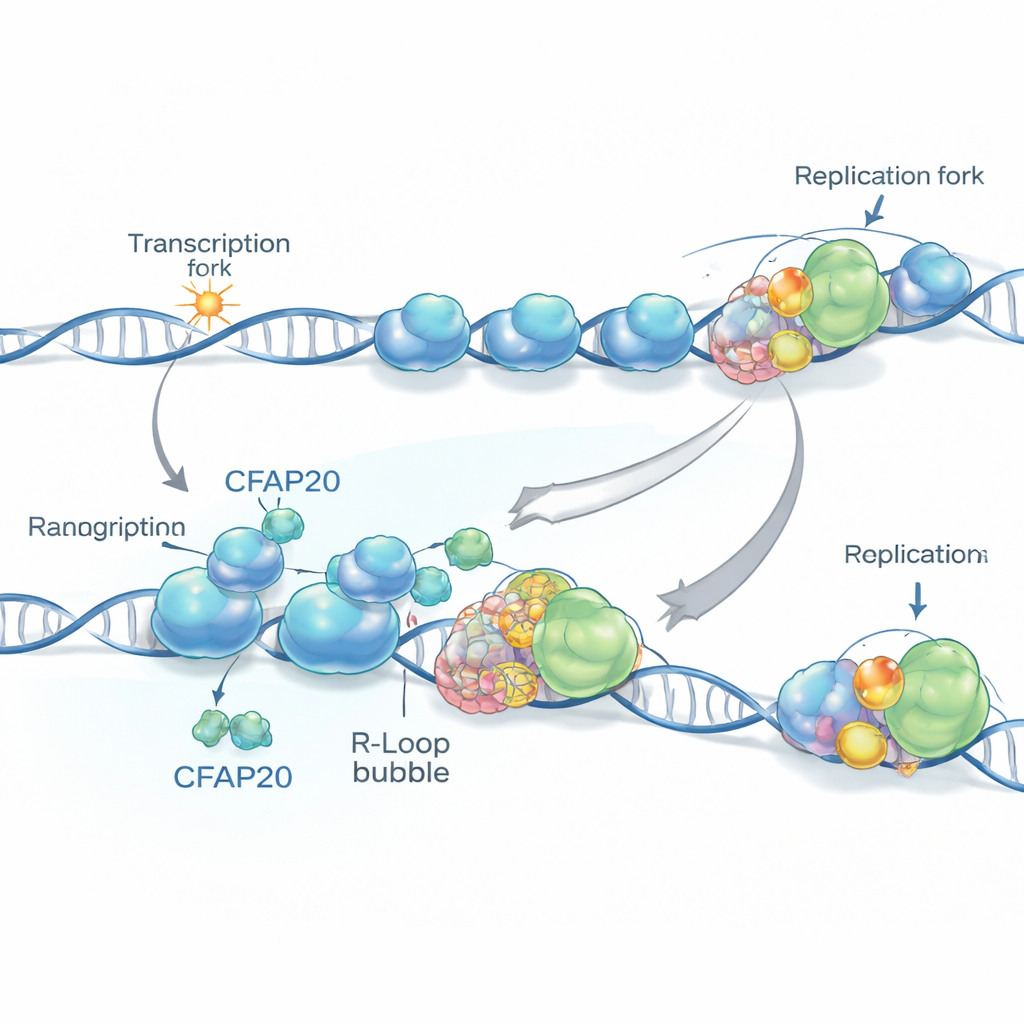
Zwei Aufgaben auf derselben DNA‑Autobahn
In unseren Zellen teilen sich zwei zentrale Aktivitäten die DNA‑„Straße“. Die eine ist die Replikation, bei der spezialisierte Komplexe die DNA vor der Zellteilung kopieren. Die andere ist die Transkription, bei der die RNA‑Polymerase II die DNA abliest, um RNA zu produzieren — der erste Schritt zur Proteinsynthese. Oft bewegen sich beide Maschinen in derselben Richtung entlang von Genen, besonders in der Nähe von Promotoren, den Startpunkten der Transkription, wo häufig auch die Replikation beginnt. Diese Anordnung wirkt geordnet, kann aber leicht verstopfen: Die RNA‑Polymerase pausiert oder bleibt oft nahe Promotoren stecken, und diese angehaltenen Komplexe können die von hinten kommende DNA‑Kopiermaschinerie blockieren.
Gefährliche DNA–RNA‑Verknüpfungen
Wenn die RNA‑Polymerase langsamer wird, kann die frisch entstandene RNA zurückschlagen und an die Vorlage‑DNA binden, wodurch dreisträngige Strukturen entstehen, sogenannte R‑Schleifen. Diese Strukturen sind natürlich und mitunter nützlich, werden aber in Überzahl zu gefährlichen Hindernissen. Mit genomeweiten Kartierungswerkzeugen zeigten die Forschenden, dass R‑Schleifen besonders häufig in der Nähe von Promotoren vorkommen, die nahe bei Replikationsstartpunkten liegen und in gleicher Richtung wie die Replikation orientiert sind. An diesen Stellen können eine angehaltene Ablesemaschine zusammen mit einer R‑Schleife ein mächtiges Hindernis für die Kopiermaschinerie darstellen und das Risiko für Brüche und Lücken in der DNA erhöhen.
Ein kleines Protein mit großer Schutzfunktion
Um Faktoren zu finden, die Zellen beim Umgang mit Stress auf beiden Seiten — Ablesen und Kopieren — helfen, nutzte das Team groß angelegte CRISPR‑Gen‑Knockout‑Screens. CFAP20, zuvor hauptsächlich für seine Rolle in winzigen, haarähnlichen Zellstrukturen (Cilien) bekannt, erwies sich als überraschender Treffer. Entfernten die Forschenden CFAP20 aus menschlichen Zellen, häuften sich R‑Schleifen in Promotor‑Nähe, Replikationsgabeln beschleunigten ungewöhnlich zwischen gestörten Regionen, und insgesamt feuerten weniger Replikationsstartpunkte. Das Ergebnis war ein ungleichmäßiges Replikationsmuster, bei dem manche Gabeln steckenblieben, während benachbarte vorausrasenden und verwundbare einsträngige Lücken hinterließen. Eine krebsassoziierte mutantische Variante von CFAP20 konnte diese Probleme nicht verhindern, was die spezifische Schutzfunktion des Proteins im Kern unterstreicht, getrennt von seiner Rolle in Cilien.
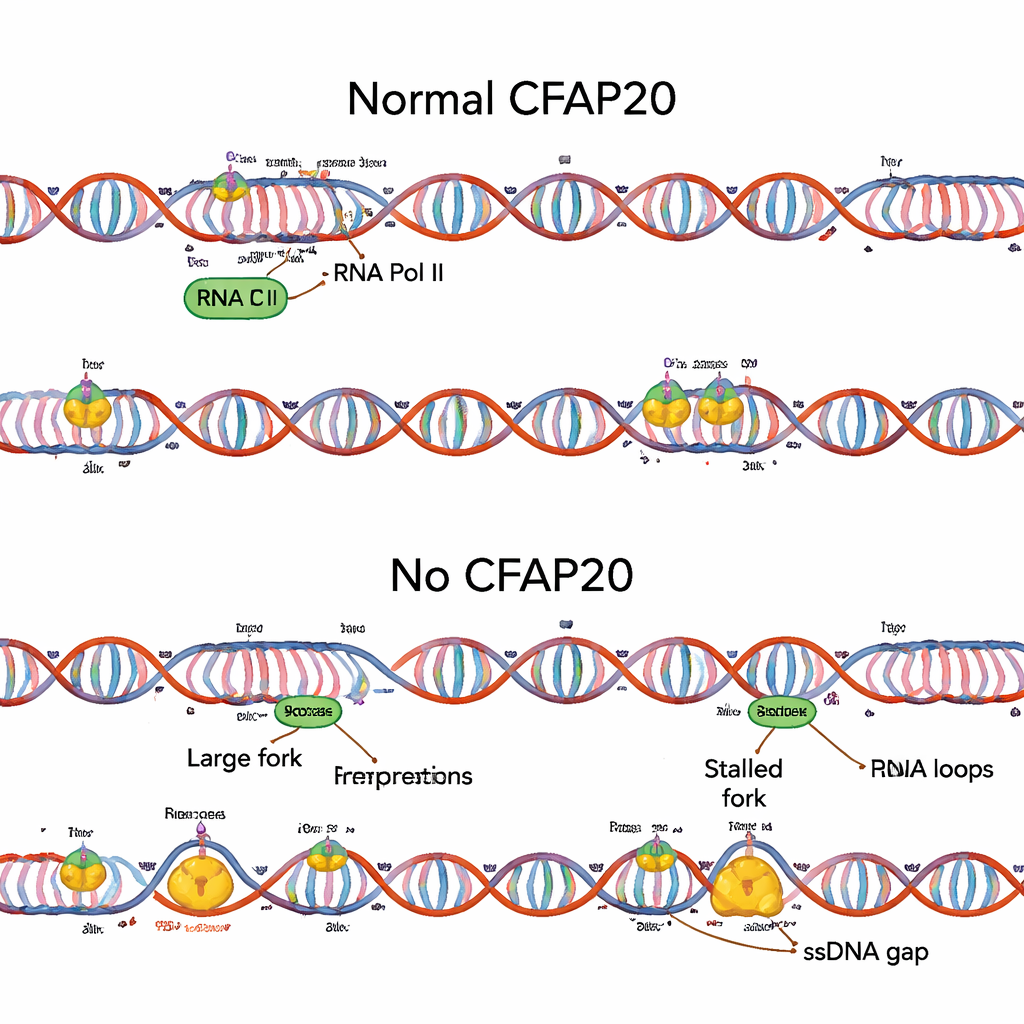
Starke Transkription mit sicherer Replikation in Einklang bringen
Die Studie untersuchte zudem, wie CFAP20 mit Mediator interagiert, einem großen Komplex, der die Aktivität der RNA‑Polymerase II an Promotoren verstärkt. Ohne CFAP20 wird Mediator‑getriebene hohe Transkription zur Belastung: R‑Schleifen nehmen zu und die Replikation gerät durcheinander. Interessanterweise verschwanden viele der schädlichen Effekte des CFAP20‑Verlusts, wenn die Forschenden eine Mediator‑Untereinheit deaktivierten, die diese starke Transkription antreibt. R‑Schleifen gingen zurück, die Geschwindigkeit der Replikationsgabeln normalisierte sich und die Kopiermuster der DNA wurden regelmäßiger. Weitere Experimente zeigten, dass CFAP20 physisch mit der RNA‑Polymerase II assoziiert und dabei hilft, langsame oder angehaltene Polymerasen, die mit R‑Schleifen verheddert sind, zu lösen — im Grunde räumt es die Strecke, bevor die Kopiermaschinerie eintrifft.
Warum das für Gesundheit und Krankheit wichtig ist
Vereinfacht gesagt wirkt CFAP20 wie ein Verkehrsmanager auf unserer DNA, der angehaltene Ablesemaschinen rettet, sodass sie das Kopieren nicht behindern und keine gefährlichen Lücken erzeugen. Fehlt CFAP20 oder ist es defekt, lösen lokale Staus in Promotor‑Nähe kompensatorisches Beschleunigen an anderen Stellen aus, was paradoxerweise die Genomstabilität schwächt. Da viele Tumoren eine verstärkte Transkription und Replikationsstress aufweisen, könnten sie besonders abhängig von diesem Schutzprotein sein. Zu verstehen, wie CFAP20 diese beiden essentiellen Prozesse koordiniert, klärt nicht nur einen grundlegenden Aspekt der Zellbiologie, sondern könnte auch neue Verwundbarkeiten aufdecken, die in bestimmten Krebsarten therapeutisch genutzt werden könnten.
Zitation: Uruci, S., Boer, D.E.C., Chrystal, P.W. et al. CFAP20 salvages arrested RNAPII from the path of co-directional replisomes. Nature 650, 1025–1034 (2026). https://doi.org/10.1038/s41586-025-09943-7
Schlüsselwörter: DNA-Replikation, Transkription, R‑Schleifen, Genomstabilität, CFAP20