Clear Sky Science · de
Krankheitstoleranz und Pathogenese von Infektionen: altersbedingte Zielkonflikte bei Mäusen
Warum manche Infektionen im Alter tödlicher sind
Warum kommen ältere Erwachsene bei schweren Infektionen so oft schlechter davon, selbst wenn sie denselben Erregern ausgesetzt sind wie Jüngere? Diese Studie nutzt Mäuse, um dieses Rätsel zu untersuchen, mit Fokus auf Sepsis – eine lebensbedrohliche Reaktion auf Infektion. Die Forschenden zeigen, dass körpereigene Schutzprogramme mit dem Alter umschlagen können: Gene, die in der Jugend Herz und andere Organe vor Schaden bewahren, können im höheren Alter tatsächlich schädlich wirken. Das Verständnis dieses altersabhängigen Umschlags könnte beeinflussen, wie wir Behandlungen für Infektionen bei Kindern, Erwachsenen und älteren Menschen gestalten.
Unterschiedliche Verläufe bei derselben Infektion
Um einen häufigen menschlichen Notfall nachzuahmen, infizierte das Team junge und alte Mäuse mit einer Mischung aus zwei häufigen Sepsis verursachenden Bakterien, Escherichia coli und Staphylococcus aureus. Sie wählten sorgfältig eine Dosis, die etwa die Hälfte der Tiere tötete (eine LD50), sodass einige Mäuse überleben und andere nicht, obwohl die Ausgangsexposition gleich war. Überraschenderweise trugen beide Altersgruppen ähnliche Bakterienmengen in ihren Organen. Unterschiedlich war, wie ihre Körper mit dem Schaden umgingen. Junge und alte Mäuse durchliefen bei Sepsis unterschiedliche „Gesundheitsverläufe“: Körpertemperatur, sichtbare Krankheitssymptome und der Zeitpunkt von Verschlechterung oder Erholung teilten sich klar in Überlebens- und Nichtüberlebens‑Trajektorien. 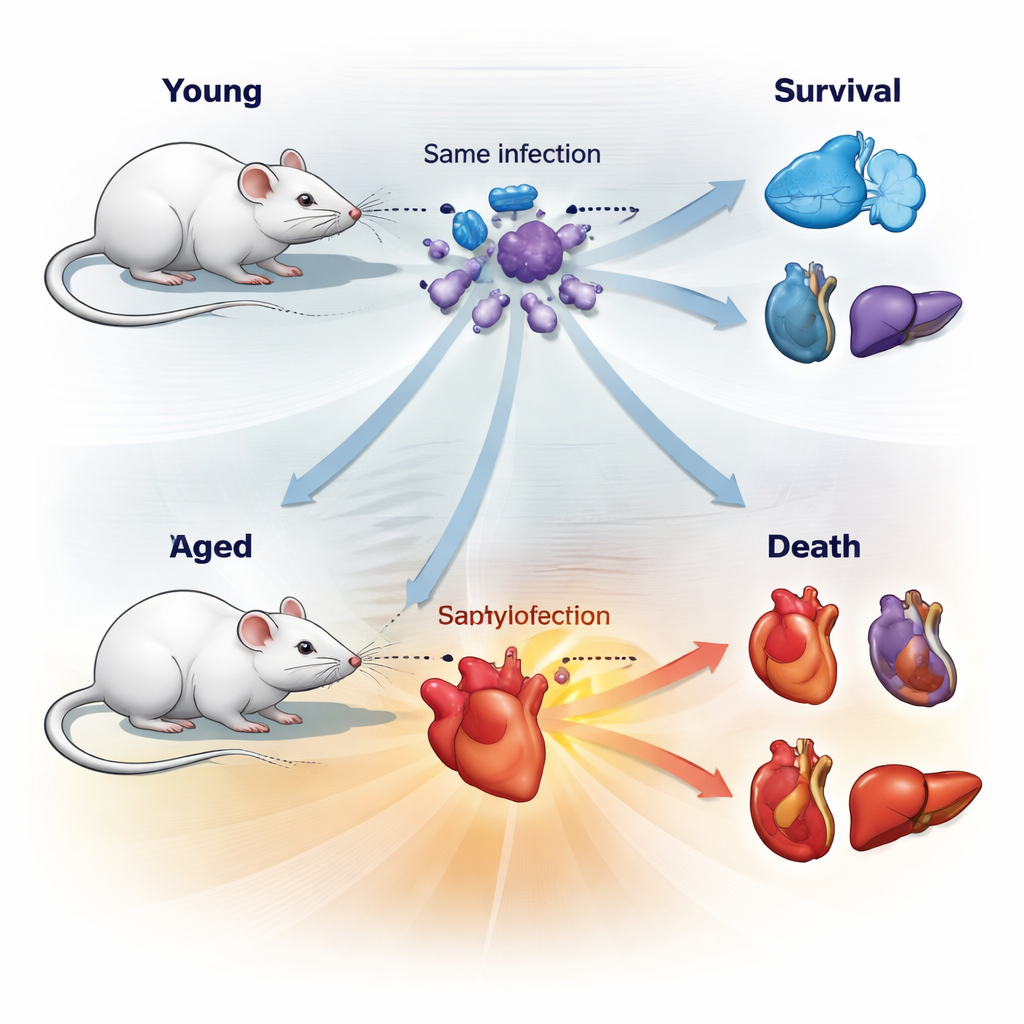
Herzveränderungen erzählen zwei alterspezifische Geschichten
Bei der Untersuchung der Organe trat das Herz als zentraler Akteur hervor. Junge Mäuse, die an Sepsis starben, entwickelten vergrößerte, geschwollene Herzen mit gedehnten Kammern – Zeichen starker Belastung – und zeigten hohe Werte von Blutmarkern, die in Kliniken auf Herzschädigung und Herzversagen hinweisen. Nieren und Leber waren ebenfalls geschädigt, jedoch weniger dramatisch. Im Gegensatz dazu zeigten alte Mäuse, die starben, das entgegengesetzte Herzbild: Ihre Herzen wurden kleiner und atrophisch, während Nierenschäden und Funktionsverluste ausgeprägter waren. Alte Überlebende hatten interessanterweise oft vergrößerte Herzen, aber insgesamt weniger Schaden. Die Genaktivitätsprofile des Herzgewebes bestätigten, dass junge und alte Mäuse unterschiedliche Umbauprogramme aktivierten: Jüngere Herzen schalteten Wege an, die mit Wachstum und struktureller Veränderung verbunden sind, während ältere Herzen Pfade hochfuhren, die mit Proteinabbau und Zellatrophie verknüpft sind.
Ein Schutzkreis in jungen Herzen
Bei der Analyse dieser molekularen Signaturen hoben die Forschenden ein Steuerungsgen namens Foxo1 und eines seiner Ziele, Trim63, hervor, das ein Protein kodiert, bekannt als MuRF1, das an der Markierung von Muskelproteinen für den Abbau beteiligt ist. In Herzen überlebender junger Mäuse waren Foxo1 und Trim63 deutlich stärker aktiviert als bei jungen Mäusen, die starben oder nie infiziert wurden. Die Blockade von FoxO1 mit einem Wirkstoff oder das gezielte Entfernen dieses Gens in Herzmuskelzellen machte junge Mäuse deutlich anfälliger für Krankheit und Tod, obwohl sich ihre Bakterienlast und entzündlichen Signale kaum veränderten. Ebenso litten junge Mäuse ohne Trim63 an stärkerer Herzschwellung, vermehrtem Austritt von Herzschädigungsmarkern ins Blut und weitreichenderen Schäden an Leber und Nieren. Diese Ergebnisse deuten darauf hin, dass der FoxO1–Trim63‑Weg in der Jugend als ein Krankheitstoleranzsystem wirkt: Er bekämpft die Erreger nicht direkt, sondern hilft dem Herzen, sich an Stress anzupassen und ein Multi‑Organ‑Versagen zu verhindern.
Wenn der Beschützer von gestern zur Gefahr von heute wird
Die gleichen Gene erzählten im Alter eine andere Geschichte. Bei alten Mäusen hing das Überleben nicht mehr davon ab, FoxO1 im Herzen hochzufahren. Stattdessen schützte das Abschalten von FoxO1 – entweder genetisch in Muskelzellen oder mit einem Wirkstoff – ältere Tiere tatsächlich vor sepsisbedingter Krankheit und Tod. Alte Mäuse ohne Trim63 oder solche, die mit einem MuRF1‑Hemmer behandelt wurden, kamen ebenfalls besser davon: Sie hatten vergrößerte, aber strukturell gesündere Herzen, niedrigere Blutwerte von Markern für Herzbelastung und weniger Schäden an Nieren und Leber. Anders gesagt: Der Kreislauf, der in jungen Herzen eine gesunde Anpassung an Infektionen fördert, trieb in älteren Herzen nun schädlichen Umbau und Organverletzung voran. Dieser altersabhängige Funktionsumschlag passt zu einem Konzept aus der Evolutionsbiologie, der „antagonistischen Pleiotropie“, wonach Eigenschaften, die in frühem Leben die Fitness steigern, später verborgene Kosten mit sich bringen können. 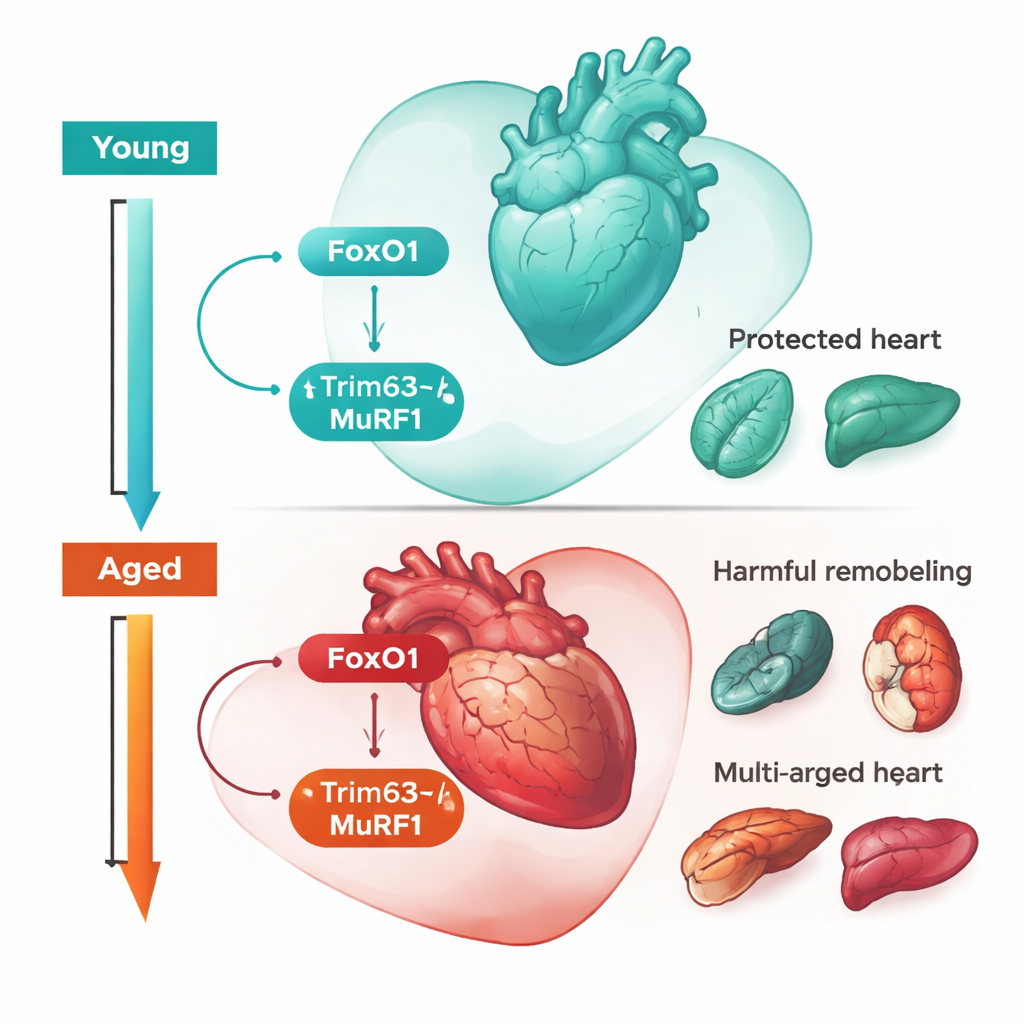
Was das für die Behandlung von Infektionen über die Lebensspanne bedeutet
Für eine nichtfachliche Leserschaft lautet die Kernbotschaft, dass die Bekämpfung schwerer Infektionen wie Sepsis nicht nur darin besteht, Keime zu töten – es geht auch darum, wie unsere Organe den Sturm überstehen. Diese Studie zeigt, dass die Stressreaktionsmaschinerie des Herzens, zentriert um FoxO1 und Trim63, jungen Körpern hilft, Infektionen zu tolerieren, im Alter aber zur Belastung werden kann. Folglich könnte ein Wirkstoff, der diesen Weg blockiert, für einen älteren Patienten lebensrettend sein, für einen jüngeren jedoch gefährlich. Die Arbeit unterstreicht, dass Therapien für Infektionskrankheiten altersangepasst sein sollten und berücksichtigt werden muss, dass dasselbe Gen zwei Gesichter haben kann: Beschützer in der Jugend, Störenfried im Alter.
Zitation: Sanchez, K.K., McCarville, J.L., Stengel, S.J. et al. Disease tolerance and infection pathogenesis age-related tradeoffs in mice. Nature 650, 727–735 (2026). https://doi.org/10.1038/s41586-025-09923-x
Schlüsselwörter: Sepsis, Altern, Krankheitstoleranz, Herzumgestaltung, FoxO1-Trim63-Weg