Clear Sky Science · de
Zweiseitige CRISPR-Screens entschlüsseln einen GLIS3‑abhängigen fibrotischen Zellkreis
Wenn Heilung in schädliche Vernarbung umschlägt
Unser Darm ist darauf ausgelegt, sich nach jeder Schürfwunde und Reizung selbst zu reparieren. Bei chronischen Erkrankungen wie Morbus Crohn und Colitis ulcerosa kann dieser Heilungsprozess jedoch aus dem Ruder laufen und dichte, starre Narbenmasse bilden, die den Darm verengt und oft operativ behandelt werden muss. Diese Studie enthüllt einen bislang verborgenen Dialog zwischen Immunzellen und strukturellen Zellen im Darm, der diese Vernarbung antreibt, und identifiziert einen Schaltergen namens GLIS3, das einen neuen Ansatzpunkt bieten könnte, um den Teufelskreis zu durchbrechen.
Ein verborgenes Netzwerk in entzündeten Därmen
Um zu verstehen, warum manche Patientinnen und Patienten hartnäckige Entzündungen und Fibrosen entwickeln, erstellten die Forschenden einen zellulären „Atlas“ des menschlichen Darms. Sie kombinierten Einzelzell‑RNA‑Sequenzierung, die die in einzelnen Zellen aktiven Gene erfasst, mit räumlicher Profilierung, die zeigt, wo diese Zellen in Gewebeschnitten sitzen. Anhand von Proben aus Fällen von Morbus Crohn, Colitis ulcerosa und Kontrollen kartierten sie mehr als vier Millionen Zellen durch die Darmwand. Innerhalb dieses Zellensembles stach eine Fibroblasten‑Untergruppe hervor: entzündungsassoziierte Fibroblasten, kurz IAFs. Diese Zellen sammelten sich in Bereichen aktiver und chronischer Kolitis und trugen ein Genprofil, das mit Resistenz gegen gängige Anti‑TNF‑Therapien verknüpft ist, was darauf hindeutet, dass sie eine zentrale Rolle bei schwer behandelbaren Verläufen spielen. 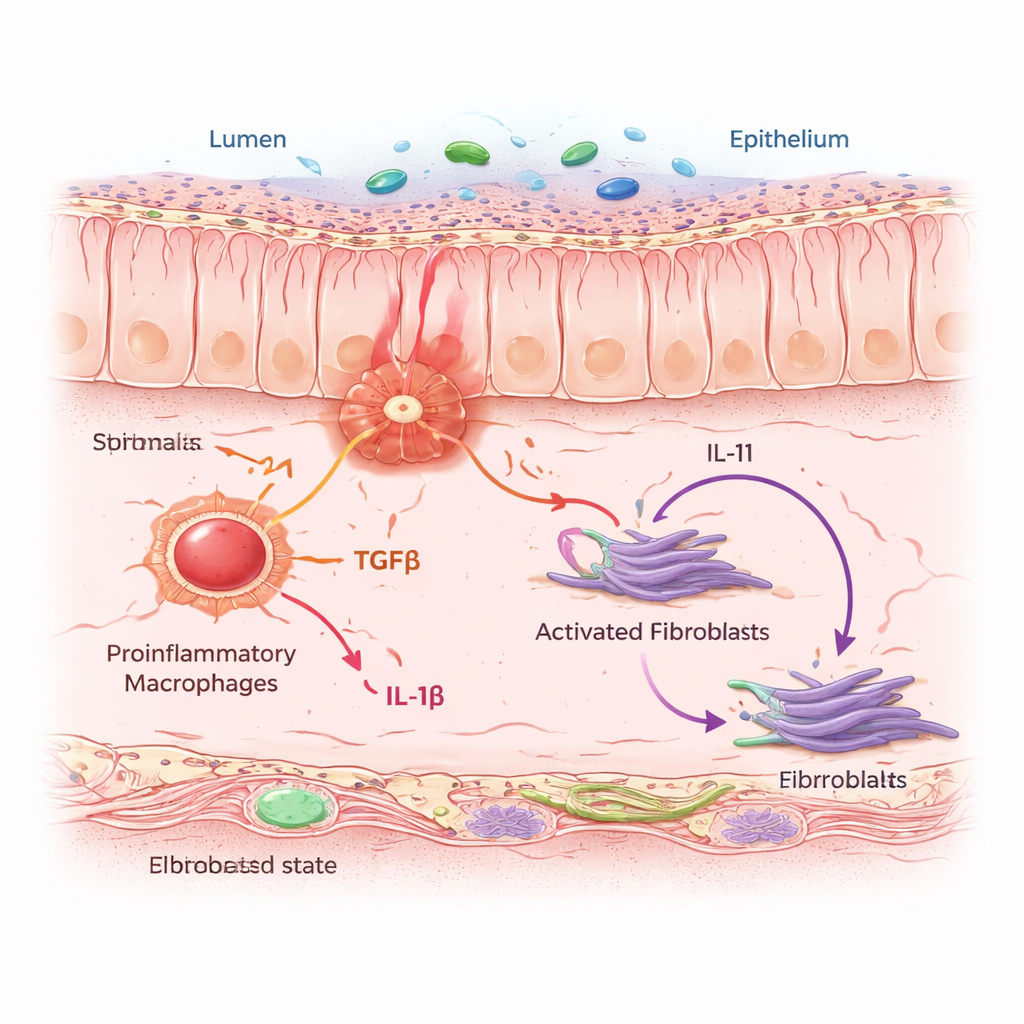
Makrophagen flüstern, Fibroblasten vernarben
IAFs agierten nicht allein. Sie traten in „Nachbarschaften“ auf, die dicht von proinflammatorischen Makrophagen bevölkert waren — Immunzellen, die Gefahren erkennen und Alarmsignale aussenden. Mit Hilfe computergestützter Modelle und Zell‑Co‑Kultur‑Experimenten zeigte das Team, dass entzündlich aktivierte Makrophagen zwei entscheidende Botenproteine ausschütten: TGFβ und IL‑1β. Nahegelegene Fibroblasten nehmen diese Signale über spezifische Rezeptoren auf. Wenn beide Signale zusammen eintreffen, schalten Fibroblasten in den IAF‑Zustand und beginnen, IL‑11 zu produzieren — ein Zytokin, das bereits mit Fibrose in Verbindung gebracht wird — sowie Kollagen und andere Matrixproteine, die die Darmwand verdicken und versteifen. Bei Mäusen, die einem chronischen Kolitis‑Protokoll ausgesetzt wurden, reduzierte das Blockieren von IL‑11 oder dessen selektive Entfernung in Fibroblasten die Kollagenablagerung, ohne die anfängliche Entzündung zu verhindern, was zeigt, dass IL‑11 ein entscheidender Treiber der Vernarbungsphase ist.
GLIS3: Der Master‑Schalter in fibrotischen Fibroblasten
Um von Korrelationen zu Mechanismen vorzudringen, setzten die Autoren leistungsfähige genomweite CRISPR‑Werkzeuge ein. Sie konstruierten menschliche Fibroblasten so, dass die IL‑11‑Produktion über ein fluoreszierendes Tag verfolgt werden konnte, und führten parallele Screens durch, bei denen Gene entweder ausgeschaltet oder aktiviert wurden. Durch Sortierung der Zellen, die nach TGFβ‑ und IL‑1β‑Stimulation ungewöhnlich hohe oder niedrige IL‑11‑Mengen produzierten, identifizierten sie Gene, die diese Antwort steuern. Unter vielen Signalübertragungs‑Komponenten trat ein Transkriptionsfaktor hervor — GLIS3 — als zentraler Regulator. Wurde GLIS3 deaktiviert, produzierten Fibroblasten deutlich weniger IL‑11; wurde es verstärkt, stieg IL‑11 massiv an. Weitere Experimente zeigten, dass GLIS3 als Reaktion auf Makrophagen‑Signale in den Zellkern der Fibroblasten gelangt, direkt an DNA‑Regionen in der Nähe des IL11‑Gens und anderer Gene bindet und ein weites Programm entzündlicher und fibrotischer Gene aktiviert, einschließlich Kollagenen und Faktoren, die weitere Immunzellen anlocken. 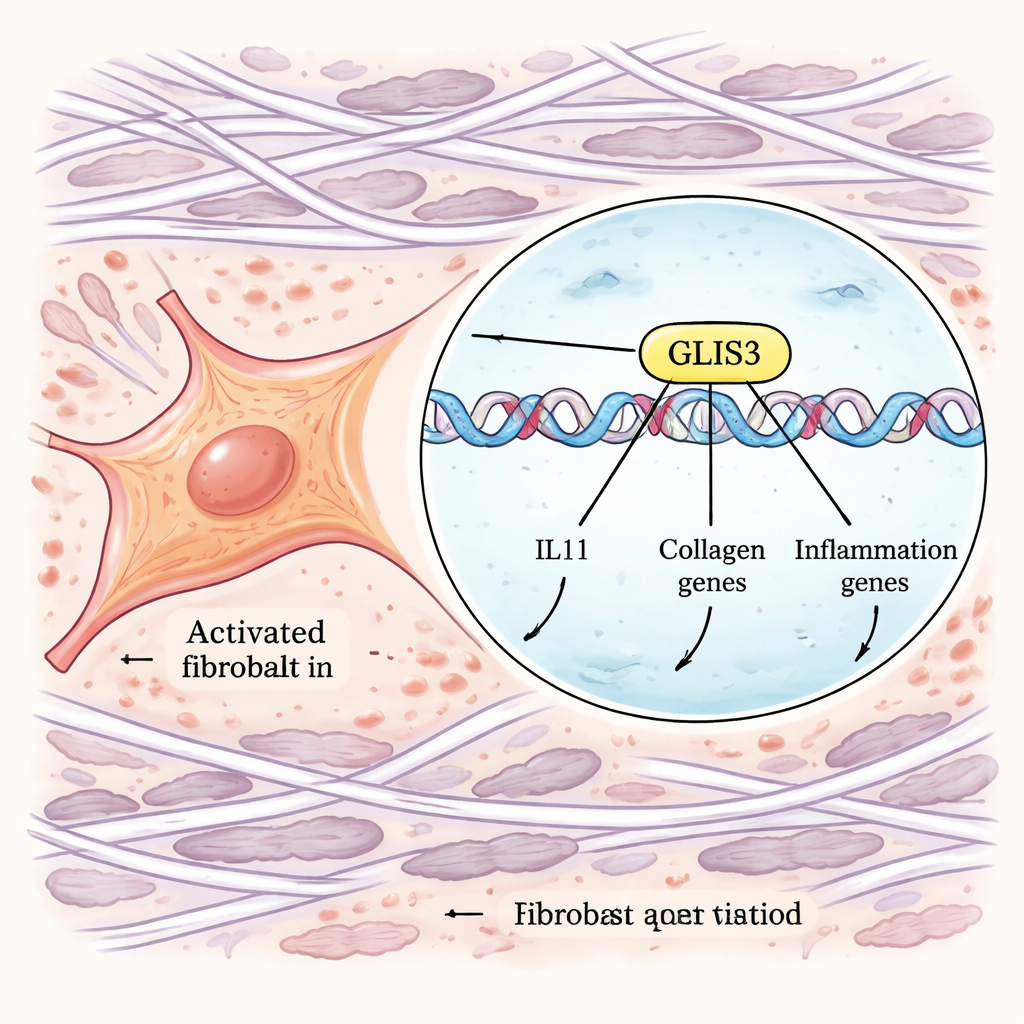
Von Mausmodellen bis zur Schwere bei Patienten
Dann prüften die Forschenden, ob dieses GLIS3‑gesteuerte Programm in lebenden Organismen eine Rolle spielt. In Mäusen erzeugten sie eine Linie, in der GLIS3 nur in Fibroblasten entfernt werden konnte. Wurden diese Tiere chronischer Kolitis ausgesetzt, zeigten sie weniger Darmvernarbung, geringere Kollagen‑ und fibrotische Genexpression und weniger Entzündung im Vergleich zu normalen Mäusen. Räumliche Kartierungen bestätigten, dass GLIS3‑defiziente Mäuse weniger IL‑11‑produzierende Fibroblasten sowie weniger aktivierte Makrophagen und Neutrophile in der Nähe hatten, was darauf hinweist, dass eine Störung von GLIS3 den gesamten entzündlich‑fibrotischen Kreislauf abschwächt. In einer großen pädiatrischen Colitis‑ulcerosa‑Kohorte leiteten die Autorinnen und Autoren eine GLIS3‑„Signatur“ von 50 Genen ab und fanden, dass deren Aktivität in Kolonbiopsien eng mit dem Schweregrad der Erkrankung sowie der Häufigkeit von IAFs und aktivierten Makrophagen korrelierte — ein direkter Anschluss dieses Weges an Patientenergebnisse.
Den Kreislauf von Entzündung und Vernarbung durchbrechen
Für Nicht‑Spezialisten lautet die Kernbotschaft: Diese Arbeit zeigt eine sich selbst verstärkende Schleife auf — entzündliche Makrophagen veranlassen Fibroblasten, zu narbenbildenden IAFs zu werden; diese IAFs produzieren unter Kontrolle von GLIS3 IL‑11, Kollagen und andere Faktoren, die das Gewebe umbauen und weitere entzündliche Zellen anziehen. Breite Immunsuppressiva unterbrechen diesen Kreislauf möglicherweise nicht vollständig, was erklärt, warum viele Patientinnen und Patienten langfristig auf bestehende Therapien versagen. Indem die Studie GLIS3 und den IL‑11‑produzierenden Fibroblasten‑Zustand als zentrale Knotenpunkte im Entzündungs‑Fibrose‑Netz identifiziert, weist sie auf gezieltere Strategien hin — die Fibroblasten statt ausschließlich Immunzellen adressieren —, die eines Tages verhindern oder rückgängig machen könnten, dass es bei chronisch‑entzündlichen Darmerkrankungen zu nachhaltiger Vernarbung kommt.
Zitation: Pokatayev, V., Jaiswal, A., Shih, A.R. et al. Bidirectional CRISPR screens decode a GLIS3-dependent fibrotic cell circuit. Nature 650, 997–1006 (2026). https://doi.org/10.1038/s41586-025-09907-x
Schlüsselwörter: chronisch‑entzündliche Darmerkrankung, intestinales Fibrose, Fibroblasten, Makrophagen, GLIS3