Clear Sky Science · de
Stress steuert die Vererbung von Heterochromatin über Ubiquitinierung von Histon H3
Wie Zellen sich an Stress erinnern
Unsere Zellen brauchen Mechanismen, um sich an frühere Stressereignisse — etwa Hitze, Nährstoffmangel oder Medikamentenkontakt — zu „erinnern“, damit sie beim nächsten Mal schneller reagieren können. Ein mächtiges Gedächtnissystem beruht auf Heterochromatin: dicht verpackter DNA, die bestimmte Gene über viele Zellteilungen hinweg abgeschaltet hält. Diese Arbeit untersucht, wie Zellen dieses Gedächtnis aktiv an Stress anpassen und zeigt einen molekularen Knotenpunkt, der Umweltsignale mit langanhaltenden Veränderungen der Genaktivität verknüpft. Das Verständnis dieses Steuermechanismus kann helfen zu erklären, wie Pilze Resistenzen gegen Medikamente entwickeln und wie Stress das epigenetische Profil unserer eigenen Zellen umgestaltet.
Ein Schloss auf dem Genom
Man kann Heterochromatin als molekulares Schloss auf Abschnitten der DNA betrachten, das benachbarte Gene stumm schaltet. Dieses Schloss entsteht durch chemische Markierungen an Histonproteinen, vor allem durch eine Modifikation namens H3K9me3. Ist sie erst etabliert, kopiert sie sich bei jeder DNA‑Replikation und erlaubt so die Vererbung von Genrepressionen, ohne die zugrunde liegende DNA‑Sequenz zu verändern. Bisher legten die meisten Arbeiten nahe, dass dieses Selbstkopieren hauptsächlich auf einer „Lesen‑Schreiben“‑Rückkopplung beruht: Ein Enzymkomplex erkennt vorhandene H3K9me3‑Marken und fügt benachbarten Histonen dieselbe Marke hinzu, wodurch sich der stille Bereich allmählich ausbreitet. Dieses Modell konnte jedoch nicht vollständig erklären, wie Umweltbedingungen die Geschwindigkeit, das Ausmaß oder die Richtung dieser Heterochromatin‑Ausbreitung beeinflussen.
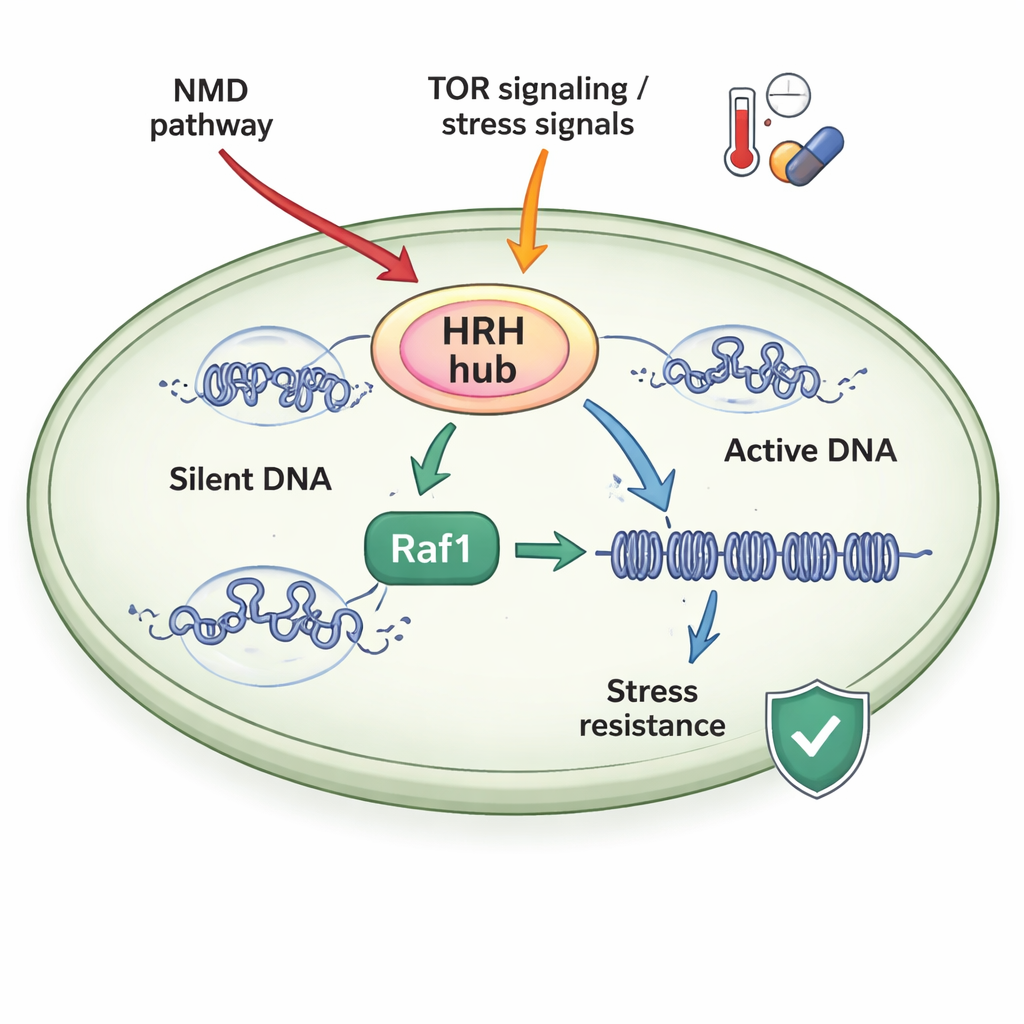
Ein stress‑sensitiver Steuerknoten
Die Autoren arbeiteten mit der Spaltpilzhefe (fission yeast), einem einfachen Modellorganismus, dessen Chromatinapparat dem höherer Organismen ähnelt. Sie konzentrierten sich auf einen Komplex namens ClrC, der sowohl die H3K9me3‑Marke setzt als auch an einer anderen Position auf Histon H3 ein kleines Protein, Ubiquitin, anheftet (H3K14ub). Eine wichtige Untereinheit von ClrC, Raf1, fungiert als limitierender „Wächter“: Ist Raf1 knapp, liegt viel des Hauptenzymes (Clr4) frei vor statt im Komplex an Chromatin gebunden, und die stillen Bereiche können sich nicht ausbreiten. Ist Raf1 hingegen ausreichend vorhanden, bildet sich mehr ClrC und bindet stabil an DNA, sodass H3K14ub‑ und H3K9me3‑Marken entlang der Chromosomen erweitert werden und die Genstilllegung verstärken.
Feinabstimmung des Schlosses mit Ubiquitin
Durch das kartieren von Chromatinmarken im gesamten Genom zeigten die Forscher, dass H3K14ub dort stark angereichert ist, wo Heterochromatin entsteht, und dass diese Marke praktisch verschwindet, wenn Raf1 entfernt wird. Tragen Zellen eine Mutation, die den Ubiquitin‑Anhang verhindert (während die H3K9me3‑Marke am Ausgangspunkt erhalten bleibt), können sich die stillen Bereiche nicht nach außen ausbreiten. Mit anderen Worten: H3K14ub ist nicht bloß dekorativ, sondern notwendig, damit die Heterochromatin‑Front voranschreitet. Biochemische und Bildgebungs‑Experimente erklären warum: H3K14ub steigert die Aktivität des Clr4‑Enzyms deutlich und hilft, den gesamten Komplex auf dem Chromatin zu verankern, wodurch die lokale Dichte von H3K9me3 über die Schwelle gehoben wird, die für stabile Vererbung nötig ist. Bemerkenswerterweise kann eine Erhöhung der Raf1‑Menge mehrere sonst erforderliche Faktoren ersetzen, die zur Aufrechterhaltung dieser stillen Bereiche nötig sind — ein Hinweis darauf, dass Raf1‑getriebene Ubiquitinierung ein zentrales Stellrad ist.
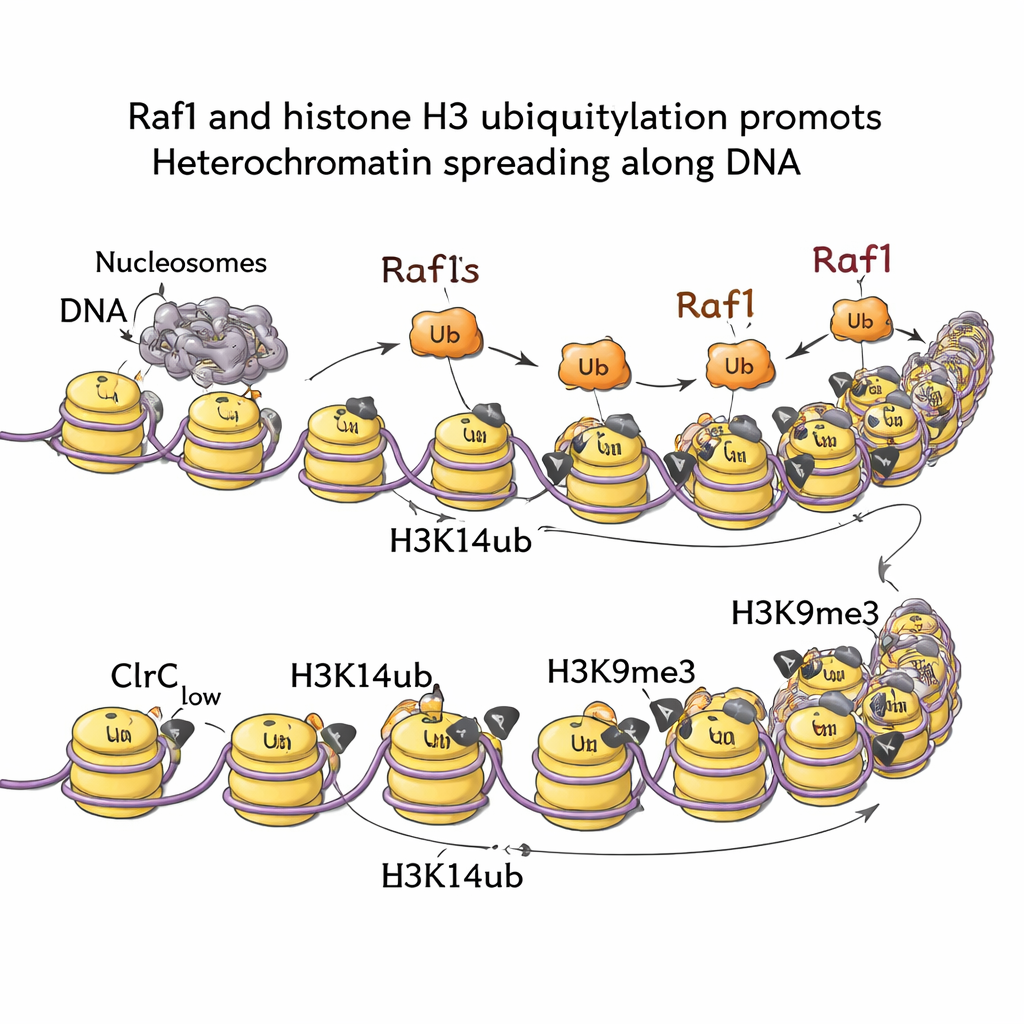
Signale aus RNA‑Abbau‑ und Wachstumswegen
Zellen überlassen Raf1‑Spiegel nicht dem Zufall. Die Studie zeigt, dass zwei wichtige stressantwortfähige Systeme in das, was die Autoren als heterochromatin‑Vererbbarkeits‑Regulationszentrum (HRH) bezeichnen und das um Raf1 zentriert ist, einfließen. Erstens zielt der Nonsense‑vermittelte Abbau (NMD) — bekannt dafür, fehlerhafte mRNAs zu zerstören — auf die Boten‑RNA für Raf1 ab und hält Raf1‑Spiegel unter normalen Bedingungen niedrig. Wird NMD ausgeschaltet, stabilisiert sich die Raf1‑RNA, die Raf1‑Proteinmenge steigt und die Heterochromatin‑Ausbreitung wird in Mutanten wiederhergestellt, die sonst keine stillen Bereiche erhalten könnten. Zweitens fördert ein Wachstums‑ und Stresssensor namens TORC2 über die Kinase Gad8 die Raf1‑Expression. Hohe Temperatur schaltet diesen Weg ab, senkt Raf1‑Spiegel, schwächt Heterochromatin und erschwert es den Zellen, stille Zustände zu bewahren, sofern Raf1 nicht experimentell erhöht wird.
Stress, Medikamentenresistenz und weiterreichende Folgen
Die Autoren verbinden diesen molekularen Knotenpunkt mit realen Anpassungsphänomenen. Die Exposition von Hefezellen gegenüber Koffein — einem Stress, der in anderen Systemen ebenfalls NMD abschwächt — erhöht Raf1‑Spiegel und fördert die Ausbreitung von Heterochromatin an neue Stellen, einschließlich Genen, deren Stilllegung Resistenz gegen Koffein und Antimykotika verleiht. Ebenso werden Zellen mit künstlich erhöhtem Raf1 resistenter gegen Fluconazol und Clotrimazol, gebräuchliche Antimykotika. Umgekehrt wird Heterochromatin instabil und epigenetisches Gedächtnis schwächer, wenn Raf1 durch Hitze oder durch Verlust der TORC2–Gad8‑Signalgebung reduziert wird — sofern Raf1 nicht wiederhergestellt wird. Da Raf1‑ähnliche Proteine, der ClrC‑Komplex und die H3K14ub‑Marke in pathogenen Pilzen und in Säugetieren Gegenstücke haben, deuten diese Ergebnisse darauf hin, dass ein ähnlicher stressüberwachender epigenetischer Knotenpunkt die Medikamentenresistenz, Entwicklung und Erkrankungen in vielen Arten formen könnte.
Warum das wichtig ist
Im Alltag bedeutet diese Arbeit, dass Genstilllegung durch Chromatin kein starres Schloss ist, sondern ein intelligentes, anpassbares System. Zellen nutzen einen zentralen Knotenpunkt, um Umwelthinweise — Temperaturänderungen, Nährstoffstatus, chemische Belastungen — zu lesen und Raf1 hoch- oder herunterzuregeln. Das bestimmt, welcher Teil des Genoms in langanhaltendem Schweigen verhüllt wird und wie leicht Zellen sich ohne DNA‑Mutationen „umprogrammieren“ können. Indem die Studie die Schlüsselrolle der Ubiquitinierung von Histon H3 und der Raf1‑Dosierung aufzeigt, liefert sie eine Blaupause dafür, wie Stress das epigenetische Landschaftsbild rasch umgestalten kann — und weist zugleich auf neue Ansätze hin, die Medikamentenresistenz bei Pilzen oder fehlerhafte Genstilllegung bei Menschen zu beeinflussen.
Zitation: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
Schlüsselwörter: Heterochromatin, epigenetische Vererbung, Histon‑Ubiquitinierung, Stressanpassung, Pilz‑Medikamentenresistenz