Clear Sky Science · de
Biomimetische Vesikel aus modifizierten Tumorzellen als personalisierte Impfstoffe für die postoperative Krebsimmuntherapie
Aus Tumorresten eine zweite Verteidigungslinie machen
Für viele Menschen mit soliden Tumoren ist die Operation nur die erste Runde in einem langen Kampf. Selbst wenn der Großteil eines Tumors entfernt wird, können winzige Zellhaufen entkommen und später tödliche Metastasen bilden. Diese Studie untersucht einen einfallsreichen Weg, die Tumorzellen des Patienten in einen personalisierten Impfstoff zu verwandeln, der darauf ausgelegt ist, diese Überreste nach der Operation aufzuspüren und dem Immunsystem zu helfen, ein Wiederauftreten des Krebses zu verhindern.
Warum verbleibende Krebszellen so schwer zu beseitigen sind
Standardbehandlungen haben Probleme mit den Zellen, die nach der chirurgischen Entfernung der Haupttumormasse verbleiben. Diese verstreuten Zellen verstecken sich oft in entfernten Organen und sind vor Medikamenten und Immunangriffen geschützt. Bestehende immunbasierte Vakzine versuchen, den Körper über spezielle Immunzellen, die dendritischen Zellen, auf Tumormarker zu schulen, doch diese lebenden Impfstoffe sind schwer herzustellen, erreichen Schlüsselorgane des Immunsystems nicht effizient und haben in der Klinik nur mäßige Vorteile gezeigt. Eine zentrale Herausforderung ist, dass jeder Tumor eines Patienten eine einzigartige Mischung von Mutationen trägt, sodass Einheitslösungen wichtige Ziele oft verfehlen.
Ein verborgener Schalter, der Krebszellen sichtbarer macht
Die Forschenden suchten zunächst nach natürlichen Schaltern im Immunsystem, die Zellen besser darin machen, ihr Inneres den Wächterzellen des Immunsystems zu zeigen. Sie konzentrierten sich auf ein Protein namens Syntaxin 11, das normalerweise in Immunzellen reichlich vorhanden, in vielen Tumoren jedoch selten ist. Durch Erhöhen dieses Proteins in aggressiven Brustkrebszellen aus Mausmodellen stellten sie fest, dass die Krebszellen anfingen, sich mehr wie professionelle Immunwächter zu verhalten: Sie zeigten höhere Mengen molekularer „Namensschilder“ und Hilfssignale auf ihrer Oberfläche. Effektiv wurden die Tumorzellen so umprogrammiert, dass sie dem Immunsystem mehr ihrer einzigartigen Merkmale offenbaren statt sie zu verbergen.
Kleine nachgeahmte Immunboten bauen
Mit diesen umprogrammierten Tumorzellen entfernte das Team deren Außenmembranen und nutzte sie, um biologisch abbaubare Nanopartikel zu umhüllen, die ein kleines immunstimulierendes Mittel enthielten. Das Ergebnis war eine Schar nanoskaliger Bläschen, von denen jedes die vollständige Sammlung der Tumormarker sowie eingebaute Aktivierungssignale für cytotoxische T‑Zellen trug. Nach subkutaner Injektion in Mäuse nach der Operation gelangten diese Vesikel effizient in nahegelegene Lymphknoten, wo Immunzellen geschult werden. Dort konnten sie sowohl direkt cytotoxische T‑Zellen aktivieren als auch von natürlichen Immunwächtern aufgenommen werden, die die Antwort weiter verstärkten. Experimente zeigten, dass T‑Zellen, die diesen Vesikeln ausgesetzt waren, sich stärker vermehrten und Krebszellen besser zerstörten als solche, die durch einfachere Nanopartikel-Designs primiert worden waren.
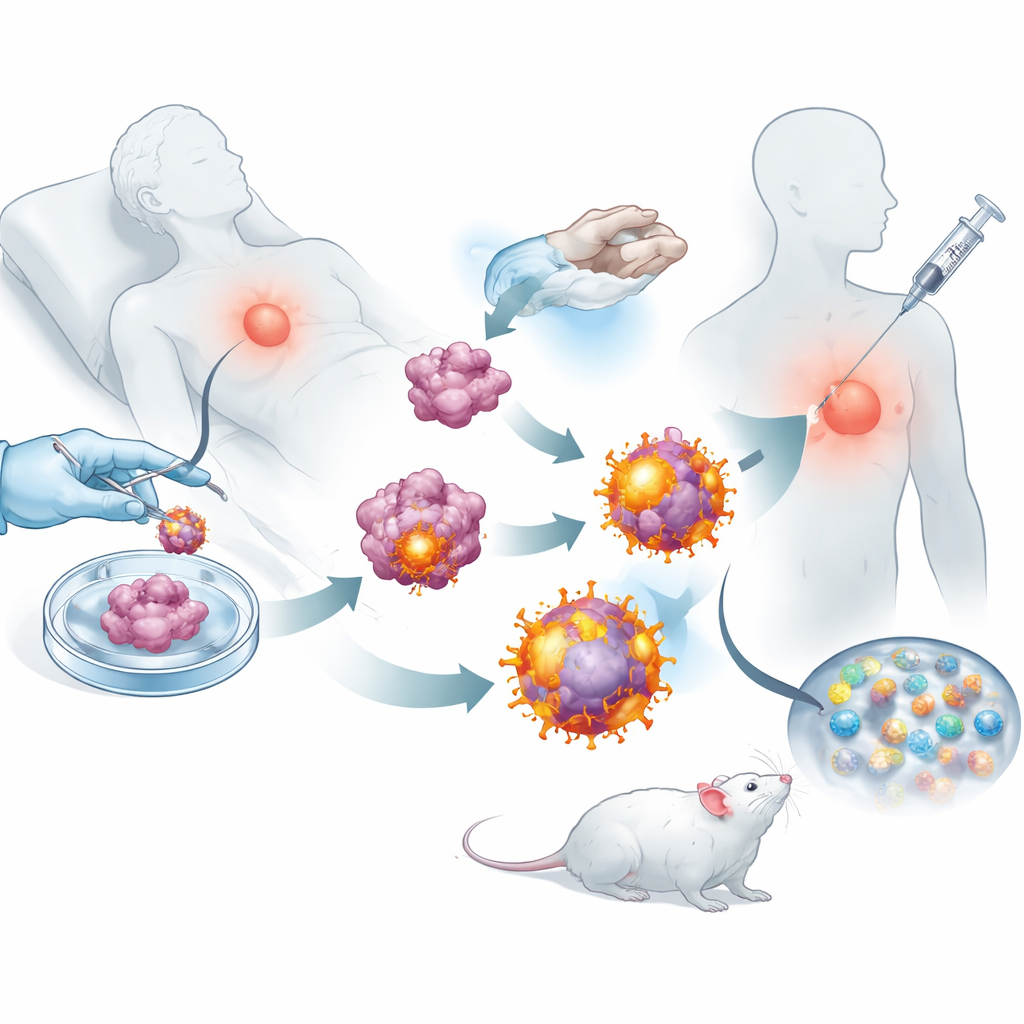
Krebs nach einer Operation fernhalten
In mehreren Mausmodellen von Brustkrebs und Melanom prüften die Forschenden, ob dieser maßgeschneiderte Impfstoff den Krankheitsverlauf tatsächlich verändern kann. In Tieren, bei denen der Großteil eines Brusttumors chirurgisch entfernt worden war, entwickelten geimpfte Mäuse kleinere Rezidive und deutlich weniger Lungenmetastasen als unbehandelte Tiere. Lymphknoten, Milz und Tumoren behandelter Mäuse wimmelten vor aktiven cytotoxischen T‑Zellen und langlebigen Gedächtniszellen, was darauf hindeutet, dass das Immunsystem sowohl geweckt als auch langfristig trainiert wurde. In Kombination mit einem zugelassenen Checkpoint‑Blocker‑Antikörper, der verhindert, dass Tumoren T‑Zellen lahmlegen, führte der Impfstoff zu dauerhafter Tumorkontrolle und in vielen Mäusen zu vollständiger Regression und langfristigem Überleben.
Eine personalisierte Behandlung beschleunigen
Ein Hindernis für die Umsetzung dieses Konzepts in eine Praxistherapie ist die Zeit: Genbasierte Methoden zur Umprogrammierung von Tumorzellen können langsam sein. Um dem zu begegnen, screente das Team natürliche Verbindungen und entdeckte Deoxypodophyllotoxin, ein kleines Molekül, das schnell die Spiegel des Schlüsselproteins und derselben immunstimulierenden Oberflächenmarker erhöht. Mit diesem Abkürzungsweg konnten sie ähnliche vesikelbeschichtete Nanopartikel in kürzerer Zeit herstellen und gleichzeitig ihre Fähigkeit bewahren, starke, tumorspezifische Immunantworten hervorzurufen. Tests zeigten, dass Impfstoffe, die mit diesem Wirkstoff hergestellt wurden, genauso wirksam waren wie die mit der genbasierten Methode erzeugten, und ihre Vorteile hingen davon ab, den richtigen Tumortyp zu erkennen, statt von einer allgemeinen Vergiftung der Krebszellen.
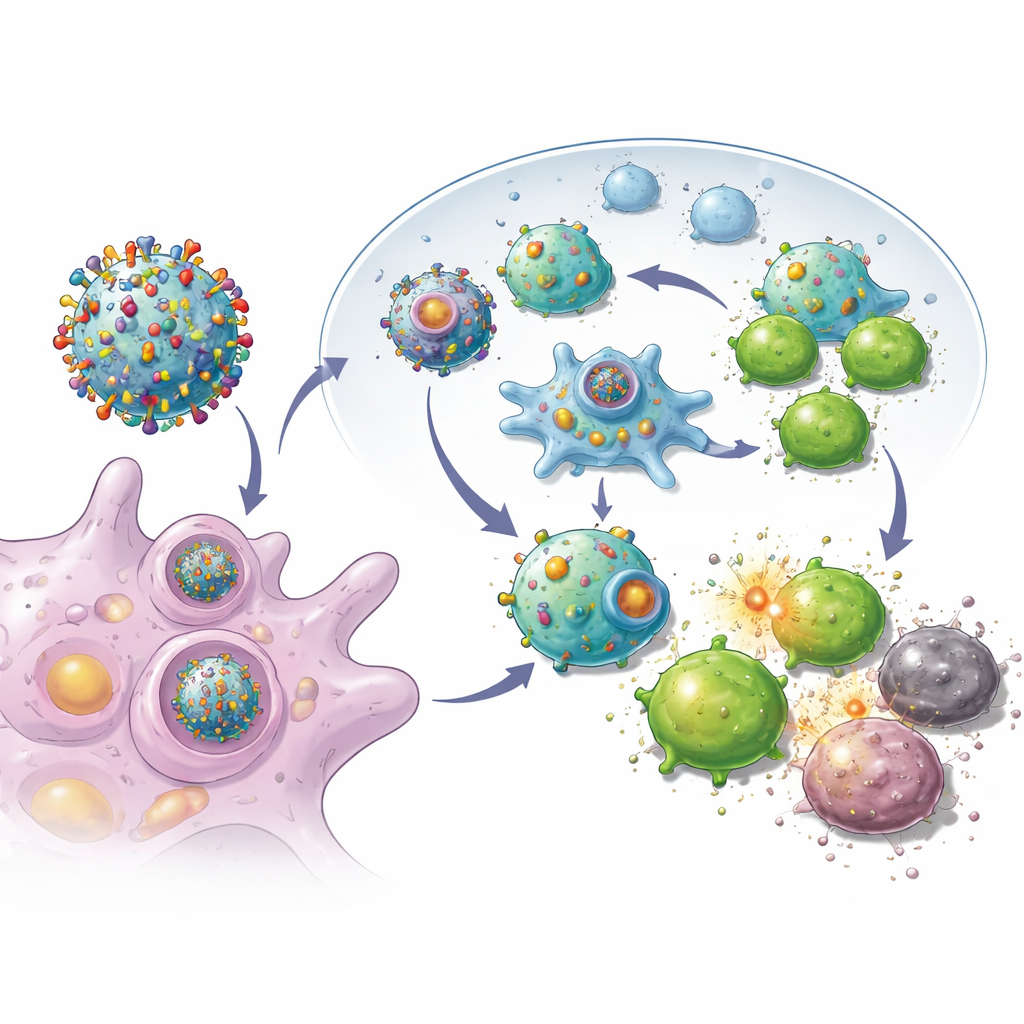
Was das für die künftige Krebsbehandlung bedeuten könnte
Für Nicht‑Spezialisten lautet die Kernaussage, dass der eigene Tumor eines Patienten in ein Miniatur‑Trainingsinstrument für das Immunsystem umgewandelt werden kann. Indem man Krebszellen in Quellen reichhaltiger, personalisierter Informationen verwandelt und diese Informationen auf robuste nanoskopische Träger verpackt, zielt dieser Ansatz darauf ab, Zellen aufzusammeln, die bei der Operation zurückbleiben, und neue Herde am Entstehen zu hindern. Obwohl viele Schritte nötig sind, bevor solche Impfstoffe routinemäßig angeboten werden können — darunter der Nachweis von Sicherheit und Wirksamkeit bei menschlichen Tumoren und der Aufbau zuverlässiger Produktionsketten — zeichnet diese Arbeit einen Weg zu hochgradig individualisierten postoperativen Behandlungen, die die Abwehrkräfte des Körpers mobilisieren, um das zu beenden, was der Chirurg begonnen hat.
Zitation: Yu, P., Jin, Z., Meng, L. et al. Biomimetic vesicles engineered from modified tumour cells act as personalized vaccines for post-surgical cancer immunotherapy. Nat. Nanotechnol. 21, 443–454 (2026). https://doi.org/10.1038/s41565-025-02113-w
Schlüsselwörter: Krebsimpfstoff, Immuntherapie, Nanomedizin, postoperative Behandlung, personalisierte Onkologie