Clear Sky Science · de
Auflösung der strukturellen Integrität von DNA-Origami und der Pharmakokinetik in vivo
Kleine DNA-Maschinen im Körper beobachten
DNA lässt sich wie Papier zu winzigen dreidimensionalen Formen falten – eine Technik, die als DNA-Origami bekannt ist. Diese Nanostrukturen können so programmiert werden, dass sie Medikamente, Impfstoffe oder Signalstoffe mit hoher Präzision transportieren. Aber bleiben sie nach der Injektion in den Körper lange genug intakt, um zu wirken, oder zerfallen sie schnell? Dieser Artikel stellt eine neue Methode vor, um diese DNA-Maschinen in lebenden Tieren zu beobachten, und zeigt, wie lange sie überleben, wie sie sich im Blutstrom bewegen und selbst, welche Teile jeder Struktur zuerst versagen.
Warum gefaltete DNA die Medizin verändern könnte
DNA-Origami nutzt dieselben Basenpaarungsregeln, die unsere genetische Information speichern, verwendet sie jedoch neu, um nanoskalige Objekte zu bauen. Forschende können Proteine, Medikamente oder immunstimulierende Signale auf diesen Objekten anordnen wie Noppen auf einer Lego-Platte und so hoch kontrollierte Therapien gegen Krebs, Autoimmunerkrankungen und Infektionen schaffen. Damit solche präzisen Behandlungen sicher und wirksam sind, müssen Aufsichtsbehörden und Wissenschaftler wissen, wie intakt diese Strukturen im Körper bleiben und wie schnell sie eliminiert werden – zusammengefasst als Pharmakokinetik. Bestehende Nachverfolgungsmethoden befestigen meist fluoreszierende Farbstoffe oder zählen einfach DNA-Fragmente, sodass zerfallene Überreste wie vollständig intakte Nanostrukturen erscheinen können. Bisher gab es keine praktikable Methode, um in lebenden Tieren festzustellen, ob die ursprünglichen DNA-Origami-Formen selbst noch ganz sind.
Ein molekularer „Integritätstest“ für DNA-Origami
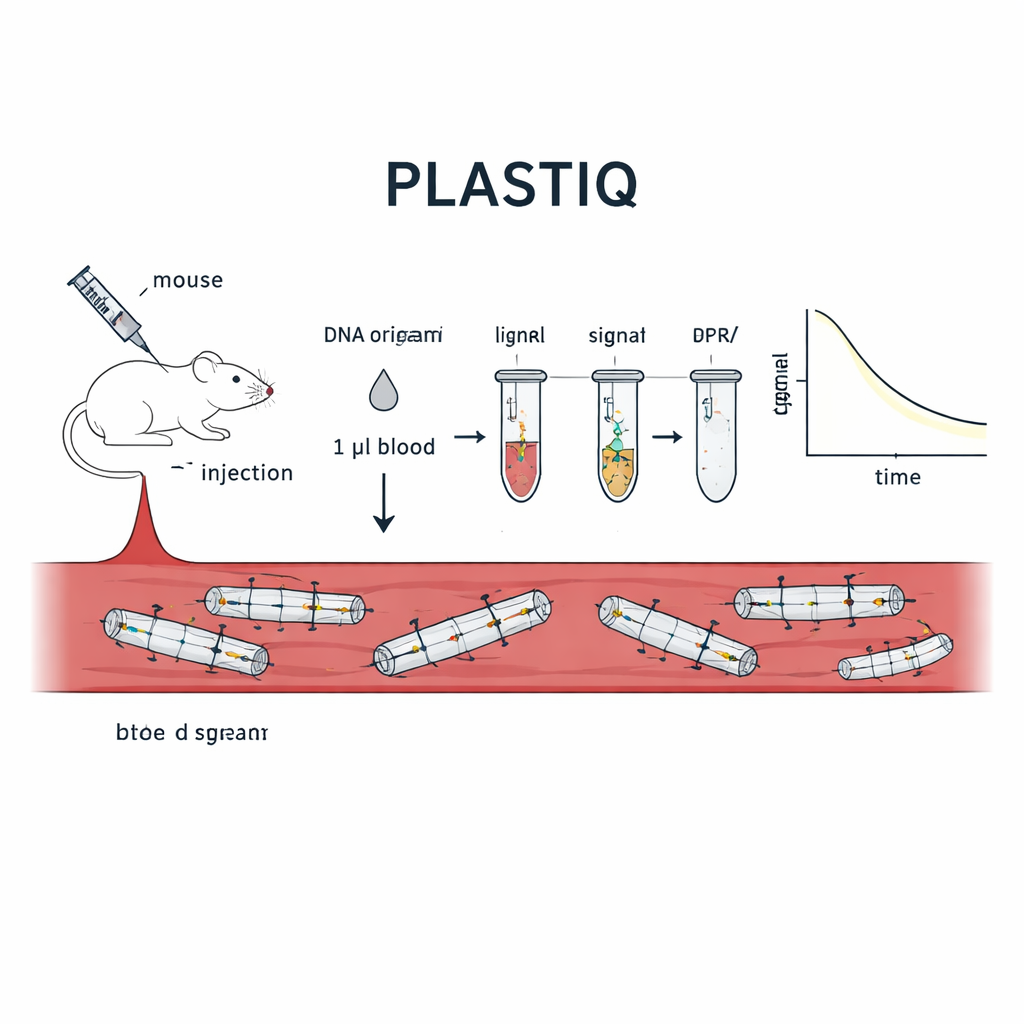
Das Team entwickelte eine Methode, die sie PLASTIQ nennen, kurz für proximity ligation assay for structural tracking and integrity quantification. Die zentrale Idee ist, dem DNA-Origami die eigene Zustandsmeldung zu überlassen. An definierten Positionen jeder Struktur platzieren die Forschenden Paaren kurzer DNA-Staples, die Schulter an Schulter entlang einer Helix liegen, wenn das Origami richtig gefaltet ist. Eines jedes Paares trägt eine kleine chemische Markierung, die ein enzymatisches Verbinden, also Ligieren, erlaubt – aber nur, wenn sie durch einen intakten Gerüststrang nahe beieinandergehalten werden. Schmilzt die Struktur, bricht sie oder wird sie durch Enzyme abgebaut, driften diese zwei Stücke auseinander und können nicht mehr ligiert werden. Nach der Ligierung werden die verbundenen Paare mittels standardmäßiger Polymerase-Kettenreaktion amplifiziert und durch empfindliche qPCR oder Sequenzierung quantifiziert, wodurch das Vorhandensein intakter lokaler Segmente aus wenigen Mikrolitern Blut in messbare Signale verwandelt wird.
Den Test in lebenden Mäusen anwenden
Um zu zeigen, dass PLASTIQ tatsächlich die strukturelle Integrität misst, wandten die Autorinnen und Autoren die Methode zunächst auf einfache, stabförmige DNA-Origami-Designs in Reagenzgläsern an. Signale tauchten nur auf, wenn die Stäbe intakt waren, und verschwanden nach hitzebedingtem Entfalten, während herkömmliche DNA-basierte Tests DNA unabhängig von der Form weiterhin registrierten. Danach injizierten sie diese Stäbe Mäusen auf verschiedenen Wegen – direkt in die Blutbahn, in die Bauchhöhle, in Muskelgewebe und unter die Haut – und entnahmen zu unterschiedlichen Zeiten nur einen Mikroliter Blut. PLASTIQ zeigte, wie die Konzentration intakter Strukturen je nach Injektionsweg anstieg und dann wieder abfiel, entsprechend den allgemeinen Erwartungen aus der Arzneimittelpharmakologie, jedoch mit deutlich feinerer struktureller Auflösung. Die Methode war bis 0,01 Femtomolar empfindlich und benötigte dennoch nur minimale Blutmengen, was wiederholte Probenahmen am selben Tier über Stunden hinweg ermöglichte.
Schutzbeschichtungen und verborgene Schwachstellen testen
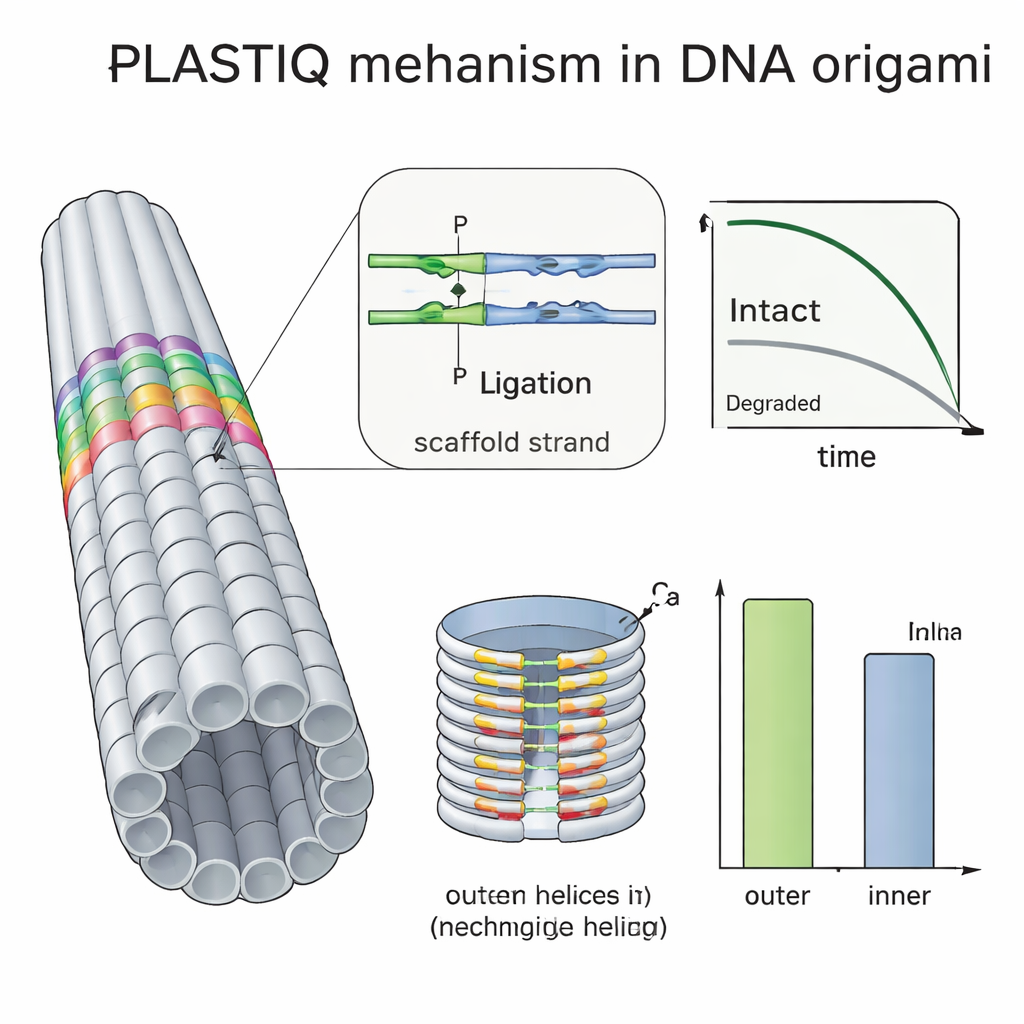
Viele Arbeitsgruppen versuchen, DNA-Origami durch Beschichtungen mit Polymeren wie PEG, durch Quervernetzen der Stränge mit ultraviolettem Licht oder durch Zusatz chemischer Bindemittel zu schützen, doch es war schwer nachzuweisen, wie sehr diese Tricks in vivo tatsächlich helfen. Mit PLASTIQ zeigten die Autorinnen und Autoren, dass PEG-beschichtete Stäbe im Blutkreislauf etwas länger intakt bleiben als unbeschichtete, aber im Kreislauf auch schneller eliminiert werden, und dass die Beschichtung die enzymatischen Schritte von PLASTIQ nicht verhindert. Durch die Kombination von PLASTIQ mit einfachen mathematischen Modellen konnten sie Absorptions- und Eliminationsraten für verschiedene Injektionswege und Beschichtungen ableiten und sogar wiederholte Dosierungsschemata simulieren. Sie erweiterten die Methode weiter mit einem doppelwandigen, fassförmigen Origami, das innen dichter gepackt war als außen. PLASTIQ-Messungen zeigten, dass Staples an der exponierten Außenseite schneller an Integrität verloren als solche zur Innenseite gewandt, und bestätigten damit direkt, dass eingebettete Helices vor abbauenden Enzymen im Blut geschützt sind.
Folgen für zukünftige DNA-basierte Therapien
Für Nichtfachleute lässt sich PLASTIQ als struktureller Check-up für nanoskalige DNA-Geräte verstehen, die durch den Körper reisen. Anstatt nur zu fragen „Ist hier DNA vorhanden?“, fragt die Methode „Ist diese DNA noch in das präzise Objekt gefaltet, das wir entworfen haben?“. Indem sie diese Frage mit hoher Empfindlichkeit aus winzigen Blutproben beantwortet, bietet PLASTIQ Arzneimittelentwicklern ein Werkzeug, um Design, Beschichtung und Dosierung von DNA-Origami-basierten Medikamenten und Impfstoffen zu optimieren. Im Laufe der Zeit könnten solche detaillierten, quantitativen Einblicke in das Verhalten dieser Nanostrukturen in realen biologischen Umgebungen dazu beitragen, DNA-Origami von einem eleganten Laborprinzip in verlässliche, von Behörden akzeptierbare Therapeutika zu überführen.
Zitation: Wang, Y., Rocamonde-Lago, I., Waldvogel, J. et al. Resolving DNA origami structural integrity and pharmacokinetics in vivo. Nat. Nanotechnol. 21, 268–276 (2026). https://doi.org/10.1038/s41565-025-02091-z
Schlüsselwörter: DNA-Origami, Nanomedizin, Arzneimittelabgabe, Pharmakokinetik, Nanotechnologie