Clear Sky Science · de
Die Störung der Tryptophanase fördert Insekten–Bakterien‑Mutualismus
Wie winzige Darmpartner ein Insekt machen oder zerstören können
Viele Tiere, einschließlich Menschen, sind auf Billionen Mikroben im Darm angewiesen. Diese verborgenen Partner helfen bei der Verdauung, stellen Vitamine her oder machen uns in manchen Fällen krank. Die vorliegende Studie untersucht eine einfache, aber überraschende genetische Veränderung bei Bakterien, die ein gewöhnliches Mikrobenexemplar in einen lebensrettenden Partner für einen pflanzenfressenden Stinkkäfer verwandelt. Indem sie sich auf ein einzelnes bakterielles Gen konzentriert, zeigt die Arbeit, wie eine mikroskopische Änderung eine stabile Freundschaft zwischen sehr unterschiedlichen Lebensformen in Gang setzen kann.
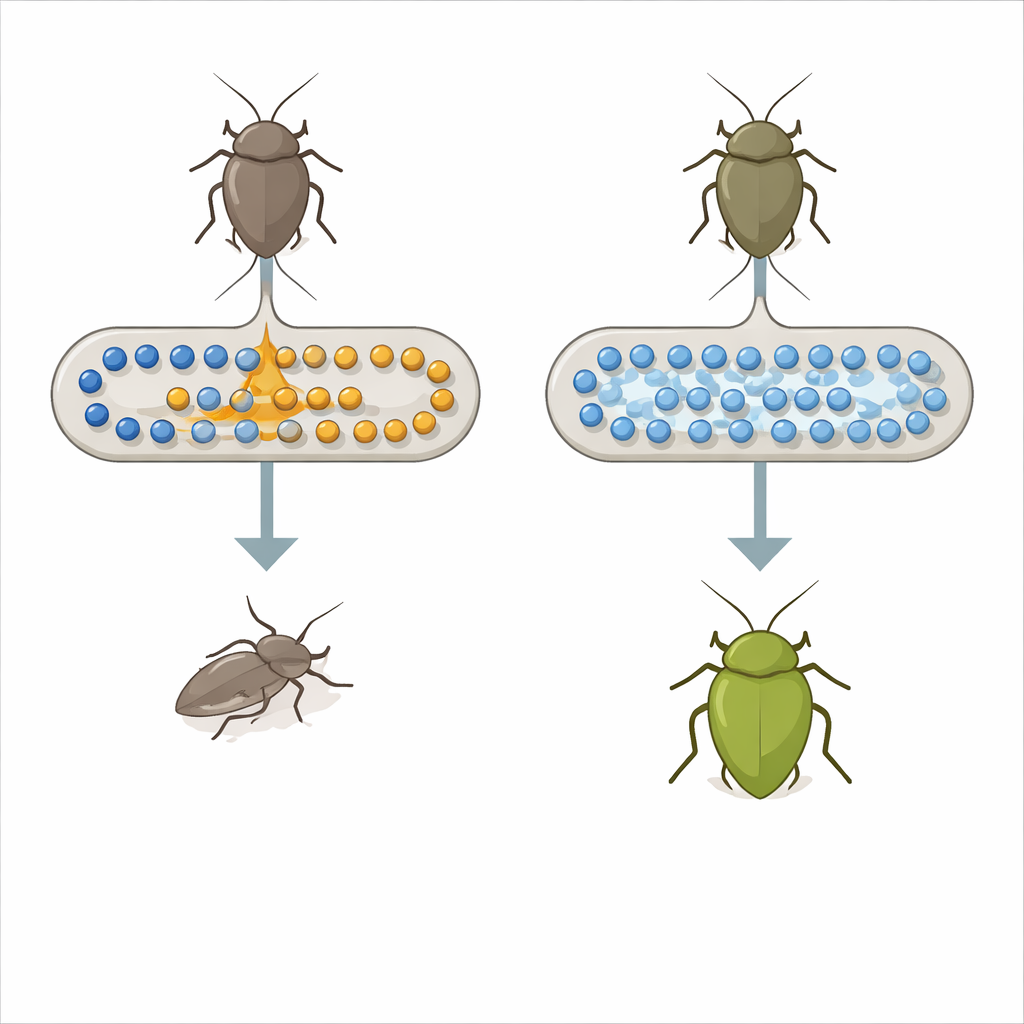
Ein Käfer, ein Bakterium und eine unwahrscheinliche Allianz
Der Stinkkäfer Plautia stali ist auf spezielle Bakterien in einer Tasche seines Mitteldarms angewiesen, um zu wachsen und zu überleben. In der Natur gehören diese Partner meist zur Gattung Pantoea, die Nährstoffe liefern, die das Insekt allein aus Pflanzensaft nicht beziehen kann. Laborversuche hatten bereits gezeigt, dass ein verbreiteter Laborstamm von Escherichia coli, ein typischer Säugetier‑Darmbewohner, sich nach nur einer einzigen Mutation in einem globalen Kontrollsystem namens Kohlenstoffkatzabolitrepression (carbon catabolite repression) rasch zu einem hilfreichen Partner dieses Stinkkäfers entwickeln kann. Dieser frühere Befund warf eine große Frage auf: Entstehen nützliche Symbiosen in der Natur wirklich durch so drastische regulatorische Änderungen, oder gibt es einen fokussierteren genetischen Schalter?
Der Spur eines einzelnen Bausteins folgen
Um das zu klären, verglichen die Forschenden Stinkkäfer mit gewöhnlichem E. coli und solche mit den entwickelten, hilfreichen E. coli‑Mutanten. Sie bestimmten zahlreiche kleine Moleküle im Insektenblut und -darm. Ein essentielles Aminosäuremolekül, Tryptophan, stach heraus: Seine Konzentration war in Insekten mit den hilfreichen Mutanten mehr als zehnmal so hoch wie in solchen mit normalem E. coli. Unter Dutzenden bakterieller Gene, die von der früheren regulatorischen Mutation beeinflusst wurden, standen zwei mit der Tryptophanverarbeitung in Verbindung. Eines, tnaA genannt, produziert ein Enzym, das Tryptophan in die Verbindung Indol und andere Abbauprodukte spaltet; das andere hilft beim Transport von Tryptophan in die Zelle. Als das Team das tnaA‑Gen aus E. coli entfernte, ging es den Stinkkäfern plötzlich deutlich besser: Die Überlebensraten stiegen und die Tiere zeigten eine satte grüne Körperfarbe, typisch für gesunde, gut ernährte Insekten.
Wenn weniger Zerstörung mehr Hilfe bedeutet
Die entscheidende Änderung war nicht, dass die Bakterien mehr Tryptophan herstellten, sondern dass sie aufhörten, es zu zerstören und überschüssiges Indol zu produzieren. Insekten mit tnaA‑defizienten E. coli wiesen hohe Tryptophan‑ und nahezu kein Indolniveau im Körper auf. Im Gegensatz dazu hatten Insekten mit normalem E. coli wenig Tryptophan und deutlich mehr Indol. Fütterungsversuche stützten dieses Bild: Indol im Trinkwasser schadete den Insekten, besonders denen mit indolproduzierenden Bakterien, während zusätzliches Tryptophan nur dann schädlich war, wenn die Bakterien es in vermehrtes Indol umwandeln konnten. Ein separater E. coli‑Stamm, der zur Überproduktion von Tryptophan konstruiert worden war, brachte den Käfern einen moderaten Vorteil, was die Idee untermauert, dass mehr dieses Bausteins und weniger toxisches Abbauprodukt die Gesundheit des Insekts verbessert.
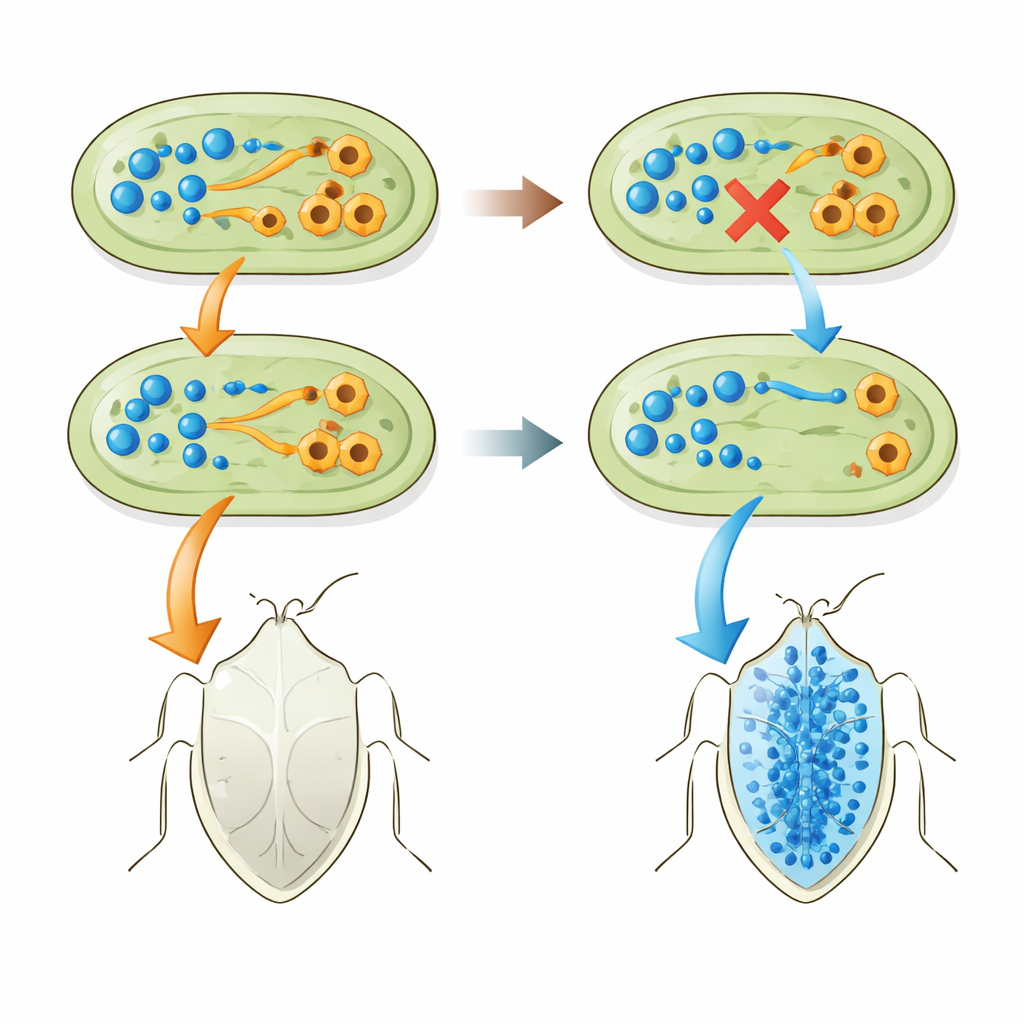
Natürliche Partner teilen denselben genetischen Verlust
Die Forschenden fragten dann, ob derselbe Genverlust auch in natürlichen Symbiosen vorkommt. Sie sequenzierten Genome vieler Pantoea‑Bakterien, die in P. stali und verwandten Stinkkäfern auf den Ryukyu‑Inseln Japans leben, sowie Pantoea‑Stämme aus Bodenproben, die man ins Labor bringen und dazu bringen konnte, die Käfer zu unterstützen. Auffällig war, dass jeder erfolgreiche oder potenziell erfolgreiche Symbiont das tnaA‑Gen nicht besaß und keine Aktivität des tryptophanspaltenden Enzyms zeigte. Dagegen konnten mehrere frei lebende Pantoea ananatis‑Stämme, die noch tnaA trugen, die Entwicklung der Stinkkäfer überhaupt nicht unterstützen. Als die Forschenden tnaA in einem dieser P. ananatis‑Stämme ausschalteten, verbesserte sich dessen Fähigkeit, den Insekten zu helfen, wenn auch nicht auf das Niveau natürlicher Partner. Und als sie einem natürlichen Symbionten ein aktives tnaA‑Operon aufzwangen, ging es den Insekten schlechter: Sie hatten weniger Tryptophan und mehr Indol im Blut.
Was das für verborgene Lebenspartnerschaften bedeutet
Zusammengefasst deuten die Ergebnisse auf eine einfache, aber wirkungsvolle Regel: Bakterien, die aufhören, Tryptophan abzubauen und damit vermeiden, ihren Wirt mit Indol zu überfluten, werden eher zu verlässlichen Partnern pflanzenfressender Stinkkäfer. Im Labor kann dies durch eine Mutation in einem globalen Regulationssystem ausgelöst werden; in der Natur zeigt es sich als direkter Verlust des tryptophanspaltenden Gens selbst. So oder so hilft das Abschalten dieses einen Enzyms, die Interessen von Insekt und Mikrobe in Einklang zu bringen. Die Studie legt nahe, dass der Weg von loser Assoziation zu enger Mutualismus manchmal auf überraschend kleinen genetischen Schritten beruhen kann und dass ähnliche Funktionsverluste im bakteriellen Stoffwechsel vielen anderen verborgenen Allianzen im Baum des Lebens zugrunde liegen könnten.
Zitation: Wang, Y., Moriyama, M., Koga, R. et al. Tryptophanase disruption promotes insect–bacterium mutualism. Nat Microbiol 11, 759–769 (2026). https://doi.org/10.1038/s41564-026-02264-z
Schlüsselwörter: Insektenmikrobiom, bakterieller Mutualismus, Tryptophan‑Stoffwechsel, Evolution der Symbiose, Pantoea‑Symbionten