Clear Sky Science · de
mRNA-Impfung überwindet haemozoin-vermittelte Beeinträchtigung von Ganzparasit-Malariaimpfstoffen bei Mäusen
Warum frühere Malaria Impfstoffe weniger wirksam macht
Malaria tötet jährlich hunderte Tausende von Menschen, und einer der vielversprechendsten Impfansätze nutzt ganze, abgeschwächte Parasiten, um das Immunsystem zu trainieren. Merkwürdigerweise funktioniert dieser „Goldstandard“-Ansatz deutlich besser bei Menschen, die nie Malaria hatten, als bei denen, die in Endemiegebieten aufgewachsen sind. Diese Studie an Mäusen stellt eine einfache, aber entscheidende Frage: Was ist es an früheren Malariainfektionen, das einen sehr wirksamen Impfstoff plötzlich schwächt — und kann ein neuer mRNA-Impfstoff das Problem beheben?
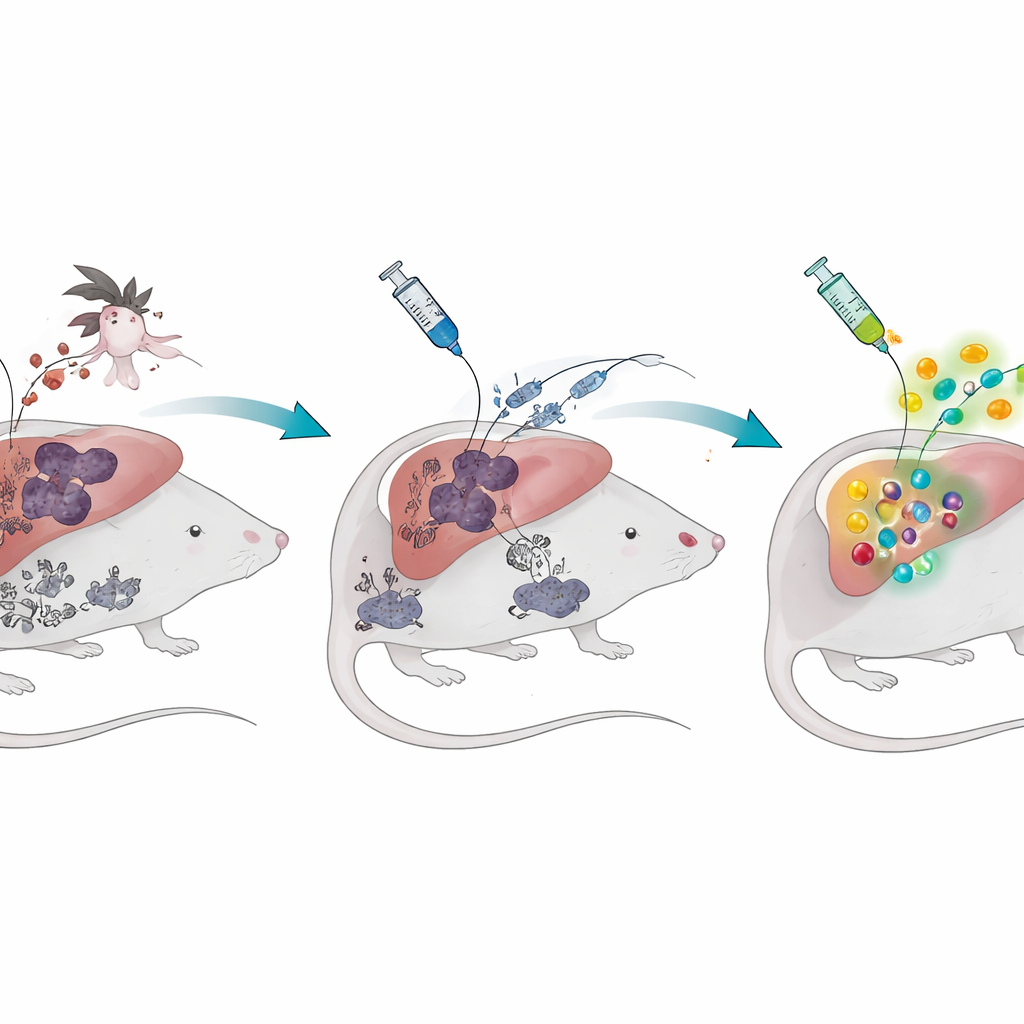
Die zwei Lebensstadien der Malariaparasiten
Der Malariaparasit hat im menschlichen Körper zwei wichtige Stadien. Zuerst, nach einem Mückenstich, infiziert er unauffällig die Leber. Später befällt er die roten Blutkörperchen und verursacht Fieber und Krankheit. Ganzparasit-Impfstoffe, sogenannte bestrahlte attenuierte Sporozoiten, zielen auf das stille Leberstadium: Die Parasiten dringen in Leberzellen ein, können ihren Lebenszyklus aber nicht vollenden, sodass das Immunsystem eine sichere Vorschau erhält. Bei malaria-naiven Mäusen erzeugt diese Strategie große Mengen spezialisierter Killer-T-Zellen, die in der Leber verbleiben und Parasiten beseitigen können, bevor sie Krankheit verursachen. Wenn die Forscher den Mäusen jedoch zuvor eine Blutstadium-Infektion verabreichten und diese abklang, produzierte derselbe Impfstoff deutlich weniger schützende T-Zellen, und die Tiere waren bei einer anschließenden Herausforderung mit lebenden Parasiten deutlich schlechter geschützt.
Ein hartnäckiges Pigment, das nicht verschwindet
Das Team fragte dann, was in diesen „malaria-erfahrenen“ Mäusen anders war. Ein auffälliger Verdächtiger war Hämozoin, ein dunkles, kristallähnliches Pigment, das der Parasit in den roten Blutkörperchen bildet, um das eisenreiche Abfallprodukt der Hämoglobinverdauung zu entgiften. Dieses Pigment verschwindet nicht, wenn die Infektion abklingt; es kann monatelang in Leber, Milz und Knochenmark verbleiben. Die Wissenschaftler fanden, dass Mäuse noch über ein Jahr nach dem Ende einer Blutstadium-Infektion sowohl gespeichertes Hämozoin als auch eine geschwächte T-Zell-Antwort auf den Leberstadium-Impfstoff aufwiesen. Gesunden Mäusen allein gereinigtes synthetisches Hämozoin zu geben — ohne lebende Parasiten — reichte aus, um diese langanhaltende Schwächung des Impfschutzes nachzuahmen und den Schutz gegen eine spätere Malaria-Herausforderung zu reduzieren.
Wie Hämozoin die Immunwächter ausbremst
Vertiefend konzentrierten sich die Forscher auf dendritische Zellen, die Wächter des Immunsystems, die Bruchstücke von Krankheitserregern aufnehmen und T-Zellen präsentieren. Damit der Ganzparasit-Leberimpfstoff wirkt, müssen dendritische Zellen Parasitenmaterial aus infizierten Leberzellen aufnehmen und den Killer-T-Zellen zeigen. In Zellkultur-Experimenten demonstrierte das Team, dass Hämozoin direkt diesen Aufnahme-Schritt stört: Je mehr Hämozoin dendritische Zellen ausgesetzt waren, desto weniger effizient nahmen sie Proteinantigene auf. Dieser Defekt trat sowohl in Maus- als auch in humanen Immunzellen aus Spenderblut auf und hing nicht von einem bekannten Entzündungssensor ab, was darauf hindeutet, dass Hämozoin selbst als physikalische oder biochemische Barriere für die normale Antigenverarbeitung wirkt.
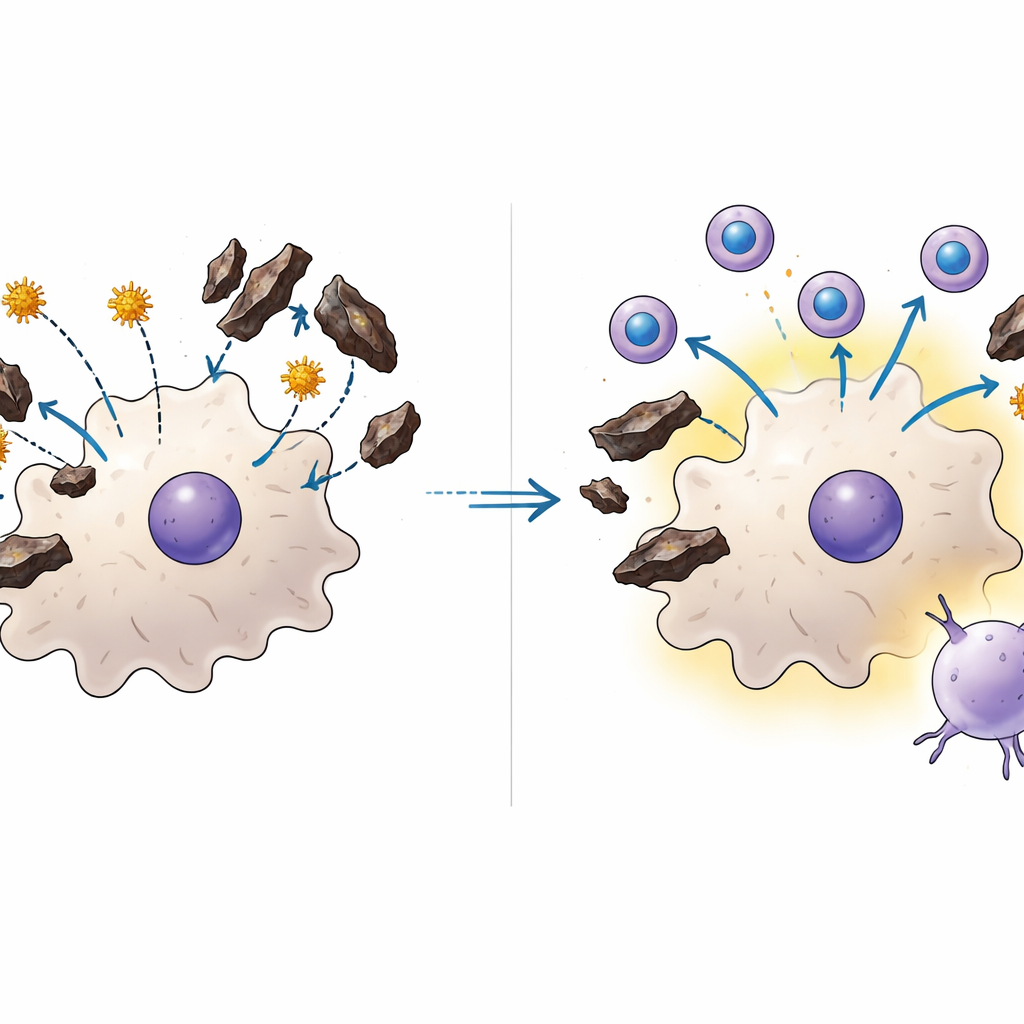
mRNA-Impfstoffe umgehen die Barriere
Um zu prüfen, ob ein anderes Impfstoffformat dieses Problem umgehen könnte, entwickelten die Wissenschaftler einen mRNA-Impfstoff, verpackt in Lipid-Nanopartikeln. Anstatt Parasitenproteine von außen bereitzustellen, gibt dieser Ansatz den Wirtszellen genetische Anweisungen, kurze Abschnitte mehrerer Parasitenproteine innerhalb der Zelle herzustellen. Bei Mäusen mit oder ohne vorausgegangene Malaria erzeugte der mRNA-Impfstoff ähnlich starke Killer-T-Zell-Antworten und verbesserte die Kontrolle der Leberinfektion. Auffällig war, dass in Kombination des mRNA-Impfstoffs mit einer Einzeldosis des Ganzparasit-Leberimpfstoffs Mäuse besonders große Pools von T-Zellen aufbauten, die langfristig in der Leber sesshaft wurden — eine Zellpopulation, die als Schlüssel für schnellen Schutz bekannt ist. In Zellkulturen blockierte Hämozoin weder die Aufnahme noch die Funktion der mRNA-beladenen Nanopartikel, was erklärt, wie diese Strategie dort erfolgreich sein kann, wo der ältere Impfstoff allein versagt.
Was das für zukünftige Malaria-Impfungen bedeutet
Vereinfacht gesagt zeigt die Studie, dass frühere Malariainfektionen mikroskopisch kleine, mineralähnliche Rückstände hinterlassen, die die Art und Weise verstopfen, wie bestimmte Immunzellen normalerweise aus Impfstoffen lernen, und so einen führenden Ganzparasit-Malariaimpfstoff abschwächen. Durch den Wechsel zu einem mRNA-basierten Impfstoff — oder dessen Kombination mit einem solchen —, der die Bauanleitung für Parasitenfragmente direkt in Zellen einschleust, können Wissenschaftler diese Rückstände umgehen und starken Schutz in malaria-erfahrenen Wirten wiederherstellen — zumindest bei Mäusen. Die Arbeit macht Hämozoin als wichtigen Hindernisfaktor für Impfstoffe bei in Endemiegebieten lebenden Menschen sichtbar und legt nahe, dass sorgfältig konzipierte mRNA- oder kombinierte Impfregime ein vielversprechender Weg zu wirksameren, breit einsetzbaren Malaria-Immunisierungen sein könnten.
Zitation: Hassert, M., Drewry, L.L., Pewe, L.L. et al. mRNA vaccination overcomes haemozoin-mediated impairment of whole-parasite malaria vaccines in mice. Nat Microbiol 11, 718–730 (2026). https://doi.org/10.1038/s41564-026-02263-0
Schlüsselwörter: Malariaimpfstoffe, Hämozoin, mRNA-Impfstoff, T-Zell-Immunität, Plasmodium-Infektion