Clear Sky Science · de
Erstlokalisationen des SIV-Wiederauftretens nach Absetzen antiretroviraler Therapie bei Rhesusaffen
Warum das Virus zurückkehrt
Moderne HIV-Medikamente können die Virusmenge im Blut so stark senken, dass Standardtests nichts nachweisen. Wenn die Behandlung jedoch stoppt, kehrt das Virus fast immer zurück. Diese Studie an Rhesusaffen, die mit einem nahen Verwandten von HIV namens SIV infiziert waren, stellt eine grundlegende, aber entscheidende Frage: Wo genau entzündet sich in erster Linie dieses virale Wiederaufleben im Körper, und welche Gewebearten entfachen daraus ein größeres Aufflammen?
Dem viralen Barcode folgen
Um das Virus mit ungewöhnlicher Präzision zu verfolgen, nutzten die Forschenden ein spezielles SIV, bei dem jedes Viruspartikel einen einzigartigen genetischen „Barcode“ trägt — eine kurze, harmlose Sequenz, die wie eine Seriennummer funktioniert. Vierundzwanzig Makaken wurden mit einem Gemisch aus Tausenden dieser barcodierten Viren infiziert und dann schnell auf eine starke Dreifach‑antiretrovirale Behandlung gesetzt. Die Medikamente drückten das Virus im Blut auf praktisch nicht nachweisbare Werte und hielten es dort über mehr als ein Jahr, was eine wirksame langfristige HIV-Therapie beim Menschen nachahmt. Weil jeder Barcode eine bestimmte virale Linie markierte, konnte das Team später identifizieren, welche spezifischen Viruslinien beim Absetzen der Therapie wieder aktiv wurden und an welchen Stellen im Körper dieses Erwachen zuerst Fuß fasste.
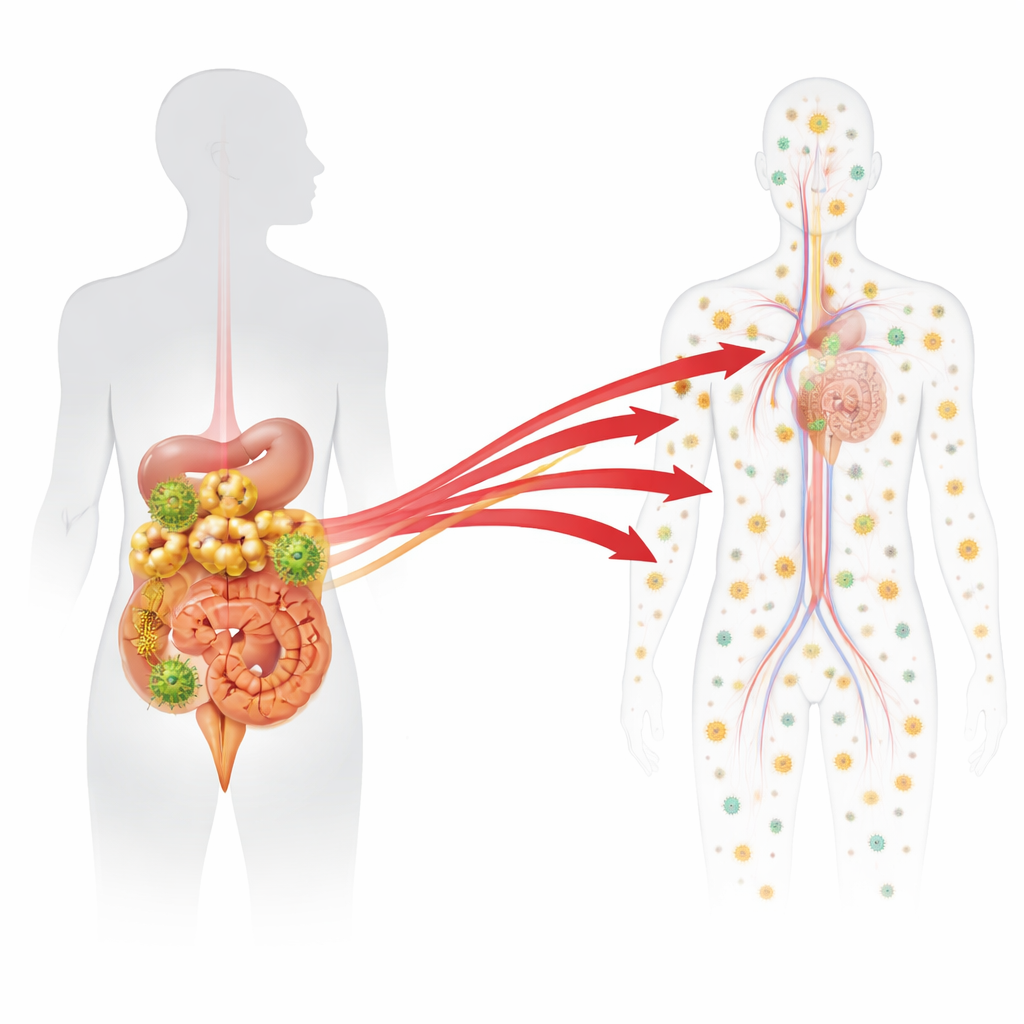
Einblick in Gewebe während und nach der Behandlung
Am Ende der langen Behandlungsphase wurden die Makaken in Gruppen eingeteilt. Einige wurden noch während der Therapie untersucht, um das normale Hintergrundmuster der winzigen Mengen viraler Genmaterialien zu bestimmen, die trotz Medikamenten verbleiben. Andere hatten die Behandlung gestoppt und wurden entweder fünf oder sieben Tage später untersucht, bevor oder gerade als das Virus wieder im Blut aufzutauchen begann. Von jedem Tier sammelten und analysierten die Wissenschaftlerinnen und Wissenschaftler rund 90 Gewebeproben aus dem Darm, verschiedenen Lymphknotenarten, blutbildenden Organen wie dem Knochenmark und nicht‑immunologischen Organen wie Leber und Lunge. Für jedes Gewebe maßen sie, wie viel virale DNA (ein Hinweis auf infizierte Zellen) und virale RNA (ein Hinweis auf aktive Virusproduktion) für jeden Barcode vorhanden war. Anschließend nutzten sie statistische Modelle, um jeden Barcode zu kennzeichnen, dessen RNA‑Level in einem bestimmten Gewebe deutlich über dem zu erwartenden niedrigen Hintergrundniveau während der Behandlung lag.
Die ersten Funken des Rebounds lokalisieren
Diese ungewöhnlich aktiven Barcodes, die die Forschenden als „Ausreißer" bezeichneten, hoben virale Linien hervor, die wahrscheinlich frische Replikationsschübe und lokale Ausbreitung nach Absetzen der Medikamente durchliefen. Über alle Tiere hinweg identifizierten sie 32 solche Ausreißer‑Barcodes. Wichtig ist: Als das Virus im Blut wieder erschien, stimmten etwa die Hälfte der in Plasma gefundenen Barcodes mit diesen Ausreißern in Geweben überein, was spezifische Gewebestellen direkt mit der frühesten Phase des systemischen Rebounds verknüpft. Die meisten Ausreißer tauchten nur in einer einzigen Gewebeprobe auf, was zu einem sehr lokalisierten Ausgangspunkt passt, während ein kleinerer Anteil sich bereits auf benachbarte Darmabschnitte und deren drainierende Lymphknoten ausgebreitet hatte. Nur bei dem einen Tier mit deutlich höheren Viruswerten im Blut sah das Team Hinweise darauf, dass mehrere Gewebe — einschließlich entfernter — bereits wieder besiedelt worden waren. Das deutet auf einen stufenweisen Verlauf hin: zuerst eine stille Zündung an einer Stelle, dann lokale Expansion und schließlich Verbreitung im ganzen Körper.
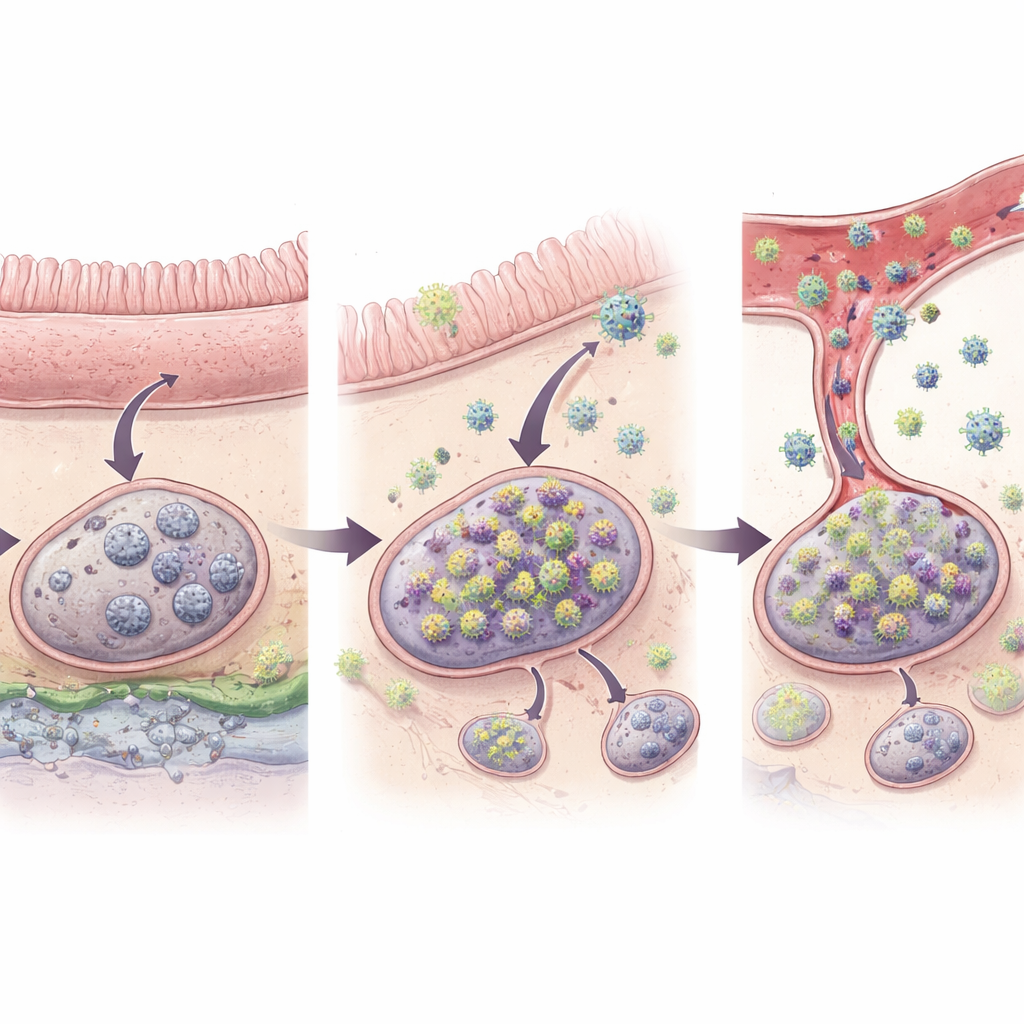
Warum der Darm am wichtigsten ist
Ein Befund stach heraus: Fast alle frühen Rebound‑Ereignisse ließen sich auf den Verdauungstrakt und die ihn versorgenden Immungewebe zurückführen. Von den 27 Barcodes, die als wahre Ursprünge des Rebounds eingestuft wurden, lagen 96 % entweder im Darm selbst oder in darmassoziierten Lymphknoten, etwa den mesenterialen Knoten, die Dünn‑ und Dickdarm entwässern. Nur ein einziger Ursprungsort wurde in einem Lymphknoten gefunden, der nicht mit dem Darm verbunden ist, und in Organen wie Leber, Lunge oder Knochenmark wurde keiner identifiziert. Statistische Analysen zeigten, dass darmassoziierte lymphatische Gewebe, selbst unter Berücksichtigung der Anzahl infizierter Zellen, etwa zehnmal wahrscheinlicher waren als andere lymphatische Orte, zur Entstehung des reboundenden Virus beizutragen. Die einzigartige Umgebung des Darms — ständige Exposition gegenüber Nahrung und Mikroben und häufige Entzündungen bei HIV‑ähnlichen Infektionen — könnte dort infizierte Zellen aktiver halten und leichter dazu bringen, wieder Virus zu produzieren.
Was das für künftige Heilungsstrategien bedeutet
Kurz gesagt, diese Arbeit legt nahe, dass wenn potente HIV‑ähnliche Medikamente abgesetzt werden, das Virus fast immer von wenigen verborgenen Reservoirs im und um den Darm neu startet, und nicht gleichmäßig aus allen Körperregionen. Zu Beginn sind diese Aufflammungen winzig und auf einen Gewebefleck beschränkt, doch sobald das Virus den Blutkreislauf und entfernte Organe erreicht, steigen die Mengen schnell an. Für Bemühungen um langfristige Remission oder Heilung bedeutet das, dass Therapien den Darm und dessen immunologisches Gewebe erreichen und dort wirksam sein müssen. Werkzeuge, die diese schwer zugänglichen Stellen beim Menschen visualisieren oder entnehmen können, oder Medikamente, die gezielt dort wirken, könnten entscheidend sein, um zu verhindern, dass die ersten Funken des Rebounds jemals entfalten.
Zitation: Keele, B.F., Okoye, A.A., Immonen, T.T. et al. Initial sites of SIV rebound after antiretroviral treatment cessation in rhesus macaques. Nat Microbiol 11, 648–663 (2026). https://doi.org/10.1038/s41564-025-02258-3
Schlüsselwörter: HIV-Rebound, virale Reservoirs, lymphatisches Gewebe des Darms, Rhesusaffen-Modell, Unterbrechung antiretroviraler Therapie